磁性纳米四氧化三铁在催化剂、DNA检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米 的流程如下:
的流程如下: 之间,生成
之间,生成 的离子方程式是
的离子方程式是___________ ,采用的加热方式为___________ 。
(2)操作Ⅲ分离 的方法为过滤,所需的玻璃仪器为
的方法为过滤,所需的玻璃仪器为___________ 。
(3)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米 为得到较纯净的纳米
为得到较纯净的纳米 ,
, 与
与 的个数之比最好为
的个数之比最好为___________ 。但实际操作时,却很难控制这一比例,原因是___________ 。
(4)经过多次实验发现,当混合溶液中 时,容易得到理想的纳米
时,容易得到理想的纳米 。烘干后再洗涤,检验纳米
。烘干后再洗涤,检验纳米 是否洗涤干净的实验方法是
是否洗涤干净的实验方法是_________ 。
(5)以太阳能为热源分解 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。
的过程如图所示。_________ 。
A.过程Ⅰ中 为氧化剂
为氧化剂
B.过程Ⅱ中 为氧化产物
为氧化产物
C.铁氧化合物循环制 具有节约能源、产物易分离等优点
具有节约能源、产物易分离等优点
②请写出反应Ⅱ对应的化学方程式_________ 。
 的流程如下:
的流程如下: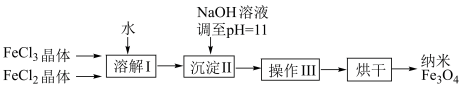
 之间,生成
之间,生成 的离子方程式是
的离子方程式是(2)操作Ⅲ分离
 的方法为过滤,所需的玻璃仪器为
的方法为过滤,所需的玻璃仪器为(3)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米
 为得到较纯净的纳米
为得到较纯净的纳米 ,
, 与
与 的个数之比最好为
的个数之比最好为(4)经过多次实验发现,当混合溶液中
 时,容易得到理想的纳米
时,容易得到理想的纳米 。烘干后再洗涤,检验纳米
。烘干后再洗涤,检验纳米 是否洗涤干净的实验方法是
是否洗涤干净的实验方法是(5)以太阳能为热源分解
 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。
的过程如图所示。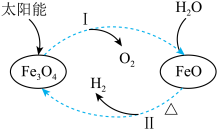
A.过程Ⅰ中
 为氧化剂
为氧化剂B.过程Ⅱ中
 为氧化产物
为氧化产物C.铁氧化合物循环制
 具有节约能源、产物易分离等优点
具有节约能源、产物易分离等优点②请写出反应Ⅱ对应的化学方程式
更新时间:2023-11-04 18:11:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某同学为了探究钠与 的反应,利用如图装置进行实验。
的反应,利用如图装置进行实验。
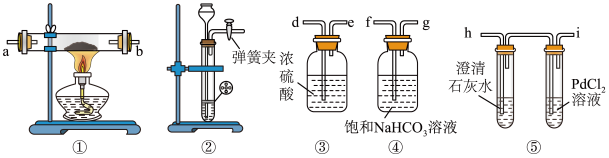
已知: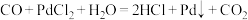 ,Pd是黑色固体。
,Pd是黑色固体。
(1)请将上图各装置连接完整(填写装置中字母):c接f,___接___,__接___,___接___,______ 。
(2)若用稀盐酸与 反应制备
反应制备 ,请写出反应的离子方程式
,请写出反应的离子方程式___________ 。
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让 充满整个装置,当观察到
充满整个装置,当观察到___________ 时再点燃酒精灯。
(4)假如反应过程中有下列两种情况,请根据信息写出化学方程式。
Ⅰ.若装置⑤ 溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,则钠与
溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,则钠与 发生的反应方程式为
发生的反应方程式为___________ 。
Ⅱ.若装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况) 气体,且所得溶液中还有黑色固体残留,装置⑤
气体,且所得溶液中还有黑色固体残留,装置⑤ 溶液中无明显现象,则钠与
溶液中无明显现象,则钠与 发生的反应方程式为
发生的反应方程式为___________ 。
 的反应,利用如图装置进行实验。
的反应,利用如图装置进行实验。
已知:
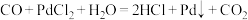 ,Pd是黑色固体。
,Pd是黑色固体。(1)请将上图各装置连接完整(填写装置中字母):c接f,___接___,__接___,___接___,
(2)若用稀盐酸与
 反应制备
反应制备 ,请写出反应的离子方程式
,请写出反应的离子方程式(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让
 充满整个装置,当观察到
充满整个装置,当观察到(4)假如反应过程中有下列两种情况,请根据信息写出化学方程式。
Ⅰ.若装置⑤
 溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,则钠与
溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,则钠与 发生的反应方程式为
发生的反应方程式为Ⅱ.若装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)
 气体,且所得溶液中还有黑色固体残留,装置⑤
气体,且所得溶液中还有黑色固体残留,装置⑤ 溶液中无明显现象,则钠与
溶液中无明显现象,则钠与 发生的反应方程式为
发生的反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
Ⅰ.从海带中提取碘单质,实验流程图如下:
回答下列问题:
(1)在进行步骤①之前,称取mg干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入_____ (填仪器名称)中灼烧至海带完全成灰烬。
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入氯水后颜色变蓝,此反应的离子方程式是_____ ;乙同学认为使用酸化的H2O2溶液能更有利于提取碘,写出离子方程式_____ 。
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是_____ (填字母)。_____ 。
Ⅱ.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
(5)将海水浓缩的方法是_____ 。
(6)步骤②通入热空气吹出Br2,利用了Br2的_____ 性质。
(7)步骤③反应的离子方程式是_____ ,从理论上分析,下列能代替SO2吸收溴的是_____ (填字母)。
A.NaOH B.Na2SO3 C.H2O D.FeCl2
Ⅰ.从海带中提取碘单质,实验流程图如下:
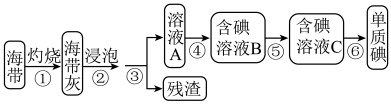
回答下列问题:
(1)在进行步骤①之前,称取mg干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入氯水后颜色变蓝,此反应的离子方程式是
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是
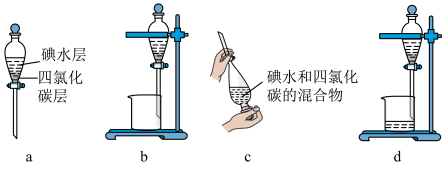
Ⅱ.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
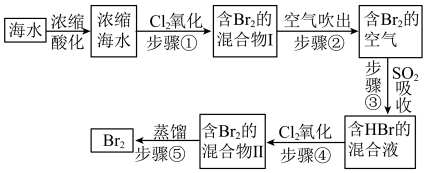
(5)将海水浓缩的方法是
(6)步骤②通入热空气吹出Br2,利用了Br2的
(7)步骤③反应的离子方程式是
A.NaOH B.Na2SO3 C.H2O D.FeCl2
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表是打开物质世界奥秘之门的一把金钥匙 ,1869 年门捷列夫发现了元素周期律并发表了元素周期表,下表是元素周期表的一部分。
(1)上述元素中化学性质最稳定的是_______ (填元素符号,下同 ),最轻的金属_______ 是制造电池的理想物质。
(2)h元素的原子结构示意图为_____ ,写出 h 单质的一种用途______ 。
(3) c、d、As 三种元素的最简单氢化物的稳定性为_____ ; c 、d、f、i 的简单离子半径由大到小顺序是____ 。
(4)e与j 组成的化合物是自然界中常见的矿石一萤石的主要成分,用电子式表示该物质______ 。
(5)元素f与g的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(6)由d、f、i三种元素组成的化合物M的水溶液是一种生活中常见的消毒剂。As可与M的碱性溶液反应,当消耗lmol还原剂时,消耗2.5mol氧化剂,转移5mol电子。则该反应的离子方程式为______ 。
a | |||||||||||||||||
b | c | d | e | ||||||||||||||
f | g | h | i | ||||||||||||||
j | As |
(2)h元素的原子结构示意图为
(3) c、d、As 三种元素的最简单氢化物的稳定性为
(4)e与j 组成的化合物是自然界中常见的矿石一萤石的主要成分,用电子式表示该物质
(5)元素f与g的最高价氧化物对应的水化物反应的化学方程式是
(6)由d、f、i三种元素组成的化合物M的水溶液是一种生活中常见的消毒剂。As可与M的碱性溶液反应,当消耗lmol还原剂时,消耗2.5mol氧化剂,转移5mol电子。则该反应的离子方程式为
您最近一年使用:0次
【推荐1】生活污水中含有大量的有机物和无机含氮化合物。脱氮是污水处理的重要内容之一。下图是生物脱氮的工艺流程图:
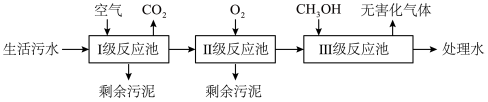
Ⅰ级反应池中有机物被氧化;Ⅱ级反应池中,在pH为8.0~8.4时,硝化细菌将NH4+转化成NO3-,其反应为:NH4++2O2=NO3-+2H++H2O。
(1)请标出该反应的电子转移方向和数目____________ 。
(2)该反应中,被氧化的是_____ ;还原产物是________ 。
(3)在Ⅱ级反应池的反应过程中,需要添加适量的_____ (填“酸性”、“中性”或“碱性”)物质,理由是____________________ 。
(4)Ⅲ级反应池中,在反硝化细菌作用下,同时加入适量CH3OH将NO3-还原,进行无害化处理,其变化可表述为:
___ NaNO3+___ CH3OH---___ +___ Na2CO3___ NaHCO3+___ H2O
请完成上述反应的方程式并配平。

Ⅰ级反应池中有机物被氧化;Ⅱ级反应池中,在pH为8.0~8.4时,硝化细菌将NH4+转化成NO3-,其反应为:NH4++2O2=NO3-+2H++H2O。
(1)请标出该反应的电子转移方向和数目
(2)该反应中,被氧化的是
(3)在Ⅱ级反应池的反应过程中,需要添加适量的
(4)Ⅲ级反应池中,在反硝化细菌作用下,同时加入适量CH3OH将NO3-还原,进行无害化处理,其变化可表述为:
请完成上述反应的方程式并配平。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】化学工业为世界能源消费生产了多种能源物质。
(1)在常温常压下,H2和C3H8的混合气体共3 mol完全燃烧生成CO2和液态水放出2792kJ的热量。
已知:
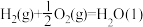 ΔH=-286 kJ·mol-1
ΔH=-286 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220 kJ·mol-1
则该混合气体中,H2和C3H8的体积比为___________ 。
(2)一种利用太阳能将甲烷重整制氢原理的示意图如下:
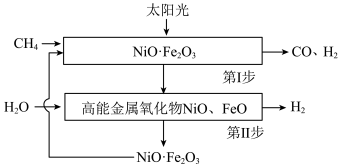
①第Ⅰ步反应的还原剂是___________ 。
②NiO·Fe2O3在整个反应过程中的作用是___________ 。
③反应每消耗1molCH4,理论上可生成标准状况下H2的体积为___________ 。
(3)在催化剂光照条件下,CO2和H2O可转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)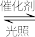 2CH3OH(g)+3O2(g)。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
①用H2O(g)表示0~3min内该反应的平均反应速率为___________ 。
②第4分钟时v逆(CH3OH)___________ (填“大于”“小于”或“等于”)第3分钟时v正(CH3OH)。
③能说明该反应已达到平衡状态的是___________ 。
A.v正(H2O)=2v逆(CO2) B.n(CH3OH):n(O2)=2:3
C.容器内密度保持不变 D.容器内压强保持不变
④上述反应达到平衡时二氧化碳的转化率为___________ 。
(1)在常温常压下,H2和C3H8的混合气体共3 mol完全燃烧生成CO2和液态水放出2792kJ的热量。
已知:
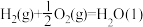 ΔH=-286 kJ·mol-1
ΔH=-286 kJ·mol-1C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220 kJ·mol-1
则该混合气体中,H2和C3H8的体积比为
(2)一种利用太阳能将甲烷重整制氢原理的示意图如下:

①第Ⅰ步反应的还原剂是
②NiO·Fe2O3在整个反应过程中的作用是
③反应每消耗1molCH4,理论上可生成标准状况下H2的体积为
(3)在催化剂光照条件下,CO2和H2O可转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)
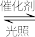 2CH3OH(g)+3O2(g)。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得n(CH3OH)随时间的变化如下表所示:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CH3OH)/mol | 0.00 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
②第4分钟时v逆(CH3OH)
③能说明该反应已达到平衡状态的是
A.v正(H2O)=2v逆(CO2) B.n(CH3OH):n(O2)=2:3
C.容器内密度保持不变 D.容器内压强保持不变
④上述反应达到平衡时二氧化碳的转化率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】Ⅰ.二氧化硒(SeO2)是一种氧化剂,被还原后的单质硒可能成为环境污染物。通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se,减少对环境的污染。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O=Se+2SO +4H+
+4H+
(1)在反应①中,被氧化的元素是_______ (填元素符号)
(2)依据反应①②判断SeO2、浓硫酸、SO2的氧化性由强到弱的顺序是_______ 。
(3)用单线桥法标出反应②电子转移的方向和数目:_______ 。
Ⅱ.有A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是NO 、SO
、SO 、Cl-、CO
、Cl-、CO 中的一种(离子在物质中不重复出现)。
中的一种(离子在物质中不重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
请回答下列问题:
(4)A的化学式为_______ ,B的化学式为_______ 。
(5)检验A溶液中阴离子的检验方法_______ 。
(6)写出D与足量醋酸溶液反应的离子方程式_______ 。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O=Se+2SO
 +4H+
+4H+(1)在反应①中,被氧化的元素是
(2)依据反应①②判断SeO2、浓硫酸、SO2的氧化性由强到弱的顺序是
(3)用单线桥法标出反应②电子转移的方向和数目:
Ⅱ.有A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是NO
 、SO
、SO 、Cl-、CO
、Cl-、CO 中的一种(离子在物质中不重复出现)。
中的一种(离子在物质中不重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
请回答下列问题:
(4)A的化学式为
(5)检验A溶液中阴离子的检验方法
(6)写出D与足量醋酸溶液反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】碲(Te)可用作半导体器件、合金、化工原料等。电解精炼铜所得的阳极泥中富含碲。工业上,常用铜阳极泥(主要成分是Cu2Te,含少量的Ag、Au)回收碲,其工艺流程如图:
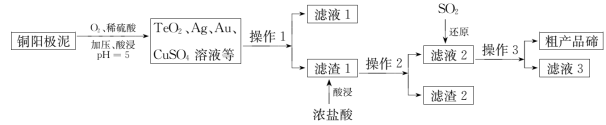
已知:①TeO2微溶于水,易与浓的强碱反应;
②TeO2与浓盐酸反应生成TeCl4。
回答下列问题:
(1)碲与硫是同主族元素,写出碲化氢的化学式:____ 。
(2)“加压、酸浸”时,Cu2Te转化为TeO2、CuSO4溶液的化学方程式为___ ;该步骤加压的目的是____ 。
(3)滤液2中通入SO2发生反应的化学方程式为___ 。
(4)滤液3中可以循环利用的物质有___ (填化学式)。
(5)工业上还可以将铜阳极泥煅烧(Cu2Te转化为TeO2、CuO)、碱浸后得到Na2TeO3溶液,再通过惰性电极电解的方法得到单质碲,则碱浸过程中生成Na2TeO3的化学方程式为___ 。

已知:①TeO2微溶于水,易与浓的强碱反应;
②TeO2与浓盐酸反应生成TeCl4。
回答下列问题:
(1)碲与硫是同主族元素,写出碲化氢的化学式:
(2)“加压、酸浸”时,Cu2Te转化为TeO2、CuSO4溶液的化学方程式为
(3)滤液2中通入SO2发生反应的化学方程式为
(4)滤液3中可以循环利用的物质有
(5)工业上还可以将铜阳极泥煅烧(Cu2Te转化为TeO2、CuO)、碱浸后得到Na2TeO3溶液,再通过惰性电极电解的方法得到单质碲,则碱浸过程中生成Na2TeO3的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】湿法冶炼脆硫铅锑矿(主要成分为Pb4FeSb6S14)制取锑白(Sb2O3)的工艺流程如下图所示。
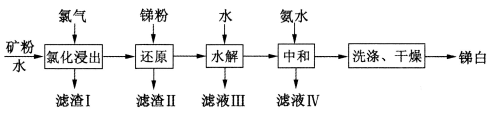
已知:①锑(Sb)为VA族元素,Sb2O3为两性氧化物
②“水解”时锑元素转化为SbOC1沉淀
回答下列问题:
(1)“氯化浸出”后的滤液中含有两种锑的氯化物,分别为SbCl3和_______ 和(填化学式)。滤渣I中所含的反应产物有PbCl2和一种单质,该单质是_______ 。
(2)“还原”是用锑粉还原高价金属离子。其中,Sb将Fe3+转化为Fe2+的离子方程式为_______ ,该转化有利于“水解”时锑铁分离。
(3)滤液Ⅳ的成分是_______ (填化学式)。“中和”时若用NaOH溶液代替氨水,Sb2O3可能会转化为_______ (填离子符号),使锑白的产量降低。
(4)锑白也可用火法冶炼脆硫铅锑矿制取,该法中有焙烧、烧结、还原和吹炼等生产环节。与火法冶炼相比,湿法冶炼的优点有_______ (任写一点)。

已知:①锑(Sb)为VA族元素,Sb2O3为两性氧化物
②“水解”时锑元素转化为SbOC1沉淀
回答下列问题:
(1)“氯化浸出”后的滤液中含有两种锑的氯化物,分别为SbCl3和
(2)“还原”是用锑粉还原高价金属离子。其中,Sb将Fe3+转化为Fe2+的离子方程式为
(3)滤液Ⅳ的成分是
(4)锑白也可用火法冶炼脆硫铅锑矿制取,该法中有焙烧、烧结、还原和吹炼等生产环节。与火法冶炼相比,湿法冶炼的优点有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钨锰铁矿[主要成分为(Fe,Mn)WO4,还含有石英及少量P、As的化合物],由钨锰铁矿的精矿粉制备金属钨的工艺流程如图所示:

(1)已知W为第六周期元素,与Cr同族,但核外电子排布完全符合构造原理,写出W的基态价电子排布式___ 。用钨做白炽灯灯丝是利用其___ (填具体性质)。
(2)“滤渣II”中除含有Mg3(PO4)2、Mg3(AsO4)2外,还含有__ (写化学式)。
(3)“萃取”时发生的反应为3(R3NH)2SO4(油层)+H2W12O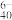 (水层)=(R3NH)6H2W12O40(油层)+3SO
(水层)=(R3NH)6H2W12O40(油层)+3SO (水层),该步骤主要目的是除去
(水层),该步骤主要目的是除去___ 。最适合作“反萃取剂”的是___ 。
(4)焦炭和氢气都可以将三氧化钨还原成钨单质,但工业上常用氢气作还原剂,此反应是___ (填“吸热”或“放热”)反应,不用焦炭的原因是__ 。
(5)某小组利用可逆反应,W(s)+I2(g) WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在
WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在___ 区(填“Ⅰ”或“Ⅱ”)。


(1)已知W为第六周期元素,与Cr同族,但核外电子排布完全符合构造原理,写出W的基态价电子排布式
(2)“滤渣II”中除含有Mg3(PO4)2、Mg3(AsO4)2外,还含有
(3)“萃取”时发生的反应为3(R3NH)2SO4(油层)+H2W12O
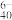 (水层)=(R3NH)6H2W12O40(油层)+3SO
(水层)=(R3NH)6H2W12O40(油层)+3SO (水层),该步骤主要目的是除去
(水层),该步骤主要目的是除去(4)焦炭和氢气都可以将三氧化钨还原成钨单质,但工业上常用氢气作还原剂,此反应是
(5)某小组利用可逆反应,W(s)+I2(g)
 WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在
WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】KNO3是重要的化工产品,下面是一种已获得专利的KNO3制备方法的主要步骤:
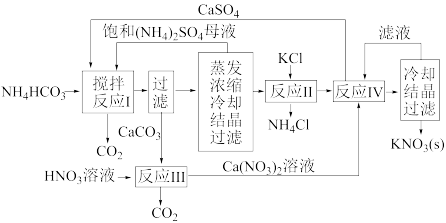
(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1∶2,该反应的化学方程式为________________ 。
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是_________________ 。从反应Ⅳ所得混合物中分离出CaSO4的方法是趁热过滤,趁热过滤的目的是______________________________ 。
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水,____________ 。
(4)整个循环流程中,需不断补充的原料除NH4HCO3外,还有____________ (填化学式)。

(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1∶2,该反应的化学方程式为
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水,
(4)整个循环流程中,需不断补充的原料除NH4HCO3外,还有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组用铝箔制备纳米Al2O3、AlCl3·6H2O及铵明矾晶体【NH4Al(SO4)2•12H2O,摩尔质量为453g•mol-1】,具体流程如图:
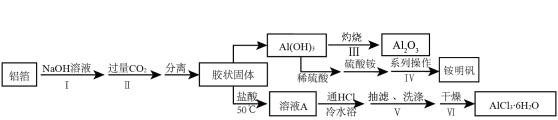
已知:a.AlCl3·6H2O易溶于水、乙醇及乙醚;
b.铵明矾晶体无色、透明,可溶于水、不溶于乙醇。120℃时失去结晶水,280℃以上分解。
请回答:
(1)步骤Ⅰ的离子方程式为______ 。
(2)下列操作或描述正确的是_____ 。
A.步骤IV制备铵明矾利用了物质的溶解度差异
B.步骤III灼烧时需将氢氧化铝放在蒸发皿里用高温炉灼烧至恒重
C.步骤II生成的固体可用抽滤法分离,为加快过滤速度,可用玻璃棒轻轻搅拌
D.步骤IV中可以选择乙醇洗涤晶体,如果在常压下快速干燥,温度选择低于120℃
(3)由溶液A制备AlCl3·6H2O的过程中要通入HCl气体,其作用是______ (写两条)。
(4)步骤V抽滤时不能用滤纸,原因是_____ 。若用如图装置图进行抽滤,则抽滤结束时应进行的操作是______ 。

(5)用电子天平称取2.760g的铵明矾粗产品,用水溶解后取相同体积的两份溶液。第一份用EDTA滴定法测得n(Al3+)为0.002900mol;第二份用BaCl2溶液滴定法测得n(SO42-)为0.006300mol。则该试样中铵明矾的纯度为______ 。

已知:a.AlCl3·6H2O易溶于水、乙醇及乙醚;
b.铵明矾晶体无色、透明,可溶于水、不溶于乙醇。120℃时失去结晶水,280℃以上分解。
请回答:
(1)步骤Ⅰ的离子方程式为
(2)下列操作或描述正确的是
A.步骤IV制备铵明矾利用了物质的溶解度差异
B.步骤III灼烧时需将氢氧化铝放在蒸发皿里用高温炉灼烧至恒重
C.步骤II生成的固体可用抽滤法分离,为加快过滤速度,可用玻璃棒轻轻搅拌
D.步骤IV中可以选择乙醇洗涤晶体,如果在常压下快速干燥,温度选择低于120℃
(3)由溶液A制备AlCl3·6H2O的过程中要通入HCl气体,其作用是
(4)步骤V抽滤时不能用滤纸,原因是

(5)用电子天平称取2.760g的铵明矾粗产品,用水溶解后取相同体积的两份溶液。第一份用EDTA滴定法测得n(Al3+)为0.002900mol;第二份用BaCl2溶液滴定法测得n(SO42-)为0.006300mol。则该试样中铵明矾的纯度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)废水处理方法之一是用Cl2将废水中的CN-氧化成没有污染的物质,则该反应的离子方程式是_________ 。
(2)某工厂用肼(N2H4)处理含有大量Cu(OH)2的废料来回收金属铜,流程如下:
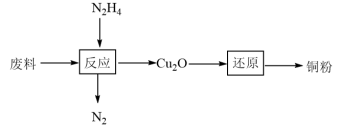
“反应”需加热,写出该反应的化学方程式:_______ 。
(3)在钢铁分析中常用过二硫酸钾氧化法测定钢中锰的含量,现有一份50.0 g钢铁样品,加入到硫酸、磷酸、硝酸组成的混合酸中,加热溶解,煮沸2~3分钟,以硝酸银为催化剂,用过二硫酸钾氧化,可得到含有高锰酸钾的溶液,加热,煮沸30~40秒,静置1~2分钟,冷却至室温。再用1.0000 mol/L亚硝酸钠溶液来滴定溶液,消耗亚硝酸钠溶液25.00 ml。
a.写出Mn2+与K2S2O8反应的离子方程式_____________________ 。
b.写出滴定时发生反应的离子方程式__________________________ 。
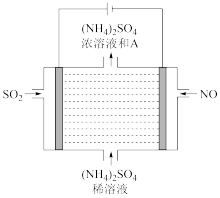
(4)用石墨为电极,利用如图电解装置可将雾霾中的NO、SO2分别转化为NH 和SO
和SO ,则阴极的电极反应式是
,则阴极的电极反应式是____________________________ 。
(5)某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
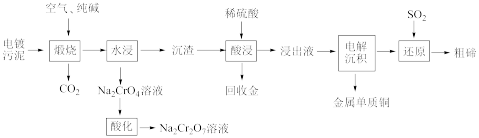
煅烧时,Cr2O3发生反应的化学方程式为__________________ 。
(1)废水处理方法之一是用Cl2将废水中的CN-氧化成没有污染的物质,则该反应的离子方程式是
(2)某工厂用肼(N2H4)处理含有大量Cu(OH)2的废料来回收金属铜,流程如下:

“反应”需加热,写出该反应的化学方程式:
(3)在钢铁分析中常用过二硫酸钾氧化法测定钢中锰的含量,现有一份50.0 g钢铁样品,加入到硫酸、磷酸、硝酸组成的混合酸中,加热溶解,煮沸2~3分钟,以硝酸银为催化剂,用过二硫酸钾氧化,可得到含有高锰酸钾的溶液,加热,煮沸30~40秒,静置1~2分钟,冷却至室温。再用1.0000 mol/L亚硝酸钠溶液来滴定溶液,消耗亚硝酸钠溶液25.00 ml。
a.写出Mn2+与K2S2O8反应的离子方程式
b.写出滴定时发生反应的离子方程式
(4)用石墨为电极,利用如图电解装置可将雾霾中的NO、SO2分别转化为NH
 和SO
和SO ,则阴极的电极反应式是
,则阴极的电极反应式是
(5)某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:

煅烧时,Cr2O3发生反应的化学方程式为
您最近一年使用:0次



