高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知 A、F 为非金属单质气体,B为常见金属单质,E 为生活中最常见的调味品,F 在标准状况下密度为 0.090g·L-1。

请回答下列问题:
(1)写出 D 的名称___________ ,Na2FeO4中 Fe 元素的化合价为___________ 。
(2)反应③,F 在 A 中点燃的反应现象为___________ 。
(3)写出反应④的化学方程式,并用“双线桥”表示电子转移的方向和数目:___________ 。

请回答下列问题:
(1)写出 D 的名称
(2)反应③,F 在 A 中点燃的反应现象为
(3)写出反应④的化学方程式,并用“双线桥”表示电子转移的方向和数目:
更新时间:2023-11-08 17:24:44
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】硫酸亚铁是一种补铁剂,某兴趣小组利用经初步处理的含有 的废液制备硫酸亚铁晶体的流程如下:
的废液制备硫酸亚铁晶体的流程如下:

(1)加入饱和 溶液后,得到白色沉淀,则操作1为
溶液后,得到白色沉淀,则操作1为___________ ,若 溶液浓度偏低可能会形成胶体,验证的方法为
溶液浓度偏低可能会形成胶体,验证的方法为___________ 。
(2)加入铁粉的作用是___________ 。
(3)测定废液中 的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:
的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________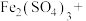 ___________
___________
(4)该兴趣小组在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设:
①假设一:按 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为
受热分解的化学方程式为___________ ;
②假设二:按 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 受热分解的化学方程式为
受热分解的化学方程式为___________ 。
(5) 和
和 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: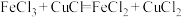 ,待固体完全溶解后,加入适量稀硫酸,用
,待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 (该条件下
(该条件下 不被氧化),消耗
不被氧化),消耗 溶液bmL,反应中
溶液bmL,反应中 被还原为
被还原为 。则样品中CuCl的质量分数为
。则样品中CuCl的质量分数为___________ 。
 的废液制备硫酸亚铁晶体的流程如下:
的废液制备硫酸亚铁晶体的流程如下:
(1)加入饱和
 溶液后,得到白色沉淀,则操作1为
溶液后,得到白色沉淀,则操作1为 溶液浓度偏低可能会形成胶体,验证的方法为
溶液浓度偏低可能会形成胶体,验证的方法为(2)加入铁粉的作用是
(3)测定废液中
 的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:
的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________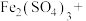 ___________
___________
(4)该兴趣小组在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设:
①假设一:按
 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为
受热分解的化学方程式为②假设二:按
 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 受热分解的化学方程式为
受热分解的化学方程式为(5)
 和
和 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: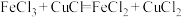 ,待固体完全溶解后,加入适量稀硫酸,用
,待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 (该条件下
(该条件下 不被氧化),消耗
不被氧化),消耗 溶液bmL,反应中
溶液bmL,反应中 被还原为
被还原为 。则样品中CuCl的质量分数为
。则样品中CuCl的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】早在春秋战国时期,我国就开始生产和使用铁器。某实验小组利用焦炭和 模拟早期炼铁并检验可能的产物,实验装置如下:
模拟早期炼铁并检验可能的产物,实验装置如下:

【查阅资料】①铁粉为黑色;常温下,Fe、 可被磁铁吸引;
可被磁铁吸引;
② ,溶液可用于检验CO,原理是:
,溶液可用于检验CO,原理是: ;
;
③ 与硫酸反应:
与硫酸反应: 。
。
【实验现象】澄清石灰水变浑浊, 溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
(1)仪器A的名称是___________ 。
(2)为了检验气体产物,装置从左到右的接口连接顺序为a→___________ 。
(3)用双线桥法标出反应 中的电子转移情况:
中的电子转移情况:___________ 。
【实验结论】反应生成CO和CO2,磁铁上的黑色固体可能是Fe、 。
。
【提出猜想】
(4)磁铁上的黑色固体是什么?
猜想一:Fe
猜想二:___________
猜想三:Fe和
【设计实验】
(5)
【归纳总结】
(6)根据实验结论和探究结果C与 反应的化学方程式为
反应的化学方程式为___________
 模拟早期炼铁并检验可能的产物,实验装置如下:
模拟早期炼铁并检验可能的产物,实验装置如下:
【查阅资料】①铁粉为黑色;常温下,Fe、
 可被磁铁吸引;
可被磁铁吸引;②
 ,溶液可用于检验CO,原理是:
,溶液可用于检验CO,原理是: ;
;③
 与硫酸反应:
与硫酸反应: 。
。【实验现象】澄清石灰水变浑浊,
 溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。(1)仪器A的名称是
(2)为了检验气体产物,装置从左到右的接口连接顺序为a→
(3)用双线桥法标出反应
 中的电子转移情况:
中的电子转移情况:【实验结论】反应生成CO和CO2,磁铁上的黑色固体可能是Fe、
 。
。【提出猜想】
(4)磁铁上的黑色固体是什么?
猜想一:Fe
猜想二:
猜想三:Fe和

【设计实验】
(5)
| 设计思路 | 操作 | 现象 | 结论 |
| 定性实验 | 取少量黑色固体于试管中,加入足量稀硫酸,充分反应 | 固体完全溶解,产生气泡 | 猜想 |
| 定量实验 | 取一定质量的稀硫酸(足量)放入烧杯中,加入5.6g黑色固体,充分反应后称量溶液的质量 | 固体完全溶解,产生气泡,溶液增加的质量为 | 猜想—成立 |
【归纳总结】
(6)根据实验结论和探究结果C与
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】次氯酸钠是家用消毒剂的有效成分。实验室制备次氯酸钠的装置如图所示。
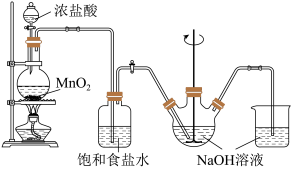
(1)在圆底烧瓶里加入二氧化锰后,通过___________ (填仪器名称)向烧瓶中加入适量的浓盐酸并加热。发生反应的离子方程式为___________ 。
(2)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
 。
。
①用双线桥标出该反应中电子转移的方向和数目___________ 。
②若产生标准状况下4.48L ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是___________ mol,转移电子的物质的量为___________ mol。
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与消毒液(主要成分是NaClO)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:___________ 。

(1)在圆底烧瓶里加入二氧化锰后,通过
(2)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
 。
。①用双线桥标出该反应中电子转移的方向和数目
②若产生标准状况下4.48L
 ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与消毒液(主要成分是NaClO)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:
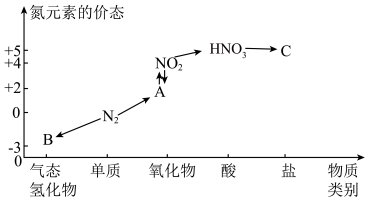
(1)B的电子式为___________ , 的用途为
的用途为___________ (写出一条即可)。
(2) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为___________ 。
(3)浓硝酸与木炭在加热条件下反应的化学方程式为___________ 。
(4)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气。实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为___________ ,请设计一个实验方案鉴定该固体中的阳离子___________ 。
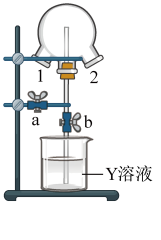
(5)标准状况下,若在烧瓶中充满混有空气的氨气,倒置于盛足量水的水槽中,当水进入烧瓶中,并使气体充分溶解,假定烧瓶中溶液无损失,所得溶液的物质的量浓度为___________ mol/L。

(1)B的电子式为
 的用途为
的用途为(2)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为(3)浓硝酸与木炭在加热条件下反应的化学方程式为
(4)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气。实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为

(5)标准状况下,若在烧瓶中充满混有空气的氨气,倒置于盛足量水的水槽中,当水进入烧瓶中,并使气体充分溶解,假定烧瓶中溶液无损失,所得溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】图中A为一种中学化学中常见的金属单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
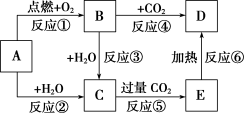
(1)B的化学式中阳离子和阴离子的个数比为______ 。
(2)以上6个反应中属于氧化还原反应的有____________ (填写编号)。
(3)写出B→D反应的化学方程式________________________ 。
(4)若用所示装置验证D、E的热稳定性,则乙中装入的固体最好是______ (填化学式)。
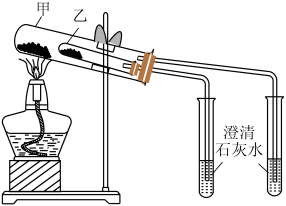
(5)向滴入酚酞的D溶液中滴入少量稀盐酸,现象是没有气泡生成,溶液__________ ,反应的离子方程式为_______________ ,继续滴加盐酸至过量,现象是_______________
(6)将一定量的B投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后溶液中上述离子数目明显增多的有
,反应完毕后溶液中上述离子数目明显增多的有______ (填离子符号).

(1)B的化学式中阳离子和阴离子的个数比为
(2)以上6个反应中属于氧化还原反应的有
(3)写出B→D反应的化学方程式
(4)若用所示装置验证D、E的热稳定性,则乙中装入的固体最好是

(5)向滴入酚酞的D溶液中滴入少量稀盐酸,现象是没有气泡生成,溶液
(6)将一定量的B投入到含有下列离子的溶液中:
 、
、 、
、 、
、 ,反应完毕后溶液中上述离子数目明显增多的有
,反应完毕后溶液中上述离子数目明显增多的有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
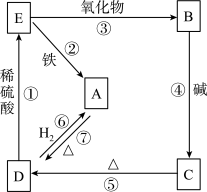
【推荐3】物质A可发生如图所表示的反应:
写出相应物质的化学式和类别(填在表格内),并依次写出各步反应的化学方程式。
(1)______________________________ 。
(2)______________________________ 。
(3)______________________________ 。
(4)______________________________ 。
(5)______________________________ 。
(6)______________________________ 。
(7)______________________________
写出相应物质的化学式和类别(填在表格内),并依次写出各步反应的化学方程式。
| A | B | C | D | E | |
| 化学式 | Cu | CuCl2 | |||
| 类 别 | 碱 | 氧化物 | 盐 |

(1)
(2)
(3)
(4)
(5)
(6)
(7)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外小组对金属钠进行研究。已知C、D都是单质,F的水溶液是一种常见的强酸。

(1)金属Na在空气中放置足够长时间,最终的生成物是:_________________________ 。
(2)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是_________________________ 。
(3)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,请写出该过程发生反应的方程式:_________________________ 。
(4)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其物质的量浓度之比为________________________ 。

(5)将NaHCO3与M的混合物在密闭容器中充分加热后排出气体,经测定,所得固体为纯净物,则NaHCO3与M的质量比为____________ 。

(1)金属Na在空气中放置足够长时间,最终的生成物是:
(2)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是
(3)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,请写出该过程发生反应的方程式:
(4)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其物质的量浓度之比为

(5)将NaHCO3与M的混合物在密闭容器中充分加热后排出气体,经测定,所得固体为纯净物,则NaHCO3与M的质量比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶的低温硫化剂和粘接剂。
S2Cl2具有下列性质:
实验室可利用硫与少量氯气在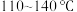 反应制得S2Cl2粗品。
反应制得S2Cl2粗品。

(1)仪器m的名称为_______ ;符合A装置制取氯气的溶液n可以为_______ 溶液。
(2)请补充完整实验装置连接顺序:A→_______→_______→_______→E→D,______ (填写装置标号),其中装置E的作用是_______ ,D装置的作用是_______ 。
(3)实验过程中,实验前和停止加热后,都需通一段时间的氮气,若停止加热后没有继续通入氮气,则S2Cl2的产率将_______ (填“偏高”、“偏低”或“无影响”)。
(4)实验中为了提高S2Cl2的纯度,实验的关键是保持干燥环境,_______ 和_______ 。
(5)S2Cl2遇水强烈反应会产生两种气体和一种沉淀,请写出该反应的化学方程式_______ 。
S2Cl2具有下列性质:
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解 ②氯气过量发生反应: 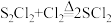 ③受热或遇水分解放热,放出腐蚀性烟气 | ||||
 反应制得S2Cl2粗品。
反应制得S2Cl2粗品。
(1)仪器m的名称为
(2)请补充完整实验装置连接顺序:A→_______→_______→_______→E→D,
(3)实验过程中,实验前和停止加热后,都需通一段时间的氮气,若停止加热后没有继续通入氮气,则S2Cl2的产率将
(4)实验中为了提高S2Cl2的纯度,实验的关键是保持干燥环境,
(5)S2Cl2遇水强烈反应会产生两种气体和一种沉淀,请写出该反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】欲做实验:氯气与氢气混合后在光照条件下爆鸣。手头没有气体发生器,也不使用加热装置,利用一个“倒Y型”玻璃试管(图)。

(1)该实验的做法是:
在倒Y形管两端底部分别放入一种固体,一端是_______ ,另一端是KMnO4或KClO3;然后在两端同时注入____ 酸,用带导管的塞子将管口塞紧,并将该导管通向盛______ 溶液的容器。临时制取的H2和Cl2即时混合后用闪光灯引爆。
(2)倒Y型试管可用来同时制取两种气体,并便于观察气体在常温下混合后的反应现象。请举一例(用两种气体的分子式表示):______ 与______

(1)该实验的做法是:
在倒Y形管两端底部分别放入一种固体,一端是
(2)倒Y型试管可用来同时制取两种气体,并便于观察气体在常温下混合后的反应现象。请举一例(用两种气体的分子式表示):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】通过简单地推理或计算填空:
(1)X原子有两个电子层,它能与最活泼的金属Y形成Y3X的化合物,X是______ 元素(写元素符号)。
(2)若某元素原子的电子层数和Na原子的相同,最外层电子数与F原子相同,则该元素的原子序数是______ 。
(3)6C元素能够与某非金属元素R形成化合物CRn,已知CRx分子中各原子核外最外层电子总数为32,核外电子数总和为74.则R是______ 元素(写元素符号),n=______ 。
(4)有A、B、C、D、E五种短周期元素,其元素特征信息如下表:
①写出E单质与A、B、C形成的化合物反应的化学方程式: ______ 。
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:______ 。
(1)X原子有两个电子层,它能与最活泼的金属Y形成Y3X的化合物,X是
(2)若某元素原子的电子层数和Na原子的相同,最外层电子数与F原子相同,则该元素的原子序数是
(3)6C元素能够与某非金属元素R形成化合物CRn,已知CRx分子中各原子核外最外层电子总数为32,核外电子数总和为74.则R是
(4)有A、B、C、D、E五种短周期元素,其元素特征信息如下表:
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C位于第_______ 周期________ 族,它的最高价氧化物的化学式为____________ 。
(2)B是________ 元素。
(3)写出B 和 D组成化合物的形成过程______________________________________ 。
(4)A与D形成稳定的化合物的化学式为______________ ,将该化合物加入含有酚酞的水作用实验现象是____________________________________________________________ 。
(5)C元素的单质有毒,可用A 的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_________________________________________________________________________ 。
(1)元素C位于第
(2)B是
(3)写出B 和 D组成化合物的形成过程
(4)A与D形成稳定的化合物的化学式为
(5)C元素的单质有毒,可用A 的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰。H可用于制造光导纤维,J是一种乳白色凝胶状沉淀。(部分生成物和部分反应条件未列出) 请回答下列问题:
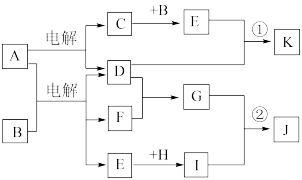
(1)形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H在高温下与碳反应方程式为 ,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式

(1)形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H在高温下与碳反应方程式为 ,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式
您最近一年使用:0次



