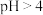常温下,将pH=11的NaOH溶液a L与pH=3的稀盐酸b L混合,所得溶液的pH=7(假设混合后溶液体积变化忽略不计),则
| A.a=b | B.a>b | C.a<b | D.无法确定 |
更新时间:2023-12-14 10:09:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温时,下列三种溶液:
①0.001 mol·L-1氨水与0.001 mol·L-1 HCl溶液等体积混合液
②pH=3的HCl与pH=11的NaOH溶液等体积混合液
③pH=11的氨水与pH=3的HCl溶液等体积混合液。
其pH大小关系正确的是
①0.001 mol·L-1氨水与0.001 mol·L-1 HCl溶液等体积混合液
②pH=3的HCl与pH=11的NaOH溶液等体积混合液
③pH=11的氨水与pH=3的HCl溶液等体积混合液。
其pH大小关系正确的是
| A.①=②=③ | B.①>②=③ |
| C.①<②=③ | D.①<②<③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将 的盐酸溶液和
的盐酸溶液和 的氨水等体积混合后,溶液中离子浓度关系正确的是
的氨水等体积混合后,溶液中离子浓度关系正确的是
 的盐酸溶液和
的盐酸溶液和 的氨水等体积混合后,溶液中离子浓度关系正确的是
的氨水等体积混合后,溶液中离子浓度关系正确的是A. |
B.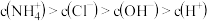 |
C. |
D.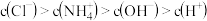 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】水存在电离平衡:H2O H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
 H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是| A.常温下,水电离出的 c(H+)=c(OH-)=10-7mol·L-1 |
| B.向水中加入NaCl,H+与 Cl-结合生成 HCl,使水的电离平衡向正反应方向移动 |
| C.向水中加入HCl或者NaOH,水的电离平衡都向逆反应方向移动 |
| D.改变温度,Kw 也会发生改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法不正确 的是
| A.活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能 |
| B.增大压强(体积减小)或升高温度,均能增大活化分子百分数,从而加快化学反应速率 |
C. 的溶液一定为中性 的溶液一定为中性 |
| D.发生化学反应的碰撞都是有效碰撞 |
您最近一年使用:0次

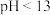 ,则ROH一定为弱电解质
,则ROH一定为弱电解质 ,升温后pH仍为a,则BA可能为强碱弱酸盐
,升温后pH仍为a,则BA可能为强碱弱酸盐 溶液,消耗盐酸的物质的量之比为1∶2
溶液,消耗盐酸的物质的量之比为1∶2 的盐酸溶液与
的盐酸溶液与