硼(B)是冶金、建材、机械领域的重要原料,利用镁还原法生产硼的主要工艺流程如图。

(1)H3BO3中B元素的化合价为___________ ,脱水炉中发生的反应属于基本反应类型中的___________ 反应。
(2)用双线桥法表示还原炉中发生的反应:___________
(3)向酸煮罐加入盐酸目的是除去 MgO,写出该反应的离子方程式:___________
(4)请配平 B单质和 NaOH、NaNO3在高温共融时发生反应的化学方程式:___________
______B+______NaOH+______NaNO3 ______NaBO2+______NaNO2+______H2O
______NaBO2+______NaNO2+______H2O
该反应中还原剂和还原产物的质量之比为___________ 。

(1)H3BO3中B元素的化合价为
(2)用双线桥法表示还原炉中发生的反应:
(3)向酸煮罐加入盐酸目的是除去 MgO,写出该反应的离子方程式:
(4)请配平 B单质和 NaOH、NaNO3在高温共融时发生反应的化学方程式:
______B+______NaOH+______NaNO3
 ______NaBO2+______NaNO2+______H2O
______NaBO2+______NaNO2+______H2O该反应中还原剂和还原产物的质量之比为
更新时间:2023-10-14 20:24:21
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】如图所示,A、B、C、D、E各代表水、锌、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质(已知C是氢氧化钡溶液,B是硫酸铜溶液).常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且A的相对分子(或原子)质量大于D,请填空:
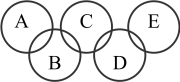
(1)写出下列物质的化学式:A______ 、D______ 、E______ .
(2)写出B与C反应的化学方程式:___________ .
(3)以B为原料,制备CuO,写出具体的化学方程式__________ .
(4)相连环物质间发生的反应中,属于置换反应的是(写出具体化学方程式)___________ .

(1)写出下列物质的化学式:A
(2)写出B与C反应的化学方程式:
(3)以B为原料,制备CuO,写出具体的化学方程式
(4)相连环物质间发生的反应中,属于置换反应的是(写出具体化学方程式)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)从Na、S、H、O四种元素中选择合适的元素,组成与表中第一栏类别相同的物质,将其化学式填在表中相应的空格内。
(2)选用你在上表中所填的物质,按下列要求写出相应的化学方程式。
①某个化合反应:_______ 。
②氧化物与足量的碱反应:_______ 。
③氧化物和足量的酸反应:_______ 。
(1)从Na、S、H、O四种元素中选择合适的元素,组成与表中第一栏类别相同的物质,将其化学式填在表中相应的空格内。
| 类型 | 碱性氧化物 | 最高价的酸性氧化物 | 二元强酸 | 有溶性碱 |
| 化学式 | ① | ② | ③ | ④ |
(2)选用你在上表中所填的物质,按下列要求写出相应的化学方程式。
①某个化合反应:
②氧化物与足量的碱反应:
③氧化物和足量的酸反应:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】实验室现有 、
、 、
、 、
、 、
、 五种溶液,现从中任取四种溶液,编号为A、B、C、D并进行相关实验。其中A属于盐类且能与B反应生成气体,B、C、D间反应现象的记录如表。回答下列问题:
五种溶液,现从中任取四种溶液,编号为A、B、C、D并进行相关实验。其中A属于盐类且能与B反应生成气体,B、C、D间反应现象的记录如表。回答下列问题:
(1)根据实验现象及已知条件,可推断出四种溶液中溶质的化学式为
A:___________ B:___________ C:___________
(2)按要求写出下列反应的反应方程式:
①C和D反应的化学方程式:___________ 。
②A和B反应的离子方程式:___________ 。
 、
、 、
、 、
、 、
、 五种溶液,现从中任取四种溶液,编号为A、B、C、D并进行相关实验。其中A属于盐类且能与B反应生成气体,B、C、D间反应现象的记录如表。回答下列问题:
五种溶液,现从中任取四种溶液,编号为A、B、C、D并进行相关实验。其中A属于盐类且能与B反应生成气体,B、C、D间反应现象的记录如表。回答下列问题:| 溶液 | B | C | D |
| B | — | 不反应 | ↓ |
| C | 不反应 | — | ↓ |
| D | ↓ | ↓ | — |
A:
(2)按要求写出下列反应的反应方程式:
①C和D反应的化学方程式:
②A和B反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
Ⅰ.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
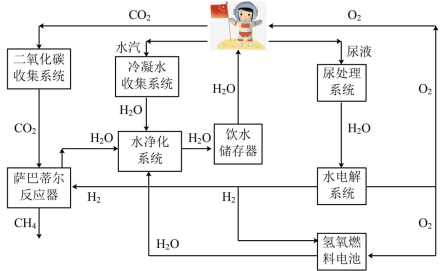
(1)“尿处理系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的___________ 不同进行分离的。
(2)“水电解系统”中发生反应的化学方程式为___________ 。
(3)在水净化系统中,用臭氧( )消素,臭氧在一定条件下转化为氧气的化学方程式为:
)消素,臭氧在一定条件下转化为氧气的化学方程式为:___________ ;该反应___________ (填“属于”或“不属于”)氧化还原反应。
(4)在一定条件下,“萨巴蒂尔反应器”可以除去 ,该反应的化学方程式为
,该反应的化学方程式为_________ 。
Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:
___________ (补全化学方程式)。
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的___________(填序号)。
Ⅰ.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“尿处理系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的
(2)“水电解系统”中发生反应的化学方程式为
(3)在水净化系统中,用臭氧(
 )消素,臭氧在一定条件下转化为氧气的化学方程式为:
)消素,臭氧在一定条件下转化为氧气的化学方程式为:(4)在一定条件下,“萨巴蒂尔反应器”可以除去
 ,该反应的化学方程式为
,该反应的化学方程式为Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:

(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的___________(填序号)。
A. | B.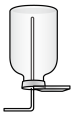 | C.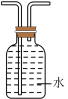 | D. |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】硫铁矿的主要成分为FeS2,工业上常用硫铁矿在空气中煅烧产气来制备硫酸,该过程中的烧渣可用于制备铁红、绿矾等。现以硫铁矿烧渣(主要成分为Fe2O3,FeO,还含有少量的Al2O3、SiO2杂质)为原料、氨水为沉淀剂制备铁红颜料的流程如图所示:
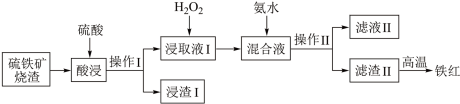
根据所学知识,回答下列问题:
(1)已知FeS2高温煅烧生成Fe2O3和SO2,请写出化学方程式:_______ ,其中氧化产物为_______ (填化学式)。
(2)“浸取液I”中加入H2O2的目的是_______ 。
(3)进行操作I所需的玻璃仪器有_______ 。
(4)在加入氨水沉淀时,调节pH可使得Fe3+沉淀而Al3+不沉淀。“滤液Ⅱ”中溶质的主要成分为_______ (填化学式)。写出获得“滤渣Ⅱ”的离子方程式:_______ 。检验滤液Ⅱ中是否存在Fe3+,应用_______ 试剂。

根据所学知识,回答下列问题:
(1)已知FeS2高温煅烧生成Fe2O3和SO2,请写出化学方程式:
(2)“浸取液I”中加入H2O2的目的是
(3)进行操作I所需的玻璃仪器有
(4)在加入氨水沉淀时,调节pH可使得Fe3+沉淀而Al3+不沉淀。“滤液Ⅱ”中溶质的主要成分为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】高效灭菌消毒剂 气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性
气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性 溶液贮存,再经酸活化处理后使用。以氯酸盐
溶液贮存,再经酸活化处理后使用。以氯酸盐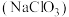 、过氧化氢和碳酸盐为主要原料制备稳定性
、过氧化氢和碳酸盐为主要原料制备稳定性 溶液的流程如下:
溶液的流程如下:

(1)反应器中发生的主要反应为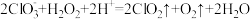 。
。
①该反应中 是
是___________ (填“氧化剂”、“还原剂”或“氧化剂和还原剂”)。
②制备时向反应器中通入空气的作用是___________ 。
(2)反应器中的反应温度控制在 左右为宜。
左右为宜。
①工业上采用的加热方式为___________ 。
②当温度超过 ,
, 的收率(
的收率(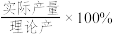 )随温度升高而减小,其原因可能是
)随温度升高而减小,其原因可能是___________ 。
(3)吸收瓶中发生反应 ,获得稳定性
,获得稳定性 溶液。当有
溶液。当有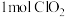 参加反应,转移的电子数为
参加反应,转移的电子数为___________  。
。
(4)以亚氯酸盐( )为原料进行酸化是生产
)为原料进行酸化是生产 最简单的方法,其反应原理为
最简单的方法,其反应原理为 ,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是
,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是___________ 。
 气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性
气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性 溶液贮存,再经酸活化处理后使用。以氯酸盐
溶液贮存,再经酸活化处理后使用。以氯酸盐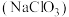 、过氧化氢和碳酸盐为主要原料制备稳定性
、过氧化氢和碳酸盐为主要原料制备稳定性 溶液的流程如下:
溶液的流程如下:
(1)反应器中发生的主要反应为
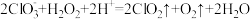 。
。①该反应中
 是
是②制备时向反应器中通入空气的作用是
(2)反应器中的反应温度控制在
 左右为宜。
左右为宜。①工业上采用的加热方式为
②当温度超过
 ,
, 的收率(
的收率(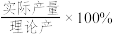 )随温度升高而减小,其原因可能是
)随温度升高而减小,其原因可能是(3)吸收瓶中发生反应
 ,获得稳定性
,获得稳定性 溶液。当有
溶液。当有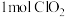 参加反应,转移的电子数为
参加反应,转移的电子数为 。
。(4)以亚氯酸盐(
 )为原料进行酸化是生产
)为原料进行酸化是生产 最简单的方法,其反应原理为
最简单的方法,其反应原理为 ,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是
,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】PFS是水处理中重要的絮凝剂,下图是以回收的废铁屑为原料制备PFS的一种工艺流程。

(1)酸浸槽以及聚合釜中用到的酸应是_____ ;在酸浸槽中,为了提高浸出率,可以采取的措施有______ ,_______ (写两条)。
(2)若废铁屑中含有较多铁锈(Fe2O3·xH2O),则酸浸时铁锈反应的化学方程式为________ 。
(3)如果反应釜中用H2O2作氧化剂,则反应的离子方程式为______ ;生产过程中,发现反应釜中产生了大量的气体,且温度明显升高,其原因可能是________ 。

(1)酸浸槽以及聚合釜中用到的酸应是
(2)若废铁屑中含有较多铁锈(Fe2O3·xH2O),则酸浸时铁锈反应的化学方程式为
(3)如果反应釜中用H2O2作氧化剂,则反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】Ag是高新技术产业的基础材料之一,依据下列回收Ag的方案回答下列问题:
(1)利用废旧电池中的 可将有毒气体甲醛(HCHO)氧化成
可将有毒气体甲醛(HCHO)氧化成 ,将上述反应设计成原电池,在
,将上述反应设计成原电池,在___________ (填“正”或“负”)极可获得Ag。
(2)以含 的废定影液为原料提取银的主要步骤为:加入过量
的废定影液为原料提取银的主要步骤为:加入过量 溶液后,过滤、洗涤、干燥。将获得的
溶液后,过滤、洗涤、干燥。将获得的 在足量空气中充分焙烧制得Ag。实验室焙烧
在足量空气中充分焙烧制得Ag。实验室焙烧 在
在___________ (填仪器名称)中完成,焙烧 的化学方程式是
的化学方程式是___________ ,常温下, 饱和溶液中
饱和溶液中 的浓度为a mol/L,则常温下
的浓度为a mol/L,则常温下 的溶度积常数
的溶度积常数 为
为___________ 。
(3)从光盘金属层中提取Ag(其他微量金属忽略不计)的流程如下图所示:
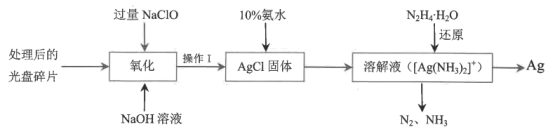
①“氧化”阶段需在80℃条件下进行,最适合的加热方式为___________ ,操作Ⅰ的名称为___________ 。
②“还原”过程 的氧化产物为
的氧化产物为 ,理论上消耗1mol
,理论上消耗1mol 可生成单质Ag的质量为
可生成单质Ag的质量为___________ 克。
③NaClO溶液与Ag反应有 生成,该反应的离子方程式为
生成,该反应的离子方程式为___________ 。
(1)利用废旧电池中的
 可将有毒气体甲醛(HCHO)氧化成
可将有毒气体甲醛(HCHO)氧化成 ,将上述反应设计成原电池,在
,将上述反应设计成原电池,在(2)以含
 的废定影液为原料提取银的主要步骤为:加入过量
的废定影液为原料提取银的主要步骤为:加入过量 溶液后,过滤、洗涤、干燥。将获得的
溶液后,过滤、洗涤、干燥。将获得的 在足量空气中充分焙烧制得Ag。实验室焙烧
在足量空气中充分焙烧制得Ag。实验室焙烧 在
在 的化学方程式是
的化学方程式是 饱和溶液中
饱和溶液中 的浓度为a mol/L,则常温下
的浓度为a mol/L,则常温下 的溶度积常数
的溶度积常数 为
为(3)从光盘金属层中提取Ag(其他微量金属忽略不计)的流程如下图所示:

①“氧化”阶段需在80℃条件下进行,最适合的加热方式为
②“还原”过程
 的氧化产物为
的氧化产物为 ,理论上消耗1mol
,理论上消耗1mol 可生成单质Ag的质量为
可生成单质Ag的质量为③NaClO溶液与Ag反应有
 生成,该反应的离子方程式为
生成,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】SPC(2Na2CO3∙3H2O2)具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO4∙10H2O)、H2O2等为原料制备SPC的工艺流程如下:

回答下列问题:
⑴步骤Ⅰ中________  填“有”或“没有”
填“有”或“没有” 发生氧化还原反应。
发生氧化还原反应。
⑵步骤Ⅱ中会生成一种可以循环使用的物质,该物质的化学式为________ 。
⑶步骤Ⅲ中需要加热,发生反应的化学方程式为_________________________________ 。
⑷步骤Ⅴ中,合成时需选择温度为15℃,其目的是___________ 。
⑸SPC的保存方法是_____________________________ 。
⑹过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600g样品,置于250mL锥形瓶中,并用100mL 0.5 mol·L-1硫酸溶解完全,立即用0.02000mol·L-1 KMnO4标准溶液滴定,滴定至终点时溶液颜色为________ ,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24mL。该样品的活性氧含量为_______ %。

回答下列问题:
⑴步骤Ⅰ中
 填“有”或“没有”
填“有”或“没有” 发生氧化还原反应。
发生氧化还原反应。⑵步骤Ⅱ中会生成一种可以循环使用的物质,该物质的化学式为
⑶步骤Ⅲ中需要加热,发生反应的化学方程式为
⑷步骤Ⅴ中,合成时需选择温度为15℃,其目的是
⑸SPC的保存方法是
⑹过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600g样品,置于250mL锥形瓶中,并用100mL 0.5 mol·L-1硫酸溶解完全,立即用0.02000mol·L-1 KMnO4标准溶液滴定,滴定至终点时溶液颜色为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】亚氯酸钠( )是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
)是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)“反应”中生成 的化学方程式为:
的化学方程式为: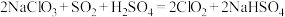 ,在此反应中氧化剂与还原剂的物质的量之比为
,在此反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和
和 ,要加入的试剂分别为
,要加入的试剂分别为_______ 、_______ 。
(3)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中氧化产物是
,此吸收反应中氧化产物是_______ 。“尾气吸收”的化学方程式为_______ 。
 )是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
)是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)“反应”中生成
 的化学方程式为:
的化学方程式为: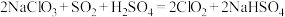 ,在此反应中氧化剂与还原剂的物质的量之比为
,在此反应中氧化剂与还原剂的物质的量之比为(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 和
和 ,要加入的试剂分别为
,要加入的试剂分别为(3)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中氧化产物是
,此吸收反应中氧化产物是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】高铁酸钾(K2FeO4)可溶于水、微溶于浓KOH溶液、难溶于无水乙醇;在强碱性溶液中比较稳定,在Fe3+或Fe(OH)3的催化作用下分解,是一种绿色高效的水处理剂。某实验小组用如图装置(加热夹持仪器已省略)制备KClO溶液,再用制得的KClO溶液与Fe(NO3)3溶液反应制备K2FeO4。
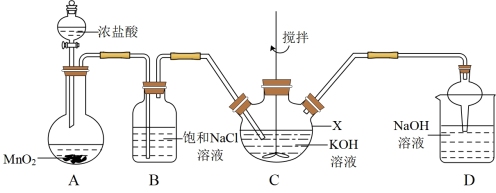
回答下列问题:
(1)K2FeO4中铁元素的化合价为_______ ,仪器X的名称为_______ 。
(2)装置B的作用是_______ (任写一点),装置D中发生反应的离子方程式为_______ 。
(3)现有①Fe(NO3)3溶液、②含KOH的KClO溶液,上述两种溶液混合时,将_______ (填标号,下同)滴入______ 中,发生的反应中氧化剂与还原剂的物质的量之比为_______ 。
(4) K2FeO4的理论产率与合成条件相应曲面投影的关系如图(虚线上的数据表示K2FeO4的理论产率)所示,则制备K2FeO4的最适宜的条件范围是_______ 。

(5)高铁酸钾是一种理想的水处理剂,其处理水的原理为_______ 。

回答下列问题:
(1)K2FeO4中铁元素的化合价为
(2)装置B的作用是
(3)现有①Fe(NO3)3溶液、②含KOH的KClO溶液,上述两种溶液混合时,将
(4) K2FeO4的理论产率与合成条件相应曲面投影的关系如图(虚线上的数据表示K2FeO4的理论产率)所示,则制备K2FeO4的最适宜的条件范围是

(5)高铁酸钾是一种理想的水处理剂,其处理水的原理为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知,短周期A、B、C、D、E、F六种主族元素,它们的原子序数依次增大,其中A的一种原子无中子,B的单质在空气中含量最高,它与A的单质在一定条件下反应生成易溶于水的化合物甲,C、E同主族,C原子的最外层电子数是其周期序数的3倍,D是短周期中原子半径最大的元素。回答下列问题:
(1)甲的电子式是_______ ;元素F最高价氧化物对应水化合物的化学式为_______ 。
(2)D、E、F的简单离子半径由大到小顺序是_______ 。
(3) 、
、 与D的最高价氧化物的水化物溶液和铂电极组成燃料电池电池的负极反应是
与D的最高价氧化物的水化物溶液和铂电极组成燃料电池电池的负极反应是_____ 。
(4)X可能是由B、D、E三种元素中的一种组成的单质,能经图所示的过程转化为W(其它条件略去)。
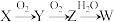
①若Z是淡黄色固体物质,则该物质含有的化学键为_______ 。
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂的物质的量之比为_______ ,将铜加入W的稀溶液中发生反应的离子方程式为_______ 。
(5)实验室可用如图所示的装置(缺收集装置)制备并收集甲。
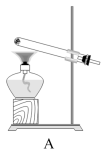
①实验室制取甲的化学方程式是_______ 。
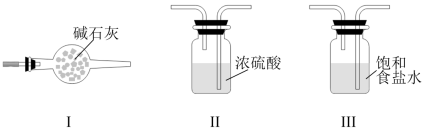
②为制取干燥的甲,可将装置A与如图所示装置_______ (填序号)进行连接。
(1)甲的电子式是
(2)D、E、F的简单离子半径由大到小顺序是
(3)
 、
、 与D的最高价氧化物的水化物溶液和铂电极组成燃料电池电池的负极反应是
与D的最高价氧化物的水化物溶液和铂电极组成燃料电池电池的负极反应是(4)X可能是由B、D、E三种元素中的一种组成的单质,能经图所示的过程转化为W(其它条件略去)。
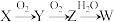
①若Z是淡黄色固体物质,则该物质含有的化学键为
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂的物质的量之比为
(5)实验室可用如图所示的装置(缺收集装置)制备并收集甲。

①实验室制取甲的化学方程式是
②为制取干燥的甲,可将装置A与如图所示装置

您最近一年使用:0次



