1898年7月,居里夫人发现了一种新的放射性元素(84号元素),建议以她祖国波兰的名字构造新元素名称钋(polonium),元素符号为Po,其表变时的核反应为 Po→
Po→ Pb+
Pb+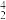 He。
He。
(1)210Po具有放射性,经衰变后形成稳定的铅,下列说法正确的是___________。
(2)已知Po的半衰期(放射性元素原子核有50%发生衰变所需的时间)为138天,那么质量为21g的Po,经276天后还剩下的Po的质量为___________ ,得到的铅的质量为___________ (计算并写出必要过程)。
 Po→
Po→ Pb+
Pb+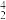 He。
He。(1)210Po具有放射性,经衰变后形成稳定的铅,下列说法正确的是___________。
| A.钋元素的质量数为210 |
| B.210Po的中子数比206Pb的多 |
| C.若一个碳原子的质量为a g,则一个210Po原子的质量是2520a g |
| D.钋元素的相对原子质量为210 |
更新时间:2023-10-25 21:55:44
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某干燥白色固体可能含有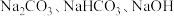 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:

(1)产生的 的物质的量为
的物质的量为_______  ,
, 段反应的离子方程式为
段反应的离子方程式为_______ 。
(2)若白色固体由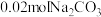 和
和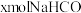 组成,则
组成,则
_______  ,
,
_______  。
。
(3)若白色固体由 和
和 组成,
组成, ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为_______ ,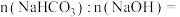
_______ 。
(4)若白色固体只由 和
和 组成,且
组成,且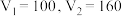 ,则
,则
_______  ,原
,原 溶液中的
溶液中的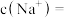
_______  。
。
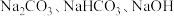 中的几种,取一定质量的该固体加蒸馏水配制
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加
溶液,并向该溶液中滴加 的盐酸,得到
的盐酸,得到 体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:
(1)产生的
 的物质的量为
的物质的量为 ,
, 段反应的离子方程式为
段反应的离子方程式为(2)若白色固体由
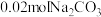 和
和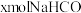 组成,则
组成,则
 ,
,
 。
。(3)若白色固体由
 和
和 组成,
组成, ,则
,则 与
与 溶于水后发生反应的离子方程式为
溶于水后发生反应的离子方程式为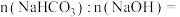
(4)若白色固体只由
 和
和 组成,且
组成,且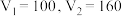 ,则
,则
 ,原
,原 溶液中的
溶液中的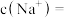
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.现有以下八种物质:
① 、②
、② 、③稀硫酸、④
、③稀硫酸、④ 溶液、⑤熔融
溶液、⑤熔融 、⑥氯水、⑦
、⑥氯水、⑦ 固体、⑧蔗糖 (C12H22O11)
固体、⑧蔗糖 (C12H22O11)
(1)以上物质中能导电的是___________ (填写编号,下同)。
(2)属于电解质的是___________ 。
(3)属于非电解质的是___________ 。
(4)溶液的导电能力由溶液中自由移动的离子浓度及其所带电荷数决定,向④中滴入同物质的量浓度的③至过量,溶液的导电能力(用I表示)的变化为___________。
Ⅱ.请回答下列问题:
(5) 与标准状况下
与标准状况下___________ 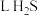 气体含有相同数目的氢原子数。
气体含有相同数目的氢原子数。
(6)标准状况下,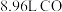 和
和 混合气体的质量为
混合气体的质量为 ,则
,则 和
和 的物质的量之比为
的物质的量之比为___________ 。
(7)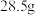 ,某金属氯化物
,某金属氯化物 中含
中含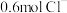 ,则M的摩尔质量为
,则M的摩尔质量为___________ 。
(8)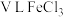 溶液中含
溶液中含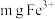 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
①
 、②
、② 、③稀硫酸、④
、③稀硫酸、④ 溶液、⑤熔融
溶液、⑤熔融 、⑥氯水、⑦
、⑥氯水、⑦ 固体、⑧蔗糖 (C12H22O11)
固体、⑧蔗糖 (C12H22O11)(1)以上物质中能导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)溶液的导电能力由溶液中自由移动的离子浓度及其所带电荷数决定,向④中滴入同物质的量浓度的③至过量,溶液的导电能力(用I表示)的变化为___________。
A.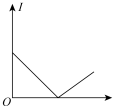 | B.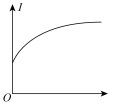 | C.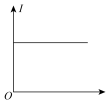 | D.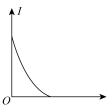 |
Ⅱ.请回答下列问题:
(5)
 与标准状况下
与标准状况下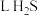 气体含有相同数目的氢原子数。
气体含有相同数目的氢原子数。(6)标准状况下,
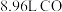 和
和 混合气体的质量为
混合气体的质量为 ,则
,则 和
和 的物质的量之比为
的物质的量之比为(7)
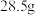 ,某金属氯化物
,某金属氯化物 中含
中含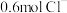 ,则M的摩尔质量为
,则M的摩尔质量为(8)
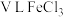 溶液中含
溶液中含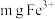 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)相同物质的量的O2和O3的质量比为__ ,分子个数比为__ ,所含氧原子的个数比为__ ,同条件下密度比__ .
(2)下列物质中:①Cl2②NH3③BaSO4④NaOH ⑤稀硝酸属于电解质的是__ ,属于非电解质的是__ .①和④反应的离子方程式__ .
(2)下列物质中:①Cl2②NH3③BaSO4④NaOH ⑤稀硝酸属于电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性.实验室可将氧气通过高压放电管来制取臭氧:3O2  2O3 。
2O3 。
(1)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为________ L。
(2)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g.则原混合气中臭氧的体积分数为________ 。
 2O3 。
2O3 。 (1)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为
(2)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g.则原混合气中臭氧的体积分数为
您最近一年使用:0次
【推荐2】无机化合物A和NaH都是重要的还原剂,遇水都强烈反应。一定条件下,2.40gNaH与气体B反应生成3.90g化合物A和2.24L(已折算成标准状况)的H2.已知气体B可使湿润红色石蕊试纸变蓝。请回答下列问题:
(1)A的化学式是_______ 。
(2)NaH与气体B反应生成化合物A的化学方程式_______ 。
(1)A的化学式是
(2)NaH与气体B反应生成化合物A的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】碘是生命体中的必需元素,碘及其化合物在生活中有重要的用途。
(1)KIO3可作为食盐中的补碘剂,KIO3中碘的化合价是__ 。
(2)实验室中制取少量碘可采用如下方法:KI+CuSO4→A(白色)↓+K2SO4+I2。16.0gCuSO4与过量KI反应后可得19.1g的A,则A的化学式为__ 。
(3)单质碘与氟气反应可制得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O H3O++OH-),生成的阳离子为IF
H3O++OH-),生成的阳离子为IF ,则阴离子为
,则阴离子为__ 。
(4)碘的纯度分析:精确量取0.1150g精制后的碘置于碘量瓶中,加入KI和水振荡至完全溶解(KI仅用于溶解)。以0.0500mol•L-1的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液17.00mL。则该碘的质量分数为多少___ ?(已知:2S2O +I2=2I-+S4O
+I2=2I-+S4O )
)
(1)KIO3可作为食盐中的补碘剂,KIO3中碘的化合价是
(2)实验室中制取少量碘可采用如下方法:KI+CuSO4→A(白色)↓+K2SO4+I2。16.0gCuSO4与过量KI反应后可得19.1g的A,则A的化学式为
(3)单质碘与氟气反应可制得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O
 H3O++OH-),生成的阳离子为IF
H3O++OH-),生成的阳离子为IF ,则阴离子为
,则阴离子为(4)碘的纯度分析:精确量取0.1150g精制后的碘置于碘量瓶中,加入KI和水振荡至完全溶解(KI仅用于溶解)。以0.0500mol•L-1的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液17.00mL。则该碘的质量分数为多少
 +I2=2I-+S4O
+I2=2I-+S4O )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2021年日本将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的不满。

(1)卡通形象中标+号的小球表示_______ (填微粒名称)。
(2)11g氚水(T216O)所含中子数为________ 个。
(3)氚和其同位素的物理性质________ (填“相同”或“不同”),化学性质________ (填“相同”或“不同”)。

(1)卡通形象中标+号的小球表示
(2)11g氚水(T216O)所含中子数为
(3)氚和其同位素的物理性质
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 微粒中的质子数是
微粒中的质子数是_______ ,中子数是_______ ,核外电子数是_______ 。它与 形成的化合物的电子式
形成的化合物的电子式_______ ,此化合物类型_______ (填“离子化合物”或“共价化合物”)。
 微粒中的质子数是
微粒中的质子数是 形成的化合物的电子式
形成的化合物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】用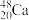 轰击
轰击 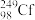 ,生成
,生成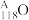 g并放出3个中子(
g并放出3个中子( )。
)。
(1)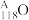 g的原子核内中子数是
g的原子核内中子数是_______ 。
(2)推测Og在元素周期表的位置_______ 。
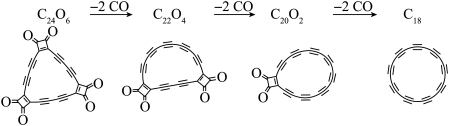
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______
(4)写出实验室制取氯气的化学方程式_______ ;
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式_______ ;
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式_______ 。
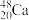 轰击
轰击 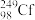 ,生成
,生成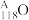 g并放出3个中子(
g并放出3个中子( )。
)。(1)
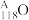 g的原子核内中子数是
g的原子核内中子数是(2)推测Og在元素周期表的位置
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______

| A.C18和金刚石、石墨互为同素异形体 |
| B.C18是一种性质很稳定的化合物 |
| C.C20O2、C22O4、C24O6随着碳原子数的增大,氧元素的质量百分含量依次增大 |
| D.C22O4、CO、CO2都是碳元素的氧化物 |
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成
 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。

请你回答:
(1)氟元素的相对原子质量为_______ ,钙元素的原子序数为_______ ;
(2)X=_______ ;
(3)A、B、C、D属于同种元素的粒子是_______ (填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_______ (填序号);
(5)某地发生了氢氟酸(HF)泄漏,消防队员用熟石灰对泄漏点进行处理,请写出化学方程式_______ 。

请你回答:
(1)氟元素的相对原子质量为
(2)X=
(3)A、B、C、D属于同种元素的粒子是
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似
(5)某地发生了氢氟酸(HF)泄漏,消防队员用熟石灰对泄漏点进行处理,请写出化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国展开“嫦娥探月”工程,向月球发起探索。2020年嫦娥五号一次带回1700多克月壤样本。研究表明,月球上有丰富的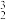 He资源,可开发用作未来的新型能源。
He资源,可开发用作未来的新型能源。
(1)α粒子是带有2个单位正电荷、质量数为4的氦离子,由此推断一个α粒子含有_____ 个电子,它的结构示意图为______ 。
(2)利用核聚变发电,3He是最安全的最清洁的能源,下列说法正确的是______ 。
(3)同温同压下,下列关于氦气和氧气的叙述中,正确的是______ 。
①氦气和氧气所含的分子数相同
②氦分子间的平均距离和氧分子间的平均距离几乎是相等的
③氦分子与氧分子的大小几乎相同
④氦分子和氧分子本身大小对于气体体积影响可以忽略不计
⑤氦气与氧气的密度之比等于32:4
(4)16克氧气含有n个O2分子,则阿伏加德罗常数可表示为______ 。
(5)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,该混合气体的平均分子量为______ ,其中氧气和氦气的分子数之比是_____ 。
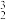 He资源,可开发用作未来的新型能源。
He资源,可开发用作未来的新型能源。(1)α粒子是带有2个单位正电荷、质量数为4的氦离子,由此推断一个α粒子含有
(2)利用核聚变发电,3He是最安全的最清洁的能源,下列说法正确的是
| A.3He、4He的化学性质基本相同 | B.3He、4He具有相同的电子数 |
| C.3He核聚变是化学变化 | D.3He液化是化学变化 |
①氦气和氧气所含的分子数相同
②氦分子间的平均距离和氧分子间的平均距离几乎是相等的
③氦分子与氧分子的大小几乎相同
④氦分子和氧分子本身大小对于气体体积影响可以忽略不计
⑤氦气与氧气的密度之比等于32:4
| A.①② | B.②④ | C.③⑤ | D.②③ |
| A.2n | B. n n | C.16n | D. n n |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)有下列6种原子:16O、17O、18O、 H、
H、 H、
H、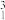 H。
H。
①元素种类有___________ 种。
②有___________ 种核素。
③其中互为同位素的是___________ 。
④这些原子可以构成水分子,其种类有___________ 种。
(2)某元素的核素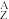 X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
①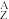 X的质量数A是
X的质量数A是___________ 。
②37 g XCl2中所含质子数的物质的量为___________ 。
(1)有下列6种原子:16O、17O、18O、
 H、
H、 H、
H、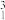 H。
H。①元素种类有
②有
③其中互为同位素的是
④这些原子可以构成水分子,其种类有
(2)某元素的核素
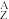 X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:①
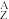 X的质量数A是
X的质量数A是②37 g XCl2中所含质子数的物质的量为
您最近一年使用:0次



