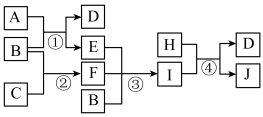
下列框图内的A~L是中学化学常见的物质,其中A由三种元素组成,E、J常温下是气体单质,F是常温下常见的液体,G是现代工业使用量最多的金属,H只有两种元素组成,L是白色难溶固体且相对分子质量为90.0。
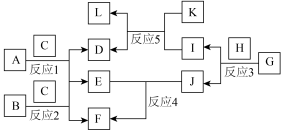
(1)A的化学式为________ 。
(2)反应1和反应2生成等量的E转移电子数目之比为_______ 。
(3)实验室不常用H来制备J的原因是________ 。
(4)写出反应5的离子反应方程式________ ,生成的L在空气中不稳定会迅速变色最后变成红褐色,写出该过程发生的化学方程式_______ 。
(5)A可以和H的浓溶液在加热下可以生成D、F和一种气体单质M,请写出该反应的化学方程式_______ ,该反应的氧化产物和还原产物质量之比为________ 。

(1)A的化学式为
(2)反应1和反应2生成等量的E转移电子数目之比为
(3)实验室不常用H来制备J的原因是
(4)写出反应5的离子反应方程式
(5)A可以和H的浓溶液在加热下可以生成D、F和一种气体单质M,请写出该反应的化学方程式
更新时间:2023-10-27 19:21:42
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
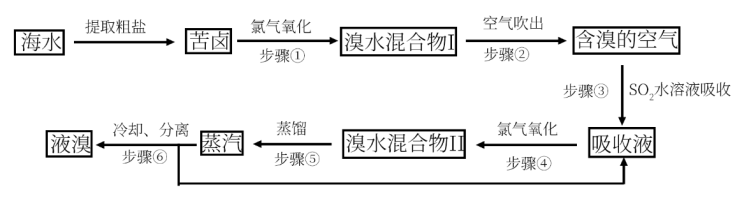
(1)步骤①获得Br2的离子反应方程式为:_________________________ 。
(2)步骤③所发生反应的化学方程式为:_________________________ 。在该反应中,氧化剂是______________ (填化学式);若反应中生成2molHBr,则转移电子数约为_____________ 个。
(3)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是:_______________ 。
(4)步骤②通入热空气或水蒸气吹出Br2,利用了溴的________ 。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(5)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:________________ 。

(1)步骤①获得Br2的离子反应方程式为:
(2)步骤③所发生反应的化学方程式为:
(3)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是:
(4)步骤②通入热空气或水蒸气吹出Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(5)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:
您最近一年使用:0次
【推荐2】抗氧化的明星营养元素硒(Se)是人体必需的微量元素,工业上从电解精炼铜的阳极泥(主要含Au、Ag、Cu、Se、CuSe、Ag2Se等)中提取硒,同时回收部分金属,工艺流程如下:
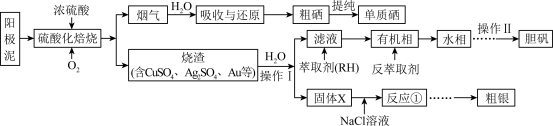
已知:
①硒(Se)的熔点217℃,沸点684.9℃,带有金属光泽。
②硒(Se)可做半导体材料,500℃下可与氧气反应。
回答下列问题:
(1)“硫酸化焙烧”即将阳极泥与浓硫酸混合均匀,在350~500℃下焙烧,为了加快该过程反应速率,该过程中可采取的措施有_______ 、_______ (回答两点即可)。
(2)烟气的主要成分为SO2、SeO2,是焙烧中CuSe与浓H2SO4反应而产生,该反应的化学方程式为_______ ;吸收与还原过程中SeO2极易溶解于水生成亚硒酸(H2SeO3),亚硒酸被烟气中的SO2还原为单质硒,若该过程中有13.44 LSO2(标准状况下)参加反应,则还原得到单质Se的质量为_______ g。
(3)粗硒需用减压蒸馏提纯得到单质硒,其原因是_______ 。
(4)上述流程中萃取与反萃取原理为2RH+Cu2+ R2Cu+2H+,反萃取剂最好选用
R2Cu+2H+,反萃取剂最好选用_______ (填化学式)溶液;操作II为_______ 、_______ 过滤、洗涤、干燥。
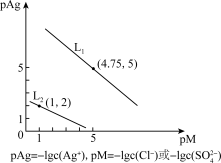
(5)已知常温下的Ag2SO4、AgC1饱和溶液中阳离子和阴离子浓度关系如图所示,其中L1表示AgCl,L2表示Ag2SO4,固体X加入NaCl溶液后,反应①Ag2SO4(s)+2Cl-(aq) 2AgCl(s)+
2AgCl(s)+ (aq),反应①的K=
(aq),反应①的K=_______ 。

已知:
①硒(Se)的熔点217℃,沸点684.9℃,带有金属光泽。
②硒(Se)可做半导体材料,500℃下可与氧气反应。
回答下列问题:
(1)“硫酸化焙烧”即将阳极泥与浓硫酸混合均匀,在350~500℃下焙烧,为了加快该过程反应速率,该过程中可采取的措施有
(2)烟气的主要成分为SO2、SeO2,是焙烧中CuSe与浓H2SO4反应而产生,该反应的化学方程式为
(3)粗硒需用减压蒸馏提纯得到单质硒,其原因是
(4)上述流程中萃取与反萃取原理为2RH+Cu2+
 R2Cu+2H+,反萃取剂最好选用
R2Cu+2H+,反萃取剂最好选用(5)已知常温下的Ag2SO4、AgC1饱和溶液中阳离子和阴离子浓度关系如图所示,其中L1表示AgCl,L2表示Ag2SO4,固体X加入NaCl溶液后,反应①Ag2SO4(s)+2Cl-(aq)
 2AgCl(s)+
2AgCl(s)+ (aq),反应①的K=
(aq),反应①的K=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)有一瓶无色澄清溶液,可能含H+、Na+、Mg2+、Ba2+、Cl-、SO 、CO
、CO 离子。现进行以下实验:
离子。现进行以下实验:
A.用pH试纸检验溶液,发现溶液呈强酸性;
B.取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C.取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有__ ;肯定不存在的离子有__ 。
②写出C中发生反应的离子方程式__ 。
(2)还原铁粉与高温水蒸气反应的化学方程式:__ ;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。__
__Fe(OH)3+__ClO-+__OH-=__FeO +__Cl-+__(___)
+__Cl-+__(___)
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___ ;当有2molH3PO4生成,转移的电子的物质的量为__ 。
 、CO
、CO 离子。现进行以下实验:
离子。现进行以下实验:A.用pH试纸检验溶液,发现溶液呈强酸性;
B.取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C.取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有
②写出C中发生反应的离子方程式
(2)还原铁粉与高温水蒸气反应的化学方程式:
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
__Fe(OH)3+__ClO-+__OH-=__FeO
 +__Cl-+__(___)
+__Cl-+__(___)(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】化合物X•3H2O是一种黄色晶体,X由四种元素组成。X•3H2O晶体的摩尔质量在400~500g·mol-1之间。取一定量的X•3H2O晶体完成如图转化,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B中阳离子具有较强的还原性,C溶液的焰色反应为紫色。
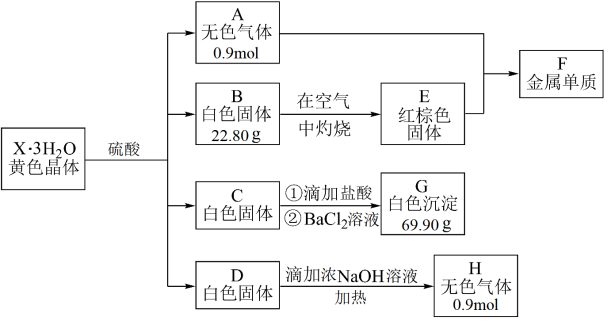
(1)A与E反应生成F的化学方程式为_______ 。
(2)B的化学式为_______ 。
(3)单质F与过量稀硝酸反应的化学方程式为_______ 。
(4)实验室收集气体H时,验满的方法是_______ 。
(5)组成X的四种元素为_______ ,黄色晶体的化学式为_______ 。

(1)A与E反应生成F的化学方程式为
(2)B的化学式为
(3)单质F与过量稀硝酸反应的化学方程式为
(4)实验室收集气体H时,验满的方法是
(5)组成X的四种元素为
您最近一年使用:0次
【推荐2】某化学兴趣小组对化合物X开展如图所示的探究实验。
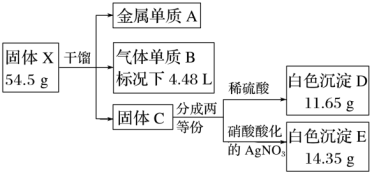
已知X是由三种元素组成的盐。阴离子的空间构型为正八面体型;金属单质A银白色,常用于实验室做焰色试验;气体B在标准状况下的密度为3.17 g·L-1;所加试剂均足量。
(1)组成X的元素有_______ ,固体C的电子式为_______ 。
(2)金属A溶于王水,生成化合物X所对应的酸和遇空气显红棕色的气体,写出金属A溶于王水的化学方程式:_______ 。
(3)已知与B中元素同主族元素之间形成的化合物的性质与气体单质B相似,在碱性环境中,XO-→X-+XO3-,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式:_______ 。
(4)某同学发现白色沉淀E在光照下颜色会变深,请解释产生该现象的原因:_______ 。

已知X是由三种元素组成的盐。阴离子的空间构型为正八面体型;金属单质A银白色,常用于实验室做焰色试验;气体B在标准状况下的密度为3.17 g·L-1;所加试剂均足量。
(1)组成X的元素有
(2)金属A溶于王水,生成化合物X所对应的酸和遇空气显红棕色的气体,写出金属A溶于王水的化学方程式:
(3)已知与B中元素同主族元素之间形成的化合物的性质与气体单质B相似,在碱性环境中,XO-→X-+XO3-,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式:
(4)某同学发现白色沉淀E在光照下颜色会变深,请解释产生该现象的原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业的汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为_________________________________________________________ ;
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式)_____________________ ;该反应是氧化还原反应,则其中的氧化剂是(填化学式)__________________________________________________ 。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为__________________________________
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式)
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.按要求回答下列问题:
(1)下列物质中① ;②乙醇;③熔融
;②乙醇;③熔融 ;④
;④ 溶液;⑤固态
溶液;⑤固态 ,其中属于电解质的是
,其中属于电解质的是___________ (只填序号,下同),属于非电解质的是___________ 。所给状态下能导电的是___________ 。
(2)配平方程式,并在方程式上用双线桥表示出电子转移情况。____________ 。

Ⅱ.下图所示装置,可用来制取 和观察
和观察 在空气中被氧化的颜色变化。实验时必须使用铁屑和
在空气中被氧化的颜色变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。
的硫酸,其他试剂任选。
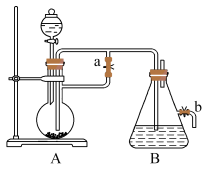
(3)实验开始时应先将活塞a___________ (填“打开”或“关闭”)。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为___________ 。
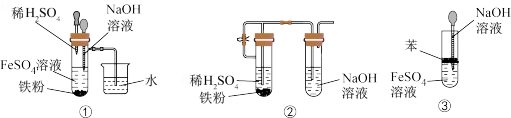
(5)下图中___________ 装置能较长时间看到 白色沉淀(填装置序号)。
白色沉淀(填装置序号)。
(1)下列物质中①
 ;②乙醇;③熔融
;②乙醇;③熔融 ;④
;④ 溶液;⑤固态
溶液;⑤固态 ,其中属于电解质的是
,其中属于电解质的是(2)配平方程式,并在方程式上用双线桥表示出电子转移情况。

Ⅱ.下图所示装置,可用来制取
 和观察
和观察 在空气中被氧化的颜色变化。实验时必须使用铁屑和
在空气中被氧化的颜色变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。
的硫酸,其他试剂任选。
(3)实验开始时应先将活塞a
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为
(5)下图中
 白色沉淀(填装置序号)。
白色沉淀(填装置序号)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室中用 溶液与
溶液与 溶液制备
溶液制备 ,装置如图,请回答下列问题:
,装置如图,请回答下列问题:
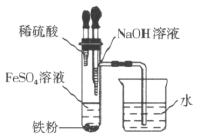
(1)配制 的
的 溶液需要的玻璃仪器有玻璃棒、
溶液需要的玻璃仪器有玻璃棒、_______ (填字母序号)。






(2)配制 溶液时使用的蒸馏水通常要煮沸,其目的是
溶液时使用的蒸馏水通常要煮沸,其目的是_______ 。
(3)制备 时,应先挤压盛有
时,应先挤压盛有_______ 的胶头滴管,目的是_______ ,烧杯中水的作用是_______ 。
(4)生成白色沉淀的离子方程式是_______ 。
 溶液与
溶液与 溶液制备
溶液制备 ,装置如图,请回答下列问题:
,装置如图,请回答下列问题:
(1)配制
 的
的 溶液需要的玻璃仪器有玻璃棒、
溶液需要的玻璃仪器有玻璃棒、





(2)配制
 溶液时使用的蒸馏水通常要煮沸,其目的是
溶液时使用的蒸馏水通常要煮沸,其目的是(3)制备
 时,应先挤压盛有
时,应先挤压盛有(4)生成白色沉淀的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.铁是生产、生活及生命中的重要元素。
(1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力。药品美蓝是其有效的解毒剂,解毒时美蓝发生___________ (填“氧化”或“还原”)反应。
(2)现有一瓶放置了一段时间的某浓度的FeCl2溶液,请设计实验检验其中是否含有Fe3+:___________ 。
(3)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。若一定量的普通铁粉和水蒸气在高温下反应生成44.8 L H2(已换算到标况下),则转移电子数目为___________ ;“引火铁”是一种极细的铁粉,它在空气中可以自燃,其原因是___________ 。
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如下实验:

气体甲可使湿润红色石蕊试纸变蓝。请回答:
(4)M的化学式为___________ 。
(5)白色沉淀乙在空气中变成红褐色沉淀丙的原因是(用化学方程式表示)___________ 。
(6)高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为___________ 。
(1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力。药品美蓝是其有效的解毒剂,解毒时美蓝发生
(2)现有一瓶放置了一段时间的某浓度的FeCl2溶液,请设计实验检验其中是否含有Fe3+:
(3)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。若一定量的普通铁粉和水蒸气在高温下反应生成44.8 L H2(已换算到标况下),则转移电子数目为
Ⅱ.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。为了研究其组成,设计如下实验:

气体甲可使湿润红色石蕊试纸变蓝。请回答:
(4)M的化学式为
(5)白色沉淀乙在空气中变成红褐色沉淀丙的原因是(用化学方程式表示)
(6)高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某工厂的工业废水中含有大量的 、较多的
、较多的 。某兴趣小组计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,回答下列问题。
。某兴趣小组计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,回答下列问题。
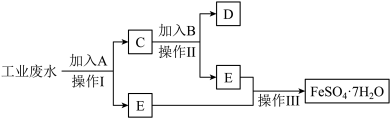
回答下列问题:
(1)A的化学式________________ C中所含物质是__________________ (填化学式)。
(2)操作I的名称是_______________ ,E是_______________________ (填化学式)。
(3)加入B后反应的离子方程式为____________________________ 。
(4)若用新制氯水和 溶液鉴定E中的金属阳离子,滴加试剂的顺序和对应现象是
溶液鉴定E中的金属阳离子,滴加试剂的顺序和对应现象是_______________ 。
(5) 古称绛矾,《新修本草》记载“绛矾本来绿色,新出窑未见风者。烧之赤色,故名绛矾矣”。下列说法错误的是________________(填标号)。
古称绛矾,《新修本草》记载“绛矾本来绿色,新出窑未见风者。烧之赤色,故名绛矾矣”。下列说法错误的是________________(填标号)。
 、较多的
、较多的 。某兴趣小组计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,回答下列问题。
。某兴趣小组计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,回答下列问题。
回答下列问题:
(1)A的化学式
(2)操作I的名称是
(3)加入B后反应的离子方程式为
(4)若用新制氯水和
 溶液鉴定E中的金属阳离子,滴加试剂的顺序和对应现象是
溶液鉴定E中的金属阳离子,滴加试剂的顺序和对应现象是(5)
 古称绛矾,《新修本草》记载“绛矾本来绿色,新出窑未见风者。烧之赤色,故名绛矾矣”。下列说法错误的是________________(填标号)。
古称绛矾,《新修本草》记载“绛矾本来绿色,新出窑未见风者。烧之赤色,故名绛矾矣”。下列说法错误的是________________(填标号)。| A.缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是防止硫酸亚铁被氧化 |
B.利用焰色试验,透过蓝色钴玻璃观察到紫色火焰,说明绛矾样品中含 |
C. 既有氧化性又有还原性还有硫酸盐的性质 既有氧化性又有还原性还有硫酸盐的性质 |
D. 属于混合物 属于混合物 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,W的单质为淡黄色固体,Y、Z左右相邻,Z、W位于同主族。
(1) X元素是_______ ;W的原子结构示意图_______ 。
(2) X与W组成的化合物中存在_______ 键(填“离子”“共价”)。
(3) Y、Z形成的简单离子的半径由大到小的顺序为_______ 。
(4)工业上由X的单质与Y的单质化合生成1molA气体时放出46.2kJ的热量,写出该反应的热化学方程式_______ 。
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为_______ 。
②已知1 mol·L-1 100mL B的溶液能与1 mol·L-1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式_______ 。
(1) X元素是
(2) X与W组成的化合物中存在
(3) Y、Z形成的简单离子的半径由大到小的顺序为
(4)工业上由X的单质与Y的单质化合生成1molA气体时放出46.2kJ的热量,写出该反应的热化学方程式
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为
②已知1 mol·L-1 100mL B的溶液能与1 mol·L-1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式
您最近一年使用:0次