过量的铁粉跟一定量的稀硫酸反应时,为了减慢反应速率,且不影响生成氢气的总量,可以采取的措施是
| A.升高温度 | B.加入 固体 固体 |
| C.加入氯化钠溶液 | D.加入少量 固体 固体 |
更新时间:2023-10-31 07:00:04
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列事实不能证明醋酸是弱酸的是( )
A.常温下,测得醋酸钠溶液的 |
| B.醋酸可以使紫色石蕊试液变红 |
| C.物质的量浓度相同时,锌粒跟盐酸反应的速率比与醋酸反应的快 |
D.常温下,测得  醋酸溶液的 醋酸溶液的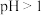 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是
| A.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 |
| B.将大小、形状相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 |
| C.向两支试管中分别加入2mL5%H2O2溶液和2mL10%的H2O2溶液,再向其中各加入相同质量的二氧化锰,产生氧气的快慢不同 |
| D.两支试管中分别加入2mL0.1mol/LNa2S2O3溶液与2mL0.1mol/L稀硫酸的混合溶液,其中一支试管放入冷水中,另一支试管放入热水中,产生浑浊的快慢不同 |
您最近一年使用:0次
【推荐3】下列相关实验不能达到预期目的的是
| 相关实验 | 预期目的 | |
| A | 在两支试管中各加入4 mL 0.01 mol/L的KMnO4 酸性溶液,再分别加入0.1 mol/L H2C2O4 溶液2 mL、0.2 mol/LH2C2O4 溶液2 mL,分别记录溶液褪色所需时间 | 探究相同条件下,溶液浓度对反应速率的影响 |
| B | 向少量火柴头的浸泡液中滴加AgNO3、足量稀HNO3和NaNO2溶液 | 验证火柴头含有氯元素 |
| C | 向盛有少量溴乙烷的试管中,先加入氢氧化钠溶液,再滴入用硝酸酸化的硝酸银溶液 | 检验溴乙烷发生消去反应的产物 |
| D | 两支试管中装有等体积、等浓度H2O2溶液,向其中一支试管中加入FeCl3溶液 | 探究FeCl3溶液对H2O2分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气进行回收,使SO2转化生成S。催化剂不同,其他条件相同(浓度、温度、压强)情况下, 相同时间内SO2的转化率随反应温度的变化如下图,下列说法不正确的是
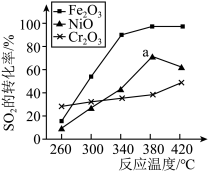

| A.不考虑催化剂价格因素,选择Fe2O3作催化剂可以节约能源 |
| B.选择Fe2O3作催化剂,最适宜温度为340 ℃左右 |
| C.a 点后SO2的转化率减小的原因可能是温度升高催化剂活性降低了 |
| D.其他条件相同的情况下,选择Cr2O3作催化剂,SO2的平衡转化率最小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应中产生气泡最快 的是 ( )
| 温度 | 浓度 | 催化剂 | |
| A | 25 ℃ | 2 mL 5% H2O2 | 0.1 mol·L-1 FeCl3 2滴 |
| B | 35 ℃ | 2 mL 8% H2O2 | MnO2粉末 |
| C | 25 ℃ | 2 mL 5% H2O2 | MnO2粉末 |
| D | 25 ℃ | 2 mL 8% H2O2 | 无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐3】我国有世界储量第一的天然石膏(主要成分CaSO4),同时也有大量磷酸工业副产品石膏,可用于硫酸及水泥的联合生产。硫酸钙在高温下被CO还原,发生的反应有:
I.CaSO4(s)+4CO(g)⇌CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)⇌4CaO(s)+4SO2(g) K3
上述反应的平衡常数的对数值(lgK)与温度(T)的关系如图所示。下列说法错误的是( )
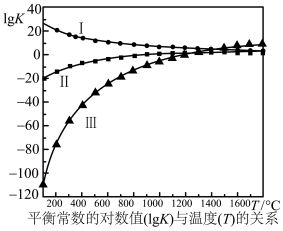
I.CaSO4(s)+4CO(g)⇌CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)⇌4CaO(s)+4SO2(g) K3
上述反应的平衡常数的对数值(lgK)与温度(T)的关系如图所示。下列说法错误的是( )

| A.反应II的△H>0 |
| B.lgK3=4lgK2−lgK1 |
| C.使用适当的催化剂能够加快反应速率,提高原料的平衡转化率 |
| D.调控适当的温度可以抑制反应I促进反应III而得到较纯净的CaO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表。忽略溶液体积变化,下列叙述不正确的是
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.6 | 16.8 | 22.4 | 26.5 | 29.9 |
| A.该反应可用MnO2、FeCl3溶液作为催化剂 |
| B.0~4 min的平均反应速率v(H2O2)=3.75×10-2mol/(L·min) |
| C.0~10 min,过氧化氢的分解速率逐渐加快 |
| D.反应到6 min时,H2O2分解了50% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】100 ml 6 mol/L H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A.Na2SO4(s) | B.H2O | C.NaOH溶液 | D.4 mol/L H2SO4 |
您最近一年使用:0次



