早期人们用氯气Cl2给自来水消毒。下列方法均可制得氯气:
①MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
②KMnO4+HCl(浓)=KCl+Cl2↑+H2O+MnCl2
(1)反应①中,MnO2发生了_______ 反应,是_______ 剂。
(2)反应②中KMnO4、Cl2的氧化性由强到弱的顺序是_______ 。
(3)并用单线桥法表示下列反应方程式的电子转移方向和数目:_______ 。
Fe+CuSO4=Cu+FeSO4
(4)该反应中有64gCu生成时,有_______ gFe被氧化。
(5)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中氧化剂为_______ ,还原剂为_______ ,氧化产物_______ ,还原产物_______ 。
(6)上反应中被还原的元素为_______ ,被氧化的元素为_______ ,该反应中硝酸既表现_______ 性,又表现_______ 性。
①MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
②KMnO4+HCl(浓)=KCl+Cl2↑+H2O+MnCl2
(1)反应①中,MnO2发生了
(2)反应②中KMnO4、Cl2的氧化性由强到弱的顺序是
(3)并用单线桥法表示下列反应方程式的电子转移方向和数目:
Fe+CuSO4=Cu+FeSO4
(4)该反应中有64gCu生成时,有
(5)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中氧化剂为
(6)上反应中被还原的元素为
更新时间:2023-11-10 10:53:31
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】氧化还原反应在生产生活中具有广泛的用途,请根据相关知识完成以下填空:
(1)实验室制取氢气的反应原理:Fe+H2SO4=FeSO4+H2↑。其中被还原的元素是___ ,氧化剂是___ ,氧化产物是___ ,还原产物是___ ,当生成1molH2时,有___ mol电子转移。
(2)在反应Cl2+NaOH=NaCl+NaClO+H2O中,被氧化与被还原的氯原子数之比为___ 。
(1)实验室制取氢气的反应原理:Fe+H2SO4=FeSO4+H2↑。其中被还原的元素是
(2)在反应Cl2+NaOH=NaCl+NaClO+H2O中,被氧化与被还原的氯原子数之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】每逢南方的梅雨季节,盒里的饼干就很容易受潮变软,不再酥脆了。有一种食品干燥剂——泡沫铁粉,是铁粉在高温炉里加入发泡剂,使铁粉变成疏松多孔的物质。饼干盒里有了它,铁粉吸收空气中的水分和氧气,自己变为铁锈,但食品的保质期却可以大大延长,味正如初。铁单质是由铁矿石冶炼得到的。

(1)问题一:铁生锈的过程中,铁发生什么反应_____ ?化合价如何变化_______ ?
(2)问题二:铁矿石一般用CO还原Fe2O3得到Fe,写出该反应的化学方程式,并用双线桥表示电子转移的方向和数目_______ 。若生成一分子CO2,转移电子数为多少_____ ?该反应是置换反应吗_______ ?

(1)问题一:铁生锈的过程中,铁发生什么反应
(2)问题二:铁矿石一般用CO还原Fe2O3得到Fe,写出该反应的化学方程式,并用双线桥表示电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)0.2L1.0molL﹣1NaCl溶液与0.1L1.0molL﹣1MgCl2溶液中的Cl﹣的物质的量浓度之比为_______ 。
(2)配制90mL1mol/LCuSO4溶液,需要胆矾_______ g。
(3)某元素R的简单阳离子Rn+核外有a个电子,中子数为b,则其质量数为_______ 。
(4)氨气常用此反应N2+3H2=2NH3合成,请用双线桥法表示该反应的电子转移的方向和数目_______ 。
(1)0.2L1.0molL﹣1NaCl溶液与0.1L1.0molL﹣1MgCl2溶液中的Cl﹣的物质的量浓度之比为
(2)配制90mL1mol/LCuSO4溶液,需要胆矾
(3)某元素R的简单阳离子Rn+核外有a个电子,中子数为b,则其质量数为
(4)氨气常用此反应N2+3H2=2NH3合成,请用双线桥法表示该反应的电子转移的方向和数目
您最近一年使用:0次
【推荐2】储氢碳纳米管的研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的碳纳米颗粒杂质。这种碳纳米颗粒可用氧化气化法提纯反应的方程式为: 3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。回答下列问题:
(1)该反应中还原剂是_______ (填化学式),被还原的元素是_______ (填元素符号)。
(2)该反应中,K2Cr2O7表现出_______ (填氧化性或者还原性)。
(3)H2SO4在该反应中表现出_______(填字母)。
(4)该反应中,还原反应得到的生成物是_______ (填化学式)。
(5)用单线桥标明电子转移方向和数目_______ 。
(6)每生成2mol水分子,转移_______ mol电子。
(1)该反应中还原剂是
(2)该反应中,K2Cr2O7表现出
(3)H2SO4在该反应中表现出_______(填字母)。
| A.只有酸性 | B.只有氧化性 | C.酸性和氧化性 | D.酸性和还原性 |
(5)用单线桥标明电子转移方向和数目
(6)每生成2mol水分子,转移
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。请回答下列问题:

(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。
(2)漂白液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生Cl2,请用离子方程式表示其原因_______ 。
(3)二氧化氯是一种高效消毒剂。工业制备ClO2的反应为:2NaClO3+4HCl=2ClO2 +Cl2
+Cl2 +2H2O+2NaCl
+2H2O+2NaCl
①用单线桥 表示反应过程中的电子转移情况_______ 。
②该反应的氧化剂与还原剂的物质的量之比为_______ ;若反应过程中消耗0.1molNaClO3,转移电子的数目为_______ 。
③ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是_______ (填字母)。
A.O3 B.FeSO4 C.KI D.KMnO4

(1)根据图中信息写出Y、Z的化学式
(2)漂白液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生Cl2,请用离子方程式表示其原因
(3)二氧化氯是一种高效消毒剂。工业制备ClO2的反应为:2NaClO3+4HCl=2ClO2
 +Cl2
+Cl2 +2H2O+2NaCl
+2H2O+2NaCl ①用
②该反应的氧化剂与还原剂的物质的量之比为
③ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是A.O3 B.FeSO4 C.KI D.KMnO4
您最近一年使用:0次
【推荐1】下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答有关问题:
(1)反应①中,浓HCl的作用为___ 。
(2)反应②的离子方程式为___ 。
(3)请将反应③配平:___ 。
KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为__ 。
(5)已知反应④:4HCl(g)+O2 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为___ 。
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②KClO3+6HCl=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答有关问题:
(1)反应①中,浓HCl的作用为
(2)反应②的离子方程式为
(3)请将反应③配平:
KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(5)已知反应④:4HCl(g)+O2
 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某学生往一支试管中按一定的顺序分别加入下列几种物质(一种物质只加一次):
A.KI溶液 B.淀粉溶液 C.NaOH溶液 D.稀H2SO4 E.氯水
发现溶液颜色按如下顺序变化:①无色→②紫色→③蓝色→④无色→⑤蓝色。依据溶液颜色的变化,回答下列问题:
(1)加入以上药品的顺序是(写序号)____________________________________________ 。
(2)①→②反应的化学方程式为_______________________________________________ 。
(3)溶液由紫色变为蓝色的原因是___________________________________________ 。
(4)③→④反应的化学方程式为________________________________________________ 。
A.KI溶液 B.淀粉溶液 C.NaOH溶液 D.稀H2SO4 E.氯水
发现溶液颜色按如下顺序变化:①无色→②紫色→③蓝色→④无色→⑤蓝色。依据溶液颜色的变化,回答下列问题:
(1)加入以上药品的顺序是(写序号)
(2)①→②反应的化学方程式为
(3)溶液由紫色变为蓝色的原因是
(4)③→④反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题
(1)高铁酸钾 是一种新型、高效、多功能绿色水处理剂,且无二次污染。
是一种新型、高效、多功能绿色水处理剂,且无二次污染。 中
中 为
为___________ 价,盐酸中加入少量 固体,产生
固体,产生 ,
, 被还原成
被还原成 ,该反应的化学方程式是
,该反应的化学方程式是___________ 。
(2) 是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 。用单线桥标出电子转移的方向和数目:
。用单线桥标出电子转移的方向和数目:___________ 。
(3)已知常温下在溶液中可发生如下反应: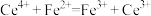 ,
,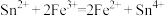 。由此可以确定
。由此可以确定 、
、 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是___________ 。
(1)高铁酸钾
 是一种新型、高效、多功能绿色水处理剂,且无二次污染。
是一种新型、高效、多功能绿色水处理剂,且无二次污染。 中
中 为
为 固体,产生
固体,产生 ,
, 被还原成
被还原成 ,该反应的化学方程式是
,该反应的化学方程式是(2)
 是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 。用单线桥标出电子转移的方向和数目:
。用单线桥标出电子转移的方向和数目:(3)已知常温下在溶液中可发生如下反应:
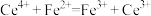 ,
,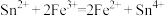 。由此可以确定
。由此可以确定 、
、 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是
您最近一年使用:0次

 4NO+6H2O反应。
4NO+6H2O反应。

