下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答有关问题:
(1)反应①中,浓HCl的作用为___ 。
(2)反应②的离子方程式为___ 。
(3)请将反应③配平:___ 。
KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为__ 。
(5)已知反应④:4HCl(g)+O2 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为___ 。
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②KClO3+6HCl=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答有关问题:
(1)反应①中,浓HCl的作用为
(2)反应②的离子方程式为
(3)请将反应③配平:
KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(5)已知反应④:4HCl(g)+O2
 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
20-21高一上·河北石家庄·期中 查看更多[3]
河北省石家庄市第十七中学2020-2021学年高一上学期期中考试化学试题(已下线)专题四 氯及其化合物(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)第06练 氯及其化合物-2022年【寒假分层作业】高一化学(人教版2019)
更新时间:2021-03-22 16:53:15
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知:Fe+2FeCl3=3FeCl2,Cu+2FeCl3=CuCl2+2FeCl2.将Fe、Cu粉与FeCl3溶液混合放在某一容器里,根据下述情况判断哪些阳离子或金属单质存在,哪些不能存在.
(1)反应后铁有剩余,则容器里可能有_____ .
(2)反应后有Cu2+和Cu,则容器里不可能有_____ .
(3)反应后有Cu2+,Fe3+,则容器里不可能有_____ .
(1)反应后铁有剩余,则容器里可能有
(2)反应后有Cu2+和Cu,则容器里不可能有
(3)反应后有Cu2+,Fe3+,则容器里不可能有
您最近一年使用:0次
【推荐2】氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)下列实验过程中的颜色变化,与氧化还原反应有关的是_______(填字母)。
(2)反应: 。该反应中氧化产物为
。该反应中氧化产物为_______ 。
(3)已知下列三个氧化还原反应:
① ;
;
② ;
;
③ (浓)
(浓) 。
。
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的_______ (从上述三个反应中选择)作氧化剂。
(4)无水情况下, 可以和
可以和 发生如下反应:
发生如下反应:
_______ _______
_______ _______Fe+_______
_______Fe+_______ _______
_______ _______
_______
配平上述反应方程式,单线桥法标出电子转移的方向和数目_______ 。
(5)向含有 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 溶液,结果溶液变为红色。已知:还原性:
溶液,结果溶液变为红色。已知:还原性: ;则下列叙述中正确的是
;则下列叙述中正确的是_______ (填序号)。
①氧化性: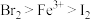
②原溶液中 一定被氧化
一定被氧化
③通入氯气后,原溶液中的 定被氧化
定被氧化
④不能确定通入氯气后的溶液中是否还存在
(6)下列转化中,不需要加入还原剂或氧化剂就能实现的是_______(填字母)。
(7) 反应中被还原和被氧化的N原子数之比为
反应中被还原和被氧化的N原子数之比为_______ 。
(1)下列实验过程中的颜色变化,与氧化还原反应有关的是_______(填字母)。
A.淡黄色 固体露置于空气中,逐渐变成白色 固体露置于空气中,逐渐变成白色 |
| B.用强光照射氯水,一段时间后溶液变成无色 |
| C.向氯水中滴加KI溶液,溶液变成棕黄色 |
D.向 溶液中滴加 溶液中滴加 溶液,产生红褐色沉淀 溶液,产生红褐色沉淀 |
 。该反应中氧化产物为
。该反应中氧化产物为(3)已知下列三个氧化还原反应:
①
 ;
;②
 ;
;③
 (浓)
(浓) 。
。若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的(4)无水情况下,
 可以和
可以和 发生如下反应:
发生如下反应:_______
 _______
_______ _______Fe+_______
_______Fe+_______ _______
_______ _______
_______
配平上述反应方程式,单线桥法标出电子转移的方向和数目
(5)向含有
 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 溶液,结果溶液变为红色。已知:还原性:
溶液,结果溶液变为红色。已知:还原性: ;则下列叙述中正确的是
;则下列叙述中正确的是①氧化性:
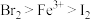
②原溶液中
 一定被氧化
一定被氧化③通入氯气后,原溶液中的
 定被氧化
定被氧化④不能确定通入氯气后的溶液中是否还存在

(6)下列转化中,不需要加入还原剂或氧化剂就能实现的是_______(填字母)。
A. | B. |
C. | D. |
 反应中被还原和被氧化的N原子数之比为
反应中被还原和被氧化的N原子数之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。下列反应可制得ClO2:NaClO3+ H2O2+ H2SO4→ClO2↑+Na2SO4+O2↑+H2O(未配平)
(1)反应中被氧化的元素是_______ ,每生成2a个ClO2时有_______ 个电子转移。
(2)写出配平后的方程式:_______ ,并用“单线桥”表示电子转移的方向和数目。
(3)上述反应中氧化性强弱排序为_______ >______
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将MnO 还原为Mn2+,自己转化为SO
还原为Mn2+,自己转化为SO ,写出反应的离子方程式:
,写出反应的离子方程式:_______ 。
(1)反应中被氧化的元素是
(2)写出配平后的方程式:
(3)上述反应中氧化性强弱排序为
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将MnO
 还原为Mn2+,自己转化为SO
还原为Mn2+,自己转化为SO ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.(1)下列右侧对左侧物质的描述与左侧任何物质都不对应的是_________ (填右侧小写的编号);
物质 描述
A.四氧化三铁 a.自来水消毒剂
B.过氧化钠 b.工业制玻璃
C.碳酸氢钠 c.红色油漆和涂料
D.硅酸钠 d.木材防火剂
E.明矾 e.呼吸面具中氧气的来源
F.青铜 f.制光纤的材料
G.硅 g.用量最大的金属材料
H.氯气 h.焰色反应为绿色
II.(2)明矾溶液中加少量Ba(OH)2溶液的离子方程式______________ ;
(3)漂白粉溶液中通过量CO2的离子方程式________________ ;
(4)将KFe2Si3O8(OH)2改写为氧化物的形式________________ ,1mol KFe2Si3O8(OH)2和足量稀盐酸反应,消耗HCl的物质的量为________ mol;
(5)配平下面的离子方程式,并用双线桥表示反应的电子转移:______
SO32- + MnO4- + — SO42-+ Mn2+ +______
III.(6)若要除去下列物质中的杂质(括号内为杂质),请将选用的试剂填入表格。
物质 描述
A.四氧化三铁 a.自来水消毒剂
B.过氧化钠 b.工业制玻璃
C.碳酸氢钠 c.红色油漆和涂料
D.硅酸钠 d.木材防火剂
E.明矾 e.呼吸面具中氧气的来源
F.青铜 f.制光纤的材料
G.硅 g.用量最大的金属材料
H.氯气 h.焰色反应为绿色
II.(2)明矾溶液中加少量Ba(OH)2溶液的离子方程式
(3)漂白粉溶液中通过量CO2的离子方程式
(4)将KFe2Si3O8(OH)2改写为氧化物的形式
(5)配平下面的离子方程式,并用双线桥表示反应的电子转移:
SO32- + MnO4- + — SO42-+ Mn2+ +______
III.(6)若要除去下列物质中的杂质(括号内为杂质),请将选用的试剂填入表格。
| 物质(杂质) | 试剂 |
| NaHCO3溶液(Na2CO3) | ① |
| FeCl3溶液(FeCl2) | ② |
| SiO2(CaCO3) | ③ |
| Fe2O3(SiO2) | ④ |
您最近一年使用:0次
【推荐2】(1)从元素的化合价态上判断,下列物质中的硫元素不能表现氧化性的是______________ 。
A.Na2S B.S C.SO2 D.H2SO4
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的还原剂是_____________ , 还原产物是___________ 。
②HNO3在该反应中表现出来的性质是____________________ 。
③当反应中生成标准状况下NO的体积是2.24 L ,此时转移的电子为___________ mol。
④请把各物质填在下面空格处,需配平:_________ +__________ =__________ +___________ +___________ +________ 。
A.Na2S B.S C.SO2 D.H2SO4
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的还原剂是
②HNO3在该反应中表现出来的性质是
③当反应中生成标准状况下NO的体积是2.24 L ,此时转移的电子为
④请把各物质填在下面空格处,需配平:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)现有①Na2CO3溶液 ②液态氯化氢 ③CCl4④Cl2⑤熔融BaCl2回答下列问题:属于电解质的是 ___________ (填代号,下同);能导电的是___________ 属于共价化合物的是___________
(2)写出CCl4的结构式___________ 写出BaCl2的电子式___________
(3)由铜片、锌片和200mL稀硫酸组成的原电池中,则当铜片上共放出3.36L(标准状况)气体时,硫酸恰好全部作用完。写出正极的电极反应式:___________ 。有___________ mol电子通过了导线
(4)其实验室制备NH3的化学方程式__________ ,实验室制氯气的离子方程式 ___________
(2)写出CCl4的结构式
(3)由铜片、锌片和200mL稀硫酸组成的原电池中,则当铜片上共放出3.36L(标准状况)气体时,硫酸恰好全部作用完。写出正极的电极反应式:
(4)其实验室制备NH3的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求完成方程式:
(1)固体碳酸氢钠加热分解的化学方程式_______ ;
(2)铝与氢氧化钠溶液反应的化学方程式_______ ;
(3)二氧化锰和浓盐酸共热制取氯气的离子方程式:_______ ;
(4)过氧化钠与水反应的离子方程式:_______ 。
(1)固体碳酸氢钠加热分解的化学方程式
(2)铝与氢氧化钠溶液反应的化学方程式
(3)二氧化锰和浓盐酸共热制取氯气的离子方程式:
(4)过氧化钠与水反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氯气是一种重要的化工原料,可用于生产塑料、合成纤维和染料等。实验室某实验小组现用下图装置来制取氯气并对氯气的某些性质和用途进行探究(K为开关,夹持装置已省略)。请回答下列问题:
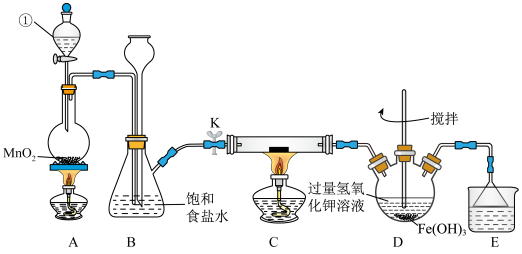
(1)仪器①的名称为___________ 。
(2)检验装置A、B的气密性:将仪器①的活塞和开关K关闭,从长颈漏斗处加水至液面高于锥形瓶中的液面,若___________ ,则说明装置气密性良好。
(3)装置A中发生反应的化学方程式为___________ ,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)装置E中的试剂是___________ ,作用是___________ 。
(5)装置C中为湿润的KI-淀粉试纸,通入 后试纸变蓝,则该反应的离子方程式为
后试纸变蓝,则该反应的离子方程式为___________ ;该小组为了研究干燥的氯气与金属钠之间的反应,欲在装置C中直接放置一块纯净的金属钠进行实验,该方案存在不妥之处,请你指出不妥之处并改正:___________ 。
(6)高铁酸盐是一种新型强氧化剂,在电池材料和水处理等方面具有广泛的应用前景。上图中的装置D可用于实验室制备高铁酸钾( ),反应原理如下,请用单线桥表示出该反应的电子转移情况:
),反应原理如下,请用单线桥表示出该反应的电子转移情况:
_________ 。

(1)仪器①的名称为
(2)检验装置A、B的气密性:将仪器①的活塞和开关K关闭,从长颈漏斗处加水至液面高于锥形瓶中的液面,若
(3)装置A中发生反应的化学方程式为
(4)装置E中的试剂是
(5)装置C中为湿润的KI-淀粉试纸,通入
 后试纸变蓝,则该反应的离子方程式为
后试纸变蓝,则该反应的离子方程式为(6)高铁酸盐是一种新型强氧化剂,在电池材料和水处理等方面具有广泛的应用前景。上图中的装置D可用于实验室制备高铁酸钾(
 ),反应原理如下,请用单线桥表示出该反应的电子转移情况:
),反应原理如下,请用单线桥表示出该反应的电子转移情况:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】过氧化氢的水溶液俗称双氧水,是化学实验室和医疗领域中的常用物质。为研究过氧化氢的性质,同学们进行了如下思考。
(1)过氧化氢中氧元素的化合价是_______ ,由此预测过氧化氢具有_______ (填“氧化性”“还原性”或“氧化性与还原性”)。
(2)双氧水可用于实验室制取氧气,反应的化学方程式是_______ ,该反应中每生成 氧气,转移电子
氧气,转移电子_______  。
。
(3)医疗中常利用化学反应 间接测定过氧化氢酶的活性,从氧化还原反应的角度分析,
间接测定过氧化氢酶的活性,从氧化还原反应的角度分析, 是该反应的
是该反应的_______ 剂,氧化产物是_______ 。
(1)过氧化氢中氧元素的化合价是
(2)双氧水可用于实验室制取氧气,反应的化学方程式是
 氧气,转移电子
氧气,转移电子 。
。(3)医疗中常利用化学反应
 间接测定过氧化氢酶的活性,从氧化还原反应的角度分析,
间接测定过氧化氢酶的活性,从氧化还原反应的角度分析, 是该反应的
是该反应的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知制备 的方法可以为:
的方法可以为: 。
。
(1)用双线桥法表示该反应电子转移的方向和数目______ 。
(2)反应中氧化剂是_______ ,氧化产物是_______ ,被还原与未被还原的 的质量之比为
的质量之比为_______ ;
(3) 在上述反应中显示出来的性质是_______;
在上述反应中显示出来的性质是_______;
(4)若有 (标准状况)
(标准状况) 生成,反应中转移电子的数目为
生成,反应中转移电子的数目为_______ 。
 的方法可以为:
的方法可以为: 。
。(1)用双线桥法表示该反应电子转移的方向和数目
(2)反应中氧化剂是
 的质量之比为
的质量之比为(3)
 在上述反应中显示出来的性质是_______;
在上述反应中显示出来的性质是_______;| A.氧化性 | B.还原性 | C.酸性 | D.挥发性 |
 (标准状况)
(标准状况) 生成,反应中转移电子的数目为
生成,反应中转移电子的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】由于NaNO2有毒,将含该物质的废水直接排放会引起水体的严重污染,所以这种废水必须经处理后才能排放。处理方法之一的原理如下:
 NaNO2+
NaNO2+ KI+
KI+ →
→ NO↑+
NO↑+ I2+
I2+ K2SO4+
K2SO4+ Na2SO4+
Na2SO4+
(1)请完成并配平该化学方程式___ 。
(2)在上述反应中,若要生成25.4gI2,则电子转移了____ 个。
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是____ 。现用铵盐来处理亚硝酸钠就能解决这个问题,写出这个离子方程式:___ 。
(4)亚硝酸钠可以与酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生分解反应:3HNO2=2NO↑+HNO3+H2O。请从浓醋酸、氨水、纯碱、稀盐酸、碘化钾溶液、淀粉溶液中选择适当的物质,设计两个简单的实验鉴别NaNO2和NaCl。
方案1:所加试剂是____ (限用一种试剂),现象是____ 。
方案2:所加试剂是____ ,现象是____ 。
 NaNO2+
NaNO2+ KI+
KI+ →
→ NO↑+
NO↑+ I2+
I2+ K2SO4+
K2SO4+ Na2SO4+
Na2SO4+
(1)请完成并配平该化学方程式
(2)在上述反应中,若要生成25.4gI2,则电子转移了
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)亚硝酸钠可以与酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生分解反应:3HNO2=2NO↑+HNO3+H2O。请从浓醋酸、氨水、纯碱、稀盐酸、碘化钾溶液、淀粉溶液中选择适当的物质,设计两个简单的实验鉴别NaNO2和NaCl。
方案1:所加试剂是
方案2:所加试剂是
您最近一年使用:0次

 ),高温时将
),高温时将 转化为
转化为 的化学方程式是
的化学方程式是

