工业上制备纯碱的原理为:NaCl+CO2+NH3+H2O=NH4Cl+NaHCO3,请回答下列问题:
(1)上述反应体系中出现的几种短周期元素中,第二周期元素原子半径由大到小的顺序是___________ 。
(2)反应体系中出现的非金属元素,可形成多种化合物,其中和铵根离子空间构型相同,且属于有机物的电子式是___________ ,该分子为___________ (填“极性”或“非极性”)分子。
(3)化合物FeF3熔点高于1000℃而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的原因可能是___________ 。
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。
①FeO立方晶胞结构如图甲所示,则Fe2+的配位数为___________ ,与O2-紧邻的所有Fe2+构成的几何构型为___________ 。
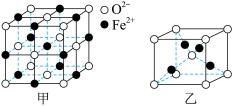
②Cu2O立方晶胞结构如图乙所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为___________ g·cm-3(用含a、NA的代数式表示,NA代表阿伏加德罗常数的值)。
(1)上述反应体系中出现的几种短周期元素中,第二周期元素原子半径由大到小的顺序是
(2)反应体系中出现的非金属元素,可形成多种化合物,其中和铵根离子空间构型相同,且属于有机物的电子式是
(3)化合物FeF3熔点高于1000℃而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的原因可能是
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。
①FeO立方晶胞结构如图甲所示,则Fe2+的配位数为

②Cu2O立方晶胞结构如图乙所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为
更新时间:2023-11-10 22:02:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】部分中学化学常见元素原子结构及性质如表所示:
(1)A元素在周期表中的位置为_____________________________________ 。
(2)B原子核外电子云有_____ 种伸展方向,B与C形成的化合物的化学式为________ 。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是_____________ 。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显______ 性,N的结构式为________ 。
③C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱______ 。
(4)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写)__________________ 。
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D原子核外电子运动状态有13种 |
| ⑤ | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(2)B原子核外电子云有
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显
③C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱
(4)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主, 中的化学键从形成的过程来看属于
中的化学键从形成的过程来看属于___________ (填“ ”或“
”或“ ”)键,从其极性来看属于
”)键,从其极性来看属于___________ (填“极性”或“非极性”)键。
(2) 、HCN、CO、
、HCN、CO、 分子中属于非极性分子的是
分子中属于非极性分子的是___________ ;与 互为等电子体的阳离子是
互为等电子体的阳离子是___________ 。(等电子体:原子数目相同,价电子总数相同的微粒。)
(3)有机物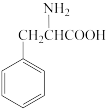 中含氧官能团的名称为
中含氧官能团的名称为___________ ,其中含有___________ 个手性碳原子。
(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的原因是___________ 。
(1)碳在形成化合物时,其键型以共价键为主,
 中的化学键从形成的过程来看属于
中的化学键从形成的过程来看属于 ”或“
”或“ ”)键,从其极性来看属于
”)键,从其极性来看属于(2)
 、HCN、CO、
、HCN、CO、 分子中属于非极性分子的是
分子中属于非极性分子的是 互为等电子体的阳离子是
互为等电子体的阳离子是(3)有机物
 中含氧官能团的名称为
中含氧官能团的名称为(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】以北京大学马丁教授为代表的多个团队,研发出了高效的铁基(如FeC、Fe2C、Fe5C2、Fe3C)费托合成催化剂,以H2和CO为原料可高产率合成烯烃、烷烃,如3CO(g)+ 6H2(g)  CH3CH=CH2(g)+3H2O(g)、nCO+(2n+1)H2
CH3CH=CH2(g)+3H2O(g)、nCO+(2n+1)H2 CnH2n+2+nH2O,为煤的气化、液化使用开拓了新途径。
CnH2n+2+nH2O,为煤的气化、液化使用开拓了新途径。
(1)Fe3+中能量最高的能级上的电子云有_____ 种伸展方向,位于不同方向中运动的电子的能量大小关系是_________ 。当Fe原子电子排布由[Ar]3d64s2→[Ar]3d64s14p1时,体系的能量_______ (填“增大”或“减小”)。
(2)Fe、C、O三种元素的第一电离能由大到小的顺序为_____________ ;CH3CH=CH2分子中碳原子的杂化轨道类型为____ ,题干所述反应中CO分子中断裂的化学键类型为______ (填字母)。
A. 2个σ键、1个π键 B. 1个σ键、2个π键 C. 非极性键
(3)新戊烷[(CH3)4C]分子中5个碳原子形成的空间构型是____________ ,该分子是________ (填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高.其原因是__________ 。
(4)碳铁之间可形成多种化合物,其中一种化合物的晶体结构(面心立方结构)如图所示:
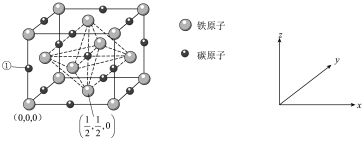
则编号为①的原子的坐标为_______________ ;该化合物的化学式为_______________ ,设该晶体的晶胞多数为a pm,阿伏加 德罗常数的值为NA,则该晶体的密度为_______________ g·cm-3(列出计算式即可)。
 CH3CH=CH2(g)+3H2O(g)、nCO+(2n+1)H2
CH3CH=CH2(g)+3H2O(g)、nCO+(2n+1)H2 CnH2n+2+nH2O,为煤的气化、液化使用开拓了新途径。
CnH2n+2+nH2O,为煤的气化、液化使用开拓了新途径。(1)Fe3+中能量最高的能级上的电子云有
(2)Fe、C、O三种元素的第一电离能由大到小的顺序为
A. 2个σ键、1个π键 B. 1个σ键、2个π键 C. 非极性键
(3)新戊烷[(CH3)4C]分子中5个碳原子形成的空间构型是
(4)碳铁之间可形成多种化合物,其中一种化合物的晶体结构(面心立方结构)如图所示:

则编号为①的原子的坐标为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)Fe、Co、Ni是三种重要的金属元素。Fe、Co、Ni都能与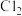 反应,其中Co和Ni均生成二氯化物,由此推断
反应,其中Co和Ni均生成二氯化物,由此推断 、
、 和
和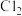 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。一种钴氧化物晶胞如图所示,该氧化物中钴离子价电子排布式为_______ 。设阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______ g﹒cm-3。

(2)以钴矿[主要成分是CoO、 、
、 ,还含
,还含 及少量
及少量 、
、 、CuO及
、CuO及 等]为原料可制取钴的氧化物。利用钴矿制取钴的氧化物的主要步骤如下:
等]为原料可制取钴的氧化物。利用钴矿制取钴的氧化物的主要步骤如下:
①浸取:用盐酸和 溶液浸取钴矿,浸取液中含有
溶液浸取钴矿,浸取液中含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子。写出
等离子。写出 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
②除杂:向浸取液中先加入足量 氧化
氧化 ,再加入NaOH调节pH除去
,再加入NaOH调节pH除去 、
、 、
、 。有关沉淀数据如下表(“完全沉淀”时金属离子浓度
。有关沉淀数据如下表(“完全沉淀”时金属离子浓度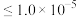 mol·L
mol·L ):
):
若浸取液中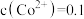 mol·L
mol·L ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是_______ (加入 和NaOH时,溶液的体积变化忽略)。
和NaOH时,溶液的体积变化忽略)。
③萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂 ,发生反应:
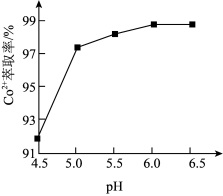
,发生反应: 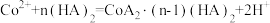 。实验测得:当溶液pH处于4.5~6.5范围内,
。实验测得:当溶液pH处于4.5~6.5范围内, 萃取率随溶液pH的增大而增大(如下图所示),其原因是
萃取率随溶液pH的增大而增大(如下图所示),其原因是_______ 。向萃取所得有机相中加入 ,反萃取得到水相。
,反萃取得到水相。
④沉钴、热分解:向反萃取后得到的水相中加入 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 晶体。称取14.64 g该晶体,在空气中加热一段时间后,得到CoO和
晶体。称取14.64 g该晶体,在空气中加热一段时间后,得到CoO和 的混合物。称量该混合物,质量为6.32 g,通过计算确定该混合物中CoO和
的混合物。称量该混合物,质量为6.32 g,通过计算确定该混合物中CoO和 的质量之比
的质量之比_______ (写出最简整数比)。
(1)Fe、Co、Ni是三种重要的金属元素。Fe、Co、Ni都能与
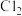 反应,其中Co和Ni均生成二氯化物,由此推断
反应,其中Co和Ni均生成二氯化物,由此推断 、
、 和
和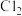 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为 ,则该晶体的密度为
,则该晶体的密度为
(2)以钴矿[主要成分是CoO、
 、
、 ,还含
,还含 及少量
及少量 、
、 、CuO及
、CuO及 等]为原料可制取钴的氧化物。利用钴矿制取钴的氧化物的主要步骤如下:
等]为原料可制取钴的氧化物。利用钴矿制取钴的氧化物的主要步骤如下:①浸取:用盐酸和
 溶液浸取钴矿,浸取液中含有
溶液浸取钴矿,浸取液中含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子。写出
等离子。写出 发生反应的离子方程式:
发生反应的离子方程式:②除杂:向浸取液中先加入足量
 氧化
氧化 ,再加入NaOH调节pH除去
,再加入NaOH调节pH除去 、
、 、
、 。有关沉淀数据如下表(“完全沉淀”时金属离子浓度
。有关沉淀数据如下表(“完全沉淀”时金属离子浓度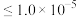 mol·L
mol·L ):
):| 沉淀 |  |  |  |  |  |
| 恰好完全沉淀时的pH | 5.2 | 2.8 | 9.4 | 6.7 | 10.1 |
若浸取液中
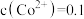 mol·L
mol·L ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是 和NaOH时,溶液的体积变化忽略)。
和NaOH时,溶液的体积变化忽略)。③萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂
 ,发生反应:
,发生反应: 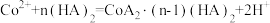 。实验测得:当溶液pH处于4.5~6.5范围内,
。实验测得:当溶液pH处于4.5~6.5范围内, 萃取率随溶液pH的增大而增大(如下图所示),其原因是
萃取率随溶液pH的增大而增大(如下图所示),其原因是 ,反萃取得到水相。
,反萃取得到水相。
④沉钴、热分解:向反萃取后得到的水相中加入
 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 晶体。称取14.64 g该晶体,在空气中加热一段时间后,得到CoO和
晶体。称取14.64 g该晶体,在空气中加热一段时间后,得到CoO和 的混合物。称量该混合物,质量为6.32 g,通过计算确定该混合物中CoO和
的混合物。称量该混合物,质量为6.32 g,通过计算确定该混合物中CoO和 的质量之比
的质量之比
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】利用铜萃取剂M,通过如下反应实现铜离子的富集:
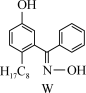
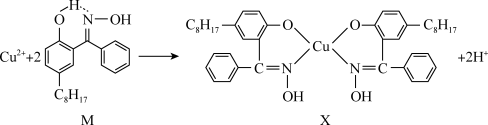
(1)关于M所含元素的说法正确的是______________ 。
A.电负性由大到小顺序:O>N>C>H
B.第一电离能由大到小的顺序:O>N>C
C.氮原子以sp2杂化轨道与氧原子形成σ键
D.从物质分类角度M属于芳香烃,M中所有的碳原子不可能共面
E.组成M元素的氢化物稳定性:CH4<H2O<NH3
(2)上述反应中断裂和生成的化学键有_______ (填序号)。
A.氢键 B.配位键 C.金属键 D.范德华力 E.共价键 F.离子键
(3)M与W(分子结构如上图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是_______________ 。
(4)基态Cu2+的外围电子排布图为________________ ,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是_____________________________________________________________ 。
(5)已知:Y原子最高价氧化物对应水化物的酸性最强。铜与Y形成化合物的晶胞如附图所示(黑点代表铜原子,空心圆代表Y原子)。
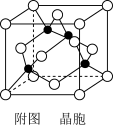
①该晶体的化学式为_______________ 。(用元素符号表示)
②已知铜和Y原子的电负性分别为1.9和3.0,则铜与Y原子形成的化合物属于____________ (填“离子”或“共价”)化合物。
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子与Y原子之间的最短距离为_______________ pm(只写计算式)。


(1)关于M所含元素的说法正确的是
A.电负性由大到小顺序:O>N>C>H
B.第一电离能由大到小的顺序:O>N>C
C.氮原子以sp2杂化轨道与氧原子形成σ键
D.从物质分类角度M属于芳香烃,M中所有的碳原子不可能共面
E.组成M元素的氢化物稳定性:CH4<H2O<NH3
(2)上述反应中断裂和生成的化学键有
A.氢键 B.配位键 C.金属键 D.范德华力 E.共价键 F.离子键
(3)M与W(分子结构如上图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是
(4)基态Cu2+的外围电子排布图为
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
(5)已知:Y原子最高价氧化物对应水化物的酸性最强。铜与Y形成化合物的晶胞如附图所示(黑点代表铜原子,空心圆代表Y原子)。

①该晶体的化学式为
②已知铜和Y原子的电负性分别为1.9和3.0,则铜与Y原子形成的化合物属于
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子与Y原子之间的最短距离为
您最近一年使用:0次



