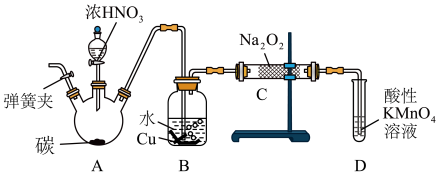
亚硝酸钠广泛用于印染、漂白等行业,在建筑行业用作防冻剂,在食品工业作防腐剂和增色剂,它是一种潜在致癌物质,过量或长期食用对人产生危害,由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生被当食盐误食的事件。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置,利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)
查阅资料:
①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②NO 能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO
能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO 还原为Mn2+且无气体生成。
还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
④HNO2在酸性溶液也是一种氧化剂,如能把I-氧化成I2。
⑤AgNO2是一种难溶于水易溶于酸的白色化合物。
(1)写出C中制备亚硝酸钠反应的化学方程式(反应物的物质的量之比为2:1)___________ 。
(2)D装置的作用是___________ 。
(3)经检验C产物中亚硝酸钠含量较少。甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。为排除干扰甲同学在B、C装置间增加装置E,E中盛放的试剂应是___________ (写名称)。
(4)人体正常的血红蛋白中含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________。
(5)能用来鉴别NaNO2和NaCl的方法是___________
A. 测溶液pH法
B.加酸法
C.AgNO3和HNO3两种试剂法
D.加KI淀粉(酸性)法
E.以上四种方法都可
(6)某同学把溴水加到NaNO2溶液观察到溴水褪色,请写出此反应的离子方程式___________ 。

查阅资料:
①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②NO
 能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO
能被很多常见的强氧化剂氧化,如在酸性溶液中可将MnO 还原为Mn2+且无气体生成。
还原为Mn2+且无气体生成。③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
④HNO2在酸性溶液也是一种氧化剂,如能把I-氧化成I2。
⑤AgNO2是一种难溶于水易溶于酸的白色化合物。
(1)写出C中制备亚硝酸钠反应的化学方程式(反应物的物质的量之比为2:1)
(2)D装置的作用是
(3)经检验C产物中亚硝酸钠含量较少。甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。为排除干扰甲同学在B、C装置间增加装置E,E中盛放的试剂应是
(4)人体正常的血红蛋白中含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________。
| A.亚硝酸盐是还原剂 |
| B.维生素C是还原剂 |
| C.维生素C将Fe3+还原Fe2+ |
| D.亚硝酸盐被还原 |
A. 测溶液pH法
B.加酸法
C.AgNO3和HNO3两种试剂法
D.加KI淀粉(酸性)法
E.以上四种方法都可
(6)某同学把溴水加到NaNO2溶液观察到溴水褪色,请写出此反应的离子方程式
14-15高三上·江西吉安·期末 查看更多[2]
更新时间:2016-12-09 05:58:57
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某活动小组利用如图装置验证NO的还原性及探究工业生产硝酸的原理(装置气密性已检查完毕)。

Ⅰ.向广口瓶中通入NO并测定NO的体积。
①通入NO前,从滴定管向广口瓶中加入水;
②从导管a通入一定量的NO,并记录滴定管液面变化的示数为V L(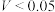 ,气体体积已换算为标准状况)。
,气体体积已换算为标准状况)。
Ⅱ.验证NO的还原性、探究工业生产硝酸的原理。
(1)停止通入NO后关闭 、
、 ,打开
,打开 ,从导管b缓缓通入
,从导管b缓缓通入 ,可观察到的现象是
,可观察到的现象是______ ,写出对应现象的化学方程式:_______ 、________ ;
(2)继续通入 ,打开
,打开 并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。
并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。
①当通入氧气的体积为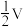 L时,广口瓶中剩余的是
L时,广口瓶中剩余的是______ 气体。
②当广口瓶中刚好充满液体时,所得溶液的物质的量浓度为______ mol⋅L 。
。

Ⅰ.向广口瓶中通入NO并测定NO的体积。
①通入NO前,从滴定管向广口瓶中加入水;
②从导管a通入一定量的NO,并记录滴定管液面变化的示数为V L(
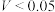 ,气体体积已换算为标准状况)。
,气体体积已换算为标准状况)。Ⅱ.验证NO的还原性、探究工业生产硝酸的原理。
(1)停止通入NO后关闭
 、
、 ,打开
,打开 ,从导管b缓缓通入
,从导管b缓缓通入 ,可观察到的现象是
,可观察到的现象是(2)继续通入
 ,打开
,打开 并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。
并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。①当通入氧气的体积为
 L时,广口瓶中剩余的是
L时,广口瓶中剩余的是②当广口瓶中刚好充满液体时,所得溶液的物质的量浓度为
 。
。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
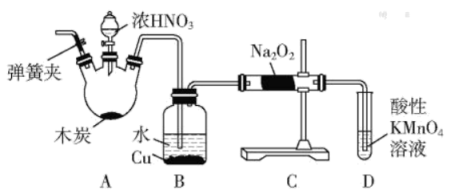
【推荐2】亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛。以木炭、浓硝酸、水和铜为原料制备亚硝酸钠的装置如图所示:
已知:室温下,①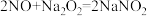 ;
;
② ;
;
③酸性条件下,NO或 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
请按要求回答下列问题:
(1)检查完该装置的气密性,装入药品后,实验开始前通入一段时间气体Ar,然后关闭弹簧夹,再滴加浓硝酸,加热控制B中导管均匀地产生气泡。上述操作的作用是___________ 。
(2)B中观察到的主要现象是___________ ;
(3)A装置中反应的化学方程式为___________ ;
(4)D装置中反应的离子方程式___________ ;
(5)预测C中反应开始阶段,固体产物除NaNO2外,还含有的副产物有Na2CO3和___________ 。为避免产生这些副产物,应在B、C装置间增加装置E,则E中盛放的试剂名称为___________ 。

已知:室温下,①
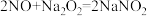 ;
;②
 ;
;③酸性条件下,NO或
 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。请按要求回答下列问题:
(1)检查完该装置的气密性,装入药品后,实验开始前通入一段时间气体Ar,然后关闭弹簧夹,再滴加浓硝酸,加热控制B中导管均匀地产生气泡。上述操作的作用是
(2)B中观察到的主要现象是
(3)A装置中反应的化学方程式为
(4)D装置中反应的离子方程式
(5)预测C中反应开始阶段,固体产物除NaNO2外,还含有的副产物有Na2CO3和
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图中A~G均为中学化学中常见的物质,它们之间有如下转化关系。常温下,A为紫红色金属固体,B为常见的强酸,G为地壳中含量最多元素组成的气态单质;D、F都是大气污染物,主要来源于汽车尾气,D为无色气体,F为红棕色气体。
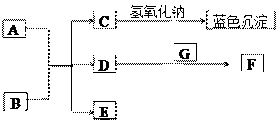
请回答以下问题:
①D的化学式是________ ;C+NaOH生成的蓝色沉淀是_____________ (填化学式);
②构成G单质的元素在元素周期表中的位置为_________________ ;
③写出B的稀溶液与A反应的化学方程式:_______________________________ 。
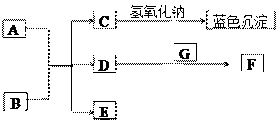
请回答以下问题:
①D的化学式是
②构成G单质的元素在元素周期表中的位置为
③写出B的稀溶液与A反应的化学方程式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氨基甲酸铵是一种重要化工产品,常温时,为白色晶体或粉末,易溶于水,难溶于CCl4,59℃时分解为氨及二氧化碳,其制备原理:2NH3(g)+CO2(g) NH2COONH4 (s) △H=-272kJ·mol-1。某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4。试回答下列问题:
NH2COONH4 (s) △H=-272kJ·mol-1。某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4。试回答下列问题:
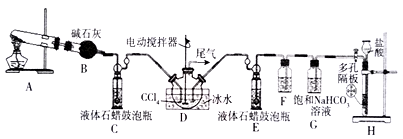
(1)仪器组装完毕后,首先应进行的操作是_____________________________ 。
(2)装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为_____________ 。
(3)装置F中试剂的名称为_________ ,装置G的作用为________________ 。
(4)为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为____________ ,装置D采用冰水浴的原因为_____________________________________________________ 。
(5)生成的氨基甲酸铵悬浮于CCl4 中,下列操作可实现产品分离的是_________ 。




(6)实验装置中存在明显不足之处的是______________ ,有同学认为装置H、G和F组成的装置过于复杂可简化,请简述该方法:__________________________ 。
 NH2COONH4 (s) △H=-272kJ·mol-1。某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4。试回答下列问题:
NH2COONH4 (s) △H=-272kJ·mol-1。某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4。试回答下列问题:
(1)仪器组装完毕后,首先应进行的操作是
(2)装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为
(3)装置F中试剂的名称为
(4)为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为
(5)生成的氨基甲酸铵悬浮于CCl4 中,下列操作可实现产品分离的是




(6)实验装置中存在明显不足之处的是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】四氯化锡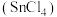 是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
I.【查阅资料】
Ⅱ 【制备产品】
【制备产品】
实验装置如图所示 省略夹持和加热装置
省略夹持和加热装置

实验步骤:
(1)检查装置气密性后,按图示加入试剂.仪器b的名称是______ ,其中无水 的作用是
的作用是 ______ ,B中的试剂是 ______  选填下列字母编号
选填下列字母编号 。
。
A. 溶液
溶液  溶液
溶液
 饱和NaCl溶液
饱和NaCl溶液  溶液
溶液
(2)先向A中烧瓶内加入盐酸并加热a,当整个装置______ 后 填实验现象
填实验现象 ,再加热熔化锡粒,反应完后,停止加热。
,再加热熔化锡粒,反应完后,停止加热。
(3)待反应结束后,经______  填写操作名称
填写操作名称 、洗涤、干燥,可回收利用装置A中未反应完的
、洗涤、干燥,可回收利用装置A中未反应完的 。
。
Ⅲ 探究与反思
探究与反思
(1)装置F中吸收 发生反应的离子方程式是
发生反应的离子方程式是 ______ 。
(2)实验在D中得到的产品很少,经分析装置设计有缺陷,应在D和E之间补充______  填装置名称
填装置名称 。
。
(3)为验证产品中是否含有 ,该小组设计了以下实验方案:
,该小组设计了以下实验方案: 所需试剂从稀
所需试剂从稀 、稀HCl、
、稀HCl、 溶液、
溶液、 溶液、KSCN溶液、蒸馏水中选择
溶液、KSCN溶液、蒸馏水中选择
取适量 产品溶入20mL蒸馏水中,加入
产品溶入20mL蒸馏水中,加入 ______ ,若 ______  填实验现象
填实验现象 ,则含有
,则含有 ,否则无
,否则无 。
。
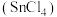 是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
是一种重要的化工产品。某兴趣小组拟制备四氯化锡。I.【查阅资料】
| 物质 | 熔点 | 沸点 | 化学性质 |
| Sn | 231 | 227 | 加热时与 反应生成 反应生成 |
 | 246 | 652 |  易被 易被 、 、 等氧化 等氧化 |
 |  | 114 | 极易水解 |
Ⅱ
 【制备产品】
【制备产品】实验装置如图所示
 省略夹持和加热装置
省略夹持和加热装置

实验步骤:
(1)检查装置气密性后,按图示加入试剂.仪器b的名称是
 的作用是
的作用是  选填下列字母编号
选填下列字母编号 。
。A.
 溶液
溶液  溶液
溶液  饱和NaCl溶液
饱和NaCl溶液  溶液
溶液(2)先向A中烧瓶内加入盐酸并加热a,当整个装置
 填实验现象
填实验现象 ,再加热熔化锡粒,反应完后,停止加热。
,再加热熔化锡粒,反应完后,停止加热。(3)待反应结束后,经
 填写操作名称
填写操作名称 、洗涤、干燥,可回收利用装置A中未反应完的
、洗涤、干燥,可回收利用装置A中未反应完的 。
。Ⅲ
 探究与反思
探究与反思
(1)装置F中吸收
 发生反应的离子方程式是
发生反应的离子方程式是 (2)实验在D中得到的产品很少,经分析装置设计有缺陷,应在D和E之间补充
 填装置名称
填装置名称 。
。(3)为验证产品中是否含有
 ,该小组设计了以下实验方案:
,该小组设计了以下实验方案: 所需试剂从稀
所需试剂从稀 、稀HCl、
、稀HCl、 溶液、
溶液、 溶液、KSCN溶液、蒸馏水中选择
溶液、KSCN溶液、蒸馏水中选择
取适量
 产品溶入20mL蒸馏水中,加入
产品溶入20mL蒸馏水中,加入  填实验现象
填实验现象 ,则含有
,则含有 ,否则无
,否则无 。
。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室中根据 已知
已知 熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备
熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备 固体。
固体。

(1)实验开始时,先点燃的酒精灯是_________ (填编号)。
(2)装置D中浓硫酸的作用除了混合气体并观察气体流速外还有___________ 。
(3)装置F的作用是____________________ 。
(4)由于可逆反应,所以从E管出来的气体中含有 、
、 。为了证明含有
。为了证明含有 可以将该气体通入
可以将该气体通入________ (填下列编号,下同)、证明含有 可以将该气体通入
可以将该气体通入_____________ 。
A.品红 B.溴水 C. 溶液 D.
溶液 D. 溶液
溶液
(5)如果没有装置G,则F中可能看到_________________ 。
(6)从装置G导出的尾气常可以用烧碱或石灰乳吸收。请写出用足量烧碱吸收尾气的离子方程式为:_________________________________________________________ 。
(7)尾气常采用烧碱或石灰乳吸收,请分析比较两种吸收剂吸收的优点__________________________________________________________ 。
 已知
已知 熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备
熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备 固体。
固体。
(1)实验开始时,先点燃的酒精灯是
(2)装置D中浓硫酸的作用除了混合气体并观察气体流速外还有
(3)装置F的作用是
(4)由于可逆反应,所以从E管出来的气体中含有
 、
、 。为了证明含有
。为了证明含有 可以将该气体通入
可以将该气体通入 可以将该气体通入
可以将该气体通入A.品红 B.溴水 C.
 溶液 D.
溶液 D. 溶液
溶液(5)如果没有装置G,则F中可能看到
(6)从装置G导出的尾气常可以用烧碱或石灰乳吸收。请写出用足量烧碱吸收尾气的离子方程式为:
(7)尾气常采用烧碱或石灰乳吸收,请分析比较两种吸收剂吸收的优点
您最近半年使用:0次



