处理废旧电池[主要含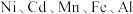 、铼
、铼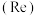 ]的流程如下:
]的流程如下:
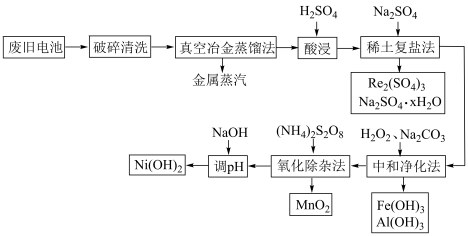
下列说法正确的是
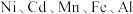 、铼
、铼 ]的流程如下:
]的流程如下:
下列说法正确的是
A.金属 的沸点高于其他金属 的沸点高于其他金属 |
B.生成复盐的离子方程式为 |
C.在实际中和净化过程中,需要的 与 与 的物质的量之比应为 的物质的量之比应为 |
D. 中, 中, 为 为 价,其中含有2个过氧键 价,其中含有2个过氧键 |
更新时间:2023-12-09 22:20:29
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作、现象和结论不正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁均有水珠 | 两种物质均受热分解 |
| B | 向硅酸钠溶液中通入CO2 | 生成白色沉淀 | 酸性:碳酸强于硅酸 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式正确的是
A.FeI2溶液中加入少量酸性高锰酸钾溶液:5Fe2++MnO +8H+=Mn2++5Fe3++4H2O +8H+=Mn2++5Fe3++4H2O |
B.硫酸铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO +4NH +4NH +2H2O +2H2O |
| C.将Fe3O4溶解于足量稀HNO3中:Fe3O4+8H+=Fe2++2Fe3++4H2O |
D.过量铁粉与一定量的稀硝酸反应:3Fe+8H++2NO =3Fe2++2NO↑+4H2O =3Fe2++2NO↑+4H2O |
您最近一年使用:0次
【推荐1】下表是五种银盐的溶度积常数(25℃),下列有关说法错误的是
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 5.0×10-13 | 8.3×10-17 |
| A.五种物质在常温下溶解度最大的是Ag2SO4 |
| B.向AgCl的悬浊液中加入0.1mol/LNa2S溶液,则可以生成黑色的Ag2S沉淀 |
| C.外界条件改变时,沉淀溶解平衡也会发生移动 |
| D.常温下,向AgI的悬浊液中加入0.1mol/LNaCl溶液,黄色沉淀变成白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s) Ca(OH)2(aq)
Ca(OH)2(aq) Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是
Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是
 Ca(OH)2(aq)
Ca(OH)2(aq) Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是
Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是| A.n(Ca2+)增大 | B.c(Ca2+)不变 | C.n(OH-)增大 | D.c(OH-)减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】实验室制备氯气:MnO2+4HCl(浓) MnCl2+ Cl2↑+2 H2O反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学设计了4组实验方案(每次均量取20 mL反应残余液进行实验),其中正确的是
MnCl2+ Cl2↑+2 H2O反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学设计了4组实验方案(每次均量取20 mL反应残余液进行实验),其中正确的是
 MnCl2+ Cl2↑+2 H2O反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学设计了4组实验方案(每次均量取20 mL反应残余液进行实验),其中正确的是
MnCl2+ Cl2↑+2 H2O反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学设计了4组实验方案(每次均量取20 mL反应残余液进行实验),其中正确的是| A.与足量AgNO3溶液反应,过滤、洗涤、干燥,称量生成的沉淀质量为a g |
| B.稀释10倍后取20 mL用已知浓度的NaOH溶液滴定,消耗NaOH的体积为b mL |
| C.与足量NaHCO3固体反应,逸出气体用足量碱石灰吸收,增重c g |
| D.加入d1g CaCO3(过量)充分反应后,称量剩余固体质量为d2 g[已知:Ksp( CaCO3)>Ksp(MnCO3)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐1】一定条件下,酸性 溶液与
溶液与 发生反应,
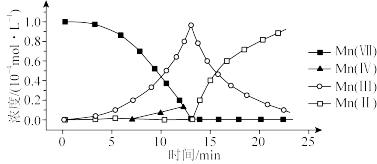
发生反应, (Ⅱ)起催化作用,过程中不同价态含
(Ⅱ)起催化作用,过程中不同价态含 粒子的浓度随时间变化如下图所示。下列说法正确的是
粒子的浓度随时间变化如下图所示。下列说法正确的是
 溶液与
溶液与 发生反应,
发生反应, (Ⅱ)起催化作用,过程中不同价态含
(Ⅱ)起催化作用,过程中不同价态含 粒子的浓度随时间变化如下图所示。下列说法正确的是
粒子的浓度随时间变化如下图所示。下列说法正确的是
A. (Ⅲ)不能氧化 (Ⅲ)不能氧化 |
| B.随着反应物浓度的减小,反应速率逐渐减小 |
C.该条件下, (Ⅱ)和 (Ⅱ)和 (Ⅶ)不能大量共存 (Ⅶ)不能大量共存 |
D.总反应为: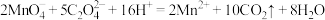 |
您最近一年使用:0次
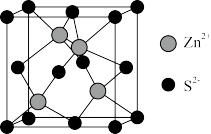
【推荐2】纳米ZnS具有独特的光电效应。以工业废渣锌灰(主要成分为Zn、ZnO,还含有 、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
 、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下: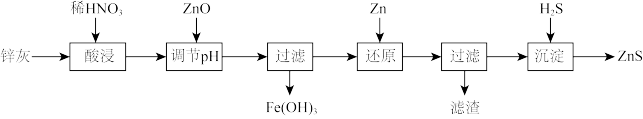
A.“酸浸”时FeO反应的离子方程式为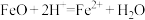 |
B.“还原”的目的是将 转化为 转化为 |
C.“沉淀”的离子方程式为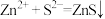 |
D.ZnS晶胞(如图所示)中每个 周围距离最近的 周围距离最近的 有4个 有4个 |
您最近一年使用:0次

 、
、 、
、
 、
、 、
、 、
、 、
、 、
、 的溶液加入:
的溶液加入: 、
、 、
、
 在空气中燃烧主要生成
在空气中燃烧主要生成
 可与硫酸铜溶液反应得到铜
可与硫酸铜溶液反应得到铜

