填空
(1)已知顺-2-丁烯与反-2-丁烯之间的转化称为“异构化”,两种物质与氢气加成的热化学方程式如下,则顺-2-丁烯异化为反-2-丁烯的热化学方程式为__________________ .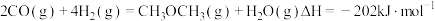 。下表是几种化学键的键能,则
。下表是几种化学键的键能,则 的键能为
的键能为_________  。
。
(3)由 和
和 构成的质子交换膜燃料电池的结构示意如下图所示,电池总反应为
构成的质子交换膜燃料电池的结构示意如下图所示,电池总反应为 ,请回答下列问题。
,请回答下列问题。
① 电极的电极反应式为
电极的电极反应式为__________________ .
②若用该燃料电池为铅蓄电池充电,电极 连接铅蓄电池的
连接铅蓄电池的_________ 极(填“ ”或“
”或“ ”),通过质子交换膜
”),通过质子交换膜 时,上述燃料电池所消耗的
时,上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为_________  ,铅蓄电池中电解液质量
,铅蓄电池中电解液质量_________ (填“增大”或“减小”)_________ g。
(1)已知顺-2-丁烯与反-2-丁烯之间的转化称为“异构化”,两种物质与氢气加成的热化学方程式如下,则顺-2-丁烯异化为反-2-丁烯的热化学方程式为
①
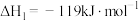
②
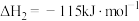
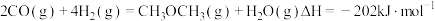 。下表是几种化学键的键能,则
。下表是几种化学键的键能,则 的键能为
的键能为 。
。化学键 |
|
|
|
|
键能 | 413 | 326 | 436 | 1072 |
(3)由
 和
和 构成的质子交换膜燃料电池的结构示意如下图所示,电池总反应为
构成的质子交换膜燃料电池的结构示意如下图所示,电池总反应为 ,请回答下列问题。
,请回答下列问题。①
 电极的电极反应式为
电极的电极反应式为②若用该燃料电池为铅蓄电池充电,电极
 连接铅蓄电池的
连接铅蓄电池的 ”或“
”或“ ”),通过质子交换膜
”),通过质子交换膜 时,上述燃料电池所消耗的
时,上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为 ,铅蓄电池中电解液质量
,铅蓄电池中电解液质量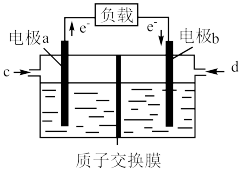
2023·山东德州·模拟预测 查看更多[2]
山东省德州市第一中学、第二中学2024届高三上学期适应性联考模拟预测化学试题(已下线)专题14 化学反应原理综合题-【好题汇编】5年(2020-2024)高考1年模拟化学真题分类汇编(山东专用)
更新时间:2023/12/03 14:31:01
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A: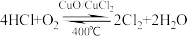
已知:i. 反应A中,4mol HCl被氧化,放出115.6kJ的热量。
ii.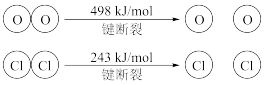
①HCl的电子式是__________ 。
②反应A的热化学方程式是____________ 。
③断开1mol H-O键与断开1mol H-Cl键所需能量相差约______ kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)_____ 。
(2)下图是容积均为1L,分别按4种投料比[n(HCl):n(O2)]分别为1:1、2:1、4:1、6:1进行投料,反应温度对HCl平衡转化率影响的曲线。
①曲线c对应的投料比是__________ 。
②用平衡移动的原理解释温度和HCl平衡转化率的关系__________ 。
③投料比为4:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是_____ ,O2的平衡转化率______ 。
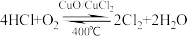
已知:i. 反应A中,4mol HCl被氧化,放出115.6kJ的热量。
ii.
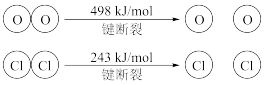
①HCl的电子式是
②反应A的热化学方程式是
③断开1mol H-O键与断开1mol H-Cl键所需能量相差约
(2)下图是容积均为1L,分别按4种投料比[n(HCl):n(O2)]分别为1:1、2:1、4:1、6:1进行投料,反应温度对HCl平衡转化率影响的曲线。
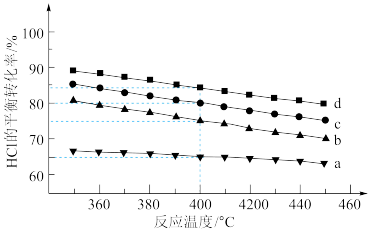
①曲线c对应的投料比是
②用平衡移动的原理解释温度和HCl平衡转化率的关系
③投料比为4:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】三氯甲硅烷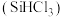 是生产多晶硅的原料,工业合成
是生产多晶硅的原料,工业合成 体系中同时存在如下反应:
体系中同时存在如下反应:
反应I:
反应Ⅱ:
反应Ⅲ: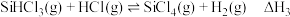
部分化学键的键能数据如表所示:
回答下列问题:
(1)
_______  。
。
(2)压强与进料比 都会影响
都会影响 的产率-
的产率- 。图甲为
。图甲为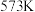 及不同压强下
及不同压强下 随
随 的变化情况,由图甲可知最合适的进料比为
的变化情况,由图甲可知最合适的进料比为_______ ;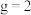 ,上述反应达到平衡时在
,上述反应达到平衡时在_______ (填 或
或 )压强下
)压强下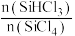 最大;
最大;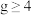 时,
时, 接近于零的原因是
接近于零的原因是_______ 。 的恒容密闭容器中加入一定量的
的恒容密闭容器中加入一定量的 和
和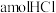 ,发生上述反应,达到平衡时,容器中
,发生上述反应,达到平衡时,容器中 为
为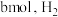 为
为 ,此时
,此时 的浓度为
的浓度为_______  (用含
(用含 的代数式表示,下同),反应Ⅲ的平衡常数为
的代数式表示,下同),反应Ⅲ的平衡常数为_______ 。
(4)忽略副反应,反应I在不同催化剂作用下反应相同时间、 的转化率随温度的变化如图乙,下列说法正确的是_______(填序号)。
的转化率随温度的变化如图乙,下列说法正确的是_______(填序号)。
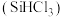 是生产多晶硅的原料,工业合成
是生产多晶硅的原料,工业合成 体系中同时存在如下反应:
体系中同时存在如下反应:反应I:

反应Ⅱ:

反应Ⅲ:
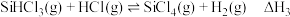
部分化学键的键能数据如表所示:
| 化学键 |  |  |  |  |
键能 | 318 | 431 | 360 | 436 |
(1)

 。
。(2)压强与进料比
 都会影响
都会影响 的产率-
的产率- 。图甲为
。图甲为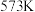 及不同压强下
及不同压强下 随
随 的变化情况,由图甲可知最合适的进料比为
的变化情况,由图甲可知最合适的进料比为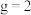 ,上述反应达到平衡时在
,上述反应达到平衡时在 或
或 )压强下
)压强下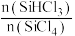 最大;
最大;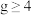 时,
时, 接近于零的原因是
接近于零的原因是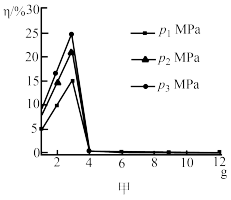
 的恒容密闭容器中加入一定量的
的恒容密闭容器中加入一定量的 和
和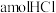 ,发生上述反应,达到平衡时,容器中
,发生上述反应,达到平衡时,容器中 为
为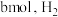 为
为 ,此时
,此时 的浓度为
的浓度为 (用含
(用含 的代数式表示,下同),反应Ⅲ的平衡常数为
的代数式表示,下同),反应Ⅲ的平衡常数为(4)忽略副反应,反应I在不同催化剂作用下反应相同时间、
 的转化率随温度的变化如图乙,下列说法正确的是_______(填序号)。
的转化率随温度的变化如图乙,下列说法正确的是_______(填序号)。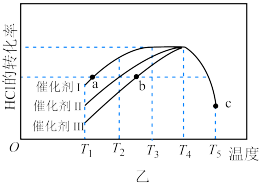
A.催化剂I效果最佳,对应 的平衡转化率最大 的平衡转化率最大 |
B.b点 ,可以适当延长反应时间提高 ,可以适当延长反应时间提高 的转化率 的转化率 |
C.c点 转化率降低可能是因为温度过高,催化剂失去活性 转化率降低可能是因为温度过高,催化剂失去活性 |
D.平衡常数: |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】生活中离不开化学运用化学知识回答下列问题。
(1) 在食品加工中是种合法的食品添加剂,它还是一种净水剂,其净水的原理为
在食品加工中是种合法的食品添加剂,它还是一种净水剂,其净水的原理为___________ (填离子方程式)。
(2)龋齿是有机酸使牙齿中的 溶解造成的。使用含氟牙膏会使其转化为
溶解造成的。使用含氟牙膏会使其转化为 抵抗酸的腐蚀,含氟牙膏能使牙齿中
抵抗酸的腐蚀,含氟牙膏能使牙齿中 转化为
转化为 的理由是:溶解度
的理由是:溶解度
___________ 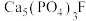 (填“>"或“<”)。
(填“>"或“<”)。
(3)某温度下,纯水中的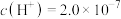 mol·L
mol·L ,则该温度时水的离子积
,则该温度时水的离子积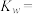
___________ 。保持温度不变,滴入稀盐酸使溶液中的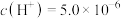 mol·L
mol·L ,则溶液中的
,则溶液中的
___________ mol·L 。
。
(4)氨气中氢含量高,是一种优良的小分子储氢载体,且安全易储运。相关化学键的键能数据如下:
则 ,
,
___________ kJ·mol 。
。
(1)
 在食品加工中是种合法的食品添加剂,它还是一种净水剂,其净水的原理为
在食品加工中是种合法的食品添加剂,它还是一种净水剂,其净水的原理为(2)龋齿是有机酸使牙齿中的
 溶解造成的。使用含氟牙膏会使其转化为
溶解造成的。使用含氟牙膏会使其转化为 抵抗酸的腐蚀,含氟牙膏能使牙齿中
抵抗酸的腐蚀,含氟牙膏能使牙齿中 转化为
转化为 的理由是:溶解度
的理由是:溶解度
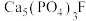 (填“>"或“<”)。
(填“>"或“<”)。(3)某温度下,纯水中的
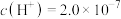 mol·L
mol·L ,则该温度时水的离子积
,则该温度时水的离子积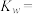
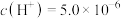 mol·L
mol·L ,则溶液中的
,则溶液中的
 。
。(4)氨气中氢含量高,是一种优良的小分子储氢载体,且安全易储运。相关化学键的键能数据如下:
| 化学键 |  |  |  |
键能E/(kJ·mol ) ) | 945.6 | 436.0 | 391.0 |
则
 ,
,
 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图是一个化学过程的示意图,回答下列问题:
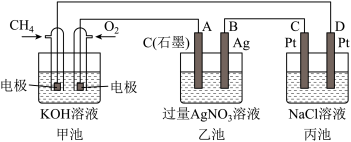
(1)乙装置中电极A的名称是___ 。
(2)甲装置中通入CH4的电极反应式为___ ,乙装置中电极B(Ag)的电极反应式为___ ,丙装置中D极的产物是___ (写化学式)。
(3)一段时间,当丙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=___ (已知:NaCl溶液足量,电解后溶液体积为500mL)。若要使丙池恢复电解前的状态,应向丙池中加入___ (写名称)。

(1)乙装置中电极A的名称是
(2)甲装置中通入CH4的电极反应式为
(3)一段时间,当丙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F、G均为常见的有机物,它们之间有如下转化关系。已知:①A是一种植物生长调节剂,有催熟作用;②醛基在氧气中易被氧化成羧基。回答下列问题:

(1)A和B中官能团名称分别是_________ 和_______________ 。
(2)在F的众多同系物中:最简单的同系物其空间构型为____________ ;含5个碳原子的同系物其同分异构体有_______ 种,其中一氯代物种类最少的同系物的结构简式为_________ 。
(3)反应⑥和⑦均可得到G,要制备得到较纯净的G,应该选用反应_____ 。
(4)反应①﹣⑦属取代反应的有______ ;反应②的化学方程式为___________________ 。
(5)以B物质和空气、KOH溶液可以构成燃料电池,该电池的正极反应式为_____________ 电池总反应方程式为___________________________________________________
(6)某同学欲用下图装置制备物质E,将试管B中的物质E分离出来,用到的主要玻璃仪器有:烧杯、________ ,插入试管B的导管接有一个球状物,其作用为____________ 。


(1)A和B中官能团名称分别是
(2)在F的众多同系物中:最简单的同系物其空间构型为
(3)反应⑥和⑦均可得到G,要制备得到较纯净的G,应该选用反应
(4)反应①﹣⑦属取代反应的有
(5)以B物质和空气、KOH溶液可以构成燃料电池,该电池的正极反应式为
(6)某同学欲用下图装置制备物质E,将试管B中的物质E分离出来,用到的主要玻璃仪器有:烧杯、

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=_______ mol·L-1.(已知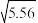 ≈2.36)。
≈2.36)。
(2)磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13。
①Na2HPO4的水溶液呈_______ (填“酸”“碱”或“中”)性。
②下列说法正确的是_______
A.磷酸溶液中存在3个平衡
B.向pH=2的磷酸溶液中加入NaH2PO4固体,溶液酸性降低
C.向Na2HPO4溶液中滴加稀盐酸的过程中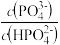 的值增大
的值增大
D.向NaH2PO4溶液中滴加NaOH至过量,水的电离程度先增大后减小
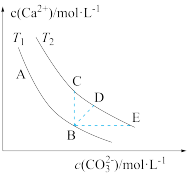
(3)不同温度下(T1、T2),CaCO3在水中的沉淀溶解平衡曲线如图所示,回答下列问题(注:CaCO3均未完全溶解)T1_______ (填“>”“<”或“=”)T2;在B点,若温度从T1到T2,则B点变到_______ 点(填“C”“D”或“E”。)
(4)某氢氧燃料电池以熔融态的碳酸盐为电解质,其中 参与电极反应。工作时负极的电极反应为
参与电极反应。工作时负极的电极反应为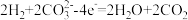 。正极的电极反应为
。正极的电极反应为_______ 。
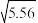 ≈2.36)。
≈2.36)。(2)磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13。
①Na2HPO4的水溶液呈
②下列说法正确的是
A.磷酸溶液中存在3个平衡
B.向pH=2的磷酸溶液中加入NaH2PO4固体,溶液酸性降低
C.向Na2HPO4溶液中滴加稀盐酸的过程中
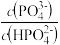 的值增大
的值增大 D.向NaH2PO4溶液中滴加NaOH至过量,水的电离程度先增大后减小
(3)不同温度下(T1、T2),CaCO3在水中的沉淀溶解平衡曲线如图所示,回答下列问题(注:CaCO3均未完全溶解)T1

(4)某氢氧燃料电池以熔融态的碳酸盐为电解质,其中
 参与电极反应。工作时负极的电极反应为
参与电极反应。工作时负极的电极反应为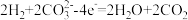 。正极的电极反应为
。正极的电极反应为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
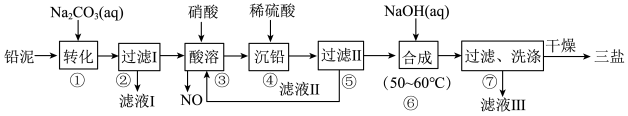
【推荐1】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4·H2O(三盐),主要制备流程如下。
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为___________ 。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为___________ 。
(2)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为___________ 。
(3)步骤⑥合成三盐的化学方程式为___________ 。
(4)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是___________ 。
(5)已知:常温下,Ksp(PbSO4)≈2.0×10−8,Ksp(PbCO3)≈1.0×10−13。在步骤①转化中,若硫酸铅和碳酸铅在浊液中共存,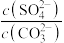 =
=___________ 。
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4
 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为(2)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为
(3)步骤⑥合成三盐的化学方程式为
(4)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是
(5)已知:常温下,Ksp(PbSO4)≈2.0×10−8,Ksp(PbCO3)≈1.0×10−13。在步骤①转化中,若硫酸铅和碳酸铅在浊液中共存,
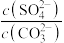 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】研究无机非金属及其相关化合物在化工生产中有重要意义。
(1)氨的催化氧化是制备硝酸的重要反应,实验中先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是___________ (填标号)。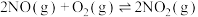 ,通入等物质的量的
,通入等物质的量的 和
和 气体,
气体, 随时间的变化如下表:
随时间的变化如下表:
①0~2s内,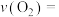
___________ 。
②下列描述能说明该反应已达到化学反应平衡状态的有___________ (填标号)
A.单位时间里,生成2mol ,消耗1mol
,消耗1mol B.
B.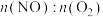 的值不再变化
的值不再变化
C.混合气体密度不再变化 D.混合气体平均摩尔质量不再变化
E.温度不再变化 F. 、
、 、
、 同时存在
同时存在
③在第5s时, 的转化率为
的转化率为___________ 。
④平衡时,容器中混合气体的压强与反应开始时的压强之比为___________ 。
(3)汽车中的电瓶为铅酸蓄电池。铅酸蓄电池的工作原理如图所示,总反应式为: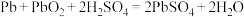 。回答下列问题:
。回答下列问题: 移向电池
移向电池___________ 极(填“正”或“负”)
②若构建该电池时,两个电极的质量相等,则当导线中通过0.2mol电子时,理论上两个电极的质量差为___________ g。
(1)氨的催化氧化是制备硝酸的重要反应,实验中先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是
A. B.
B.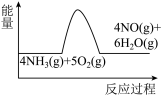 C.
C.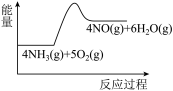
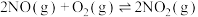 ,通入等物质的量的
,通入等物质的量的 和
和 气体,
气体, 随时间的变化如下表:
随时间的变化如下表: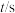 | 0 | 1 | 2 | 3 | 4 | 5 |
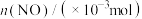 | 2.0 | 1.2 | 0.8 | 0.5 | 0.4 | 0.4 |
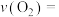
②下列描述能说明该反应已达到化学反应平衡状态的有
A.单位时间里,生成2mol
 ,消耗1mol
,消耗1mol B.
B.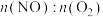 的值不再变化
的值不再变化C.混合气体密度不再变化 D.混合气体平均摩尔质量不再变化
E.温度不再变化 F.
 、
、 、
、 同时存在
同时存在③在第5s时,
 的转化率为
的转化率为④平衡时,容器中混合气体的压强与反应开始时的压强之比为
(3)汽车中的电瓶为铅酸蓄电池。铅酸蓄电池的工作原理如图所示,总反应式为:
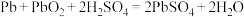 。回答下列问题:
。回答下列问题: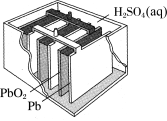
 移向电池
移向电池②若构建该电池时,两个电极的质量相等,则当导线中通过0.2mol电子时,理论上两个电极的质量差为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.如图为原电池装置示意图。__________ 。该电池在工作时,A电极的质量将_______ (填“增加”“减小”或“不变”),若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为________ 。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:_____________________________ 。该电池在工作一段时间后,溶液的碱性将________ (填“增强”“减弱”或“不变”)。
Ⅱ.现用图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。________ ,其电极反应式为_________________________ 。
(4)当量筒中收集到560 mL(标准状况下)气体时,通过导线的电子的物质的量为________ mol,此时a电极质量________ (填“增加”或“减少”)________ g。
(5)如果将a、b两电极的电极材料对调,U形管中将出现的现象是_____________ 。
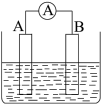
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:
Ⅱ.现用图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。
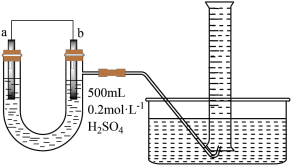
(4)当量筒中收集到560 mL(标准状况下)气体时,通过导线的电子的物质的量为
(5)如果将a、b两电极的电极材料对调,U形管中将出现的现象是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】用如图所示的装置进行电解。通电一段时间后,发现湿润的淀粉-KI试纸的C端变为蓝色。
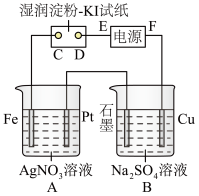
①E为电源的_________ 极,Fe为A池的_________ 极。
②A装置中发生反应的化学方程式为____________________________________ 。
③在B装置中观察到的现象是_____________________________________________ 。
④D端的电极反应式为_____________________________________________ 。

①E为电源的
②A装置中发生反应的化学方程式为
③在B装置中观察到的现象是
④D端的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
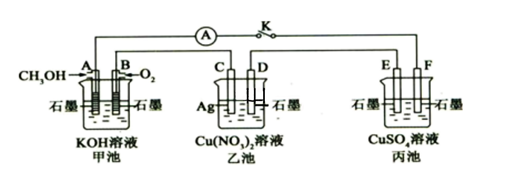
请回答下列问题:
(1)甲池为________ (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为____ 。
(2)丙池中F电极为__________ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为__________________ 。
(3)当乙池中C极质量减轻4.32g时,甲池中B电极理论上消耗O2的体积为_____ ml(标准状况)。若丙池中两端的电极不变,将其溶液换成NaCl溶液,则开关闭合一段时间后,丙池中溶液的的体积为400ml计算溶液PH____
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是________ (填选项字母)。

请回答下列问题:
(1)甲池为
(2)丙池中F电极为
(3)当乙池中C极质量减轻4.32g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】如图,C、D、E、F、X、Y都是惰性电极,A、B为电源。将电源接通后,D电极上有无色气体放出。
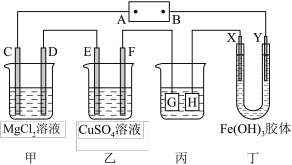
(1)A为电源_______ 极。
(2)丙装置欲在铁钉上镀铜,则G电极上的反应式为_____________________________ 。
(3)通电一段时间后,甲中出现浑浊,甲中发生反应的化学方程式为:_________________ 。
(4)工作一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这说明Fe(OH)3胶粒带________ 电,在电场作用下向Y极移动。
(5)若工作一段时间后停止通电,此时,乙中E、F两极上都产生2.24L气体(标准状况),E极气体为___________ (填化学式),欲使溶液恢复到起始状态,可向溶液中加入____________ (填序号)。
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3

(1)A为电源
(2)丙装置欲在铁钉上镀铜,则G电极上的反应式为
(3)通电一段时间后,甲中出现浑浊,甲中发生反应的化学方程式为:
(4)工作一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这说明Fe(OH)3胶粒带
(5)若工作一段时间后停止通电,此时,乙中E、F两极上都产生2.24L气体(标准状况),E极气体为
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3
您最近一年使用:0次







