I.对于反应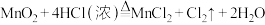 。
。
(1) 在反应中
在反应中___________ 电子,发生___________ 反应。
(2) 在反应中
在反应中___________ 电子,发生___________ 反应。
(3)用单线桥法标出该反应中电子转移的方向和数目:___________ 。
II. 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: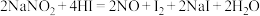 。
。
(4)反应中___________ 发生氧化反应(填化学式),___________ 是氧化剂(填化学式);
(5)用双线桥标出电子转移方向和数目:___________ 。
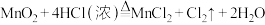 。
。(1)
 在反应中
在反应中(2)
 在反应中
在反应中(3)用单线桥法标出该反应中电子转移的方向和数目:
II.
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: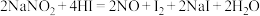 。
。(4)反应中
(5)用双线桥标出电子转移方向和数目:
更新时间:2023-12-05 11:29:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】交警检验司机是否酒驾时,通常使用酒精检测仪,学习小组分别对酒精检测仪的原理进行探究性学习。
(1)一种传统的酒精检测仪利用乙醇与酸性 溶液的反应进行检测,甲组同学进行模拟实验,向酸性
溶液的反应进行检测,甲组同学进行模拟实验,向酸性 溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现
溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现 在溶液中显绿色,该实验体现乙醇的
在溶液中显绿色,该实验体现乙醇的_______ (填“氧化性”或者“还原性”)
(2)目前常用的是燃料电池型呼气酒精检测仪,其工作原理如图所示,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。
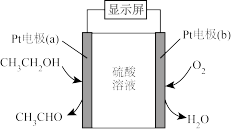
①负极电极反应式为_______ 。
②电池反应为_______ 。
(3)乙组同学设计如下装置(夹持装置省略)进一步探究 催化氧化反应。
催化氧化反应。
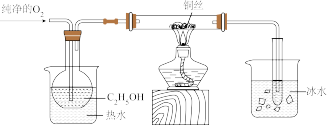
为检验反应产物,该小组同学分别取少量试管中的液体进行了如下实验,回答下列问题:已知:可以用检验葡萄糖的方法检验乙醛。
①热水浴的作用_______ 。
②实验b得出结论依据的现象是_______ 。
③实验a~c中的结论不合理的是_______ (填序号),原因是_______ 。
(1)一种传统的酒精检测仪利用乙醇与酸性
 溶液的反应进行检测,甲组同学进行模拟实验,向酸性
溶液的反应进行检测,甲组同学进行模拟实验,向酸性 溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现
溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现 在溶液中显绿色,该实验体现乙醇的
在溶液中显绿色,该实验体现乙醇的(2)目前常用的是燃料电池型呼气酒精检测仪,其工作原理如图所示,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。

①负极电极反应式为
②电池反应为
(3)乙组同学设计如下装置(夹持装置省略)进一步探究
 催化氧化反应。
催化氧化反应。
为检验反应产物,该小组同学分别取少量试管中的液体进行了如下实验,回答下列问题:已知:可以用检验葡萄糖的方法检验乙醛。
| 实验序号 | 检验试剂和反应条件 | 现象 | 结论 |
| a | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| b | 新制 悬浊液,加热 悬浊液,加热 | _______ | 产物含有乙醛 |
| c | 浅红色含酚酞的 溶液 溶液 | 浅红色褪去 | 产物可能含有乙酸 |
①热水浴的作用
②实验b得出结论依据的现象是
③实验a~c中的结论不合理的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾( )在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应: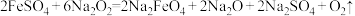 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,消耗117 g  转移
转移___________ mol电子。
(2)方法二:反应: (未配平)
(未配平)
①配平离子反应方程式:_______ ____ _____
_____ ______
______ _____
_____ _______
_______ ______
______
②若反应过程中转移了1.5 mol电子,则还原产物的物质的量为______ mol。
(3)向 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:___________ 。
 )在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。(1)方法一:可利用固体反应物反应:
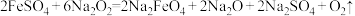 ,该反应中的氧化剂是
,该反应中的氧化剂是 转移
转移(2)方法二:反应:
 (未配平)
(未配平)①配平离子反应方程式:
 _____
_____ ______
______ _____
_____ _______
_______ ______
______
②若反应过程中转移了1.5 mol电子,则还原产物的物质的量为
(3)向
 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)在Fe3O4 +4CO 3Fe+4CO2的反应中,
3Fe+4CO2的反应中,____________ 是氧化剂,_________________ 是还原剂,_______ 元素被氧化,_______ 元素被还原。
(2)配平下列化学方程式并用单线桥法分析下列氧化还原反应中电子转移的方向和数目_________________ ,_____ Cu +___ HNO3(浓)===____ Cu(NO3)2+_____ NO2↑ +_____ H2O,浓硝酸表现出来的性质是_______________ (填写编号)。
①还原性 ②酸性 ③氧化性
 3Fe+4CO2的反应中,
3Fe+4CO2的反应中,(2)配平下列化学方程式并用单线桥法分析下列氧化还原反应中电子转移的方向和数目
①还原性 ②酸性 ③氧化性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求填空。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中
①只有氧化性的是___________ ;
②只有还原性的是___________ ;
③既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平)。
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是___________ (填序号)。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中
①只有氧化性的是
②只有还原性的是
③既有氧化性又有还原性的是
(2)某同学写出以下三个化学方程式(未配平)。
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定条件下,含氮元素的物质可发生如图所示的循环转化。
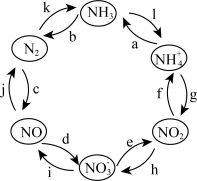
回答下列问题:
(1)氮的原子结构示意图为_________ 。
(2)图中属于“氮的固定”的是_________ (填字母,下同);转化过程中发生非氧化还原反应的是_________ 。
(3)若“反应h”是在NO2与H2O的作用下实现,则该反应中氧化产物与还原产物的物质的量之比为_________ 。
(4)若“反应i”是在酸性条件下由NO3-与Zn的作用实现,则该反应的离子方程式为_____ 。

回答下列问题:
(1)氮的原子结构示意图为
(2)图中属于“氮的固定”的是
(3)若“反应h”是在NO2与H2O的作用下实现,则该反应中氧化产物与还原产物的物质的量之比为
(4)若“反应i”是在酸性条件下由NO3-与Zn的作用实现,则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】① Cu ② CO2 ③液氨 ④H2SO4 ⑤ 酒精 ⑥NaCl溶液 ⑦水 ⑧CaCO3固体
(1)上述物质中属于电解质的是_____ (填序号,下同),属于非电解质是_____ 。
(2)常温下,② ⑦ ⑧这三种物质相互作用可生成一种新物质Ca(HCO3)2,该反应____ (填“是”或“不是”)氧化还原反应。
(3)写出④和⑧分别在水溶液中的电离方程式。______________________________________ 、_____________________________________
(1)上述物质中属于电解质的是
(2)常温下,② ⑦ ⑧这三种物质相互作用可生成一种新物质Ca(HCO3)2,该反应
(3)写出④和⑧分别在水溶液中的电离方程式。
您最近一年使用:0次
【推荐1】绿水青山就是金山银山,我国的废水处理再利用技术取得了重大突破.
(1)生活污水中的氮是造成水体富营养化的主要原因.某污水中同时存在 和
和 时,可用下列方法除去:
时,可用下列方法除去:
Ⅰ.先利用O2将 氧化成
氧化成 :
: (未配平);
(未配平);
Ⅱ.再将 还原成
还原成 (未配平).
(未配平).
①配平步骤Ⅰ中的方程式并用单线桥法标出电子转移的方向和数目____________________ .
②若该污水中含有1 mol NH4NO3,用上述方法处理完全后,共消耗__________ mol H2。
(2)含有NaCN的废水常用Ca(ClO)2处理,使其最终转化为无害物质.其反应如下:
反应Ⅰ:
反应Ⅱ: (CNO-中C为
(CNO-中C为 价)(未配平)
价)(未配平)
反应Ⅲ: (未配平)
(未配平)
①反应Ⅱ中的氧化剂是________________ (填化学式),氧化产物与还原产物的物质的量之比为________ 。
②若反应Ⅲ中转移0.6 mol电子,则生成的气体在标准状况下的总体积为__________ L。
(3)含高浓度CN-的废水可用多硫化物MS4溶液在碱性条件下处理,CN-被氧化成毒性较小的SCN-,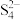 转化为S2-,写出该反应的离子方程式
转化为S2-,写出该反应的离子方程式_______________ 。
(4)工业上还可用硝酸铜和柠檬酸为原料,以 为催化剂,催化氧化处理含高浓度CN-的废水。CN-去除率与搅拌速率、时间和pH的关系如图所示:
为催化剂,催化氧化处理含高浓度CN-的废水。CN-去除率与搅拌速率、时间和pH的关系如图所示:

①由上图可知,在相同时间内最佳反应条件为______________________ 。
②分析pH>6时CN-去除率降低的原因(用相关离子方程式和文字说明)______________________ 。
(1)生活污水中的氮是造成水体富营养化的主要原因.某污水中同时存在
 和
和 时,可用下列方法除去:
时,可用下列方法除去:Ⅰ.先利用O2将
 氧化成
氧化成 :
: (未配平);
(未配平);Ⅱ.再将
 还原成
还原成 (未配平).
(未配平).①配平步骤Ⅰ中的方程式并用单线桥法标出电子转移的方向和数目
②若该污水中含有1 mol NH4NO3,用上述方法处理完全后,共消耗
(2)含有NaCN的废水常用Ca(ClO)2处理,使其最终转化为无害物质.其反应如下:
反应Ⅰ:

反应Ⅱ:
 (CNO-中C为
(CNO-中C为 价)(未配平)
价)(未配平)反应Ⅲ:
 (未配平)
(未配平)①反应Ⅱ中的氧化剂是
②若反应Ⅲ中转移0.6 mol电子,则生成的气体在标准状况下的总体积为
(3)含高浓度CN-的废水可用多硫化物MS4溶液在碱性条件下处理,CN-被氧化成毒性较小的SCN-,
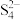 转化为S2-,写出该反应的离子方程式
转化为S2-,写出该反应的离子方程式(4)工业上还可用硝酸铜和柠檬酸为原料,以
 为催化剂,催化氧化处理含高浓度CN-的废水。CN-去除率与搅拌速率、时间和pH的关系如图所示:
为催化剂,催化氧化处理含高浓度CN-的废水。CN-去除率与搅拌速率、时间和pH的关系如图所示:
①由上图可知,在相同时间内最佳反应条件为
②分析pH>6时CN-去除率降低的原因(用相关离子方程式和文字说明)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,
该反应中Na2O2是___________ (填“氧化剂”、“还原剂”、“氧化剂和还原剂”)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:___________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为___________ mol
(3)已知:2Na+2H2O=2NaOH+H2↑
用双线桥标出该反应中电子转移的方向和数目___________ 。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,
该反应中Na2O2是
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
(3)已知:2Na+2H2O=2NaOH+H2↑
用双线桥标出该反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
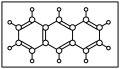
【推荐1】(1)高锰酸钾是常见的氧化剂,也是氧化还原滴定中的常用试剂。酸性KMnO4与蒽( 分子式C14H10)反应生成蒽醌(
分子式C14H10)反应生成蒽醌(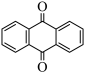 分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是
分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是_____ (填写化学式),发生氧化反应的原子是________ (在图中将相关位置的原子“○”涂黑,○表示碳原子, 表示氢原子);
(2)实验室盛放高锰酸钾溶液的试剂瓶常有黑色沉积物,是因KMnO4发生分解生成的MnO2所至,同时有KOH生成,另一反应产物是_______ (填写化学式),判断的理由是_____ 。
(3)在酸性条件下高锰酸钾与硫酸铬能发生反应,请配平该反应方程式:
____ Cr2(SO4)3+____ KMnO4+____ H2O→____ CrO3+____ K2SO4+____ MnSO4+____ H2SO4
(4)实验室称取0.867 g草酸钠(Na2C2O4,式量为134),溶解于水,加入一定量硫酸,用未知浓度的KMnO4溶液滴定,用去KMnO4溶液22.50 mL,反应式如下(未配平):MnO4+C2O42+H+→Mn2++CO2+H2O。则KMnO4溶液的浓度是________ mol/L。
 分子式C14H10)反应生成蒽醌(
分子式C14H10)反应生成蒽醌( 分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是
分子式C14H8O2),反应式为(未配平),C14H10(蒽) + KMnO4 +H2SO4→C14H8O2(蒽醌) + K2SO4+MnSO4 +H2O,反应中氧化剂是
(2)实验室盛放高锰酸钾溶液的试剂瓶常有黑色沉积物,是因KMnO4发生分解生成的MnO2所至,同时有KOH生成,另一反应产物是
(3)在酸性条件下高锰酸钾与硫酸铬能发生反应,请配平该反应方程式:
(4)实验室称取0.867 g草酸钠(Na2C2O4,式量为134),溶解于水,加入一定量硫酸,用未知浓度的KMnO4溶液滴定,用去KMnO4溶液22.50 mL,反应式如下(未配平):MnO4+C2O42+H+→Mn2++CO2+H2O。则KMnO4溶液的浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知下列信息:
Ⅰ.部分物质的溶解性:
Ⅱ.高锰酸钾是常见的氧化剂,酸性环境下,高锰酸钾被还原为Mn2+。
结合上面的信息和相关化学知识,回答下列问题:
(1)银单质不溶于水,实验室经常用稀硝酸清洗试管内壁附着的银单质。涉及的化学反应为3Cu+8HNO3=3 Cu(NO3)2+2NO↑+4H2O。
①该反应中的还原剂是____ (填化学式,下同)。
②该反应中,发生还原反应的过程是____ →____ 。
③写出该反应的离子反应方程式:_____
(2)某同学用稀硫酸酸化的高锰酸钾溶液对银单质进行清洗。实验现象如下:在试管中加入酸性高锰酸钾溶液,振荡,银溶解,溶液紫色褪去,转为无色,但略显浑浊。
上述实验过程中,银被氧化为____ (填离子符号),略显浑浊是因为生成了____ (填化学式)。该过程发生的化学反应方程式为______ 。
Ⅰ.部分物质的溶解性:
| SO42- | OH- | Cl- | NO3- | |
| Mn2+ | 溶 | 不 | 溶 | 溶 |
| Ba2+ | 不 | 溶 | 溶 | 溶 |
| Ag+ | 微 | — | 不 | 溶 |
| Ca2+ | 微 | 微 | 溶 | 溶 |
| H+ | 溶 | 溶 | 溶 |
Ⅱ.高锰酸钾是常见的氧化剂,酸性环境下,高锰酸钾被还原为Mn2+。
结合上面的信息和相关化学知识,回答下列问题:
(1)银单质不溶于水,实验室经常用稀硝酸清洗试管内壁附着的银单质。涉及的化学反应为3Cu+8HNO3=3 Cu(NO3)2+2NO↑+4H2O。
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的离子反应方程式:
(2)某同学用稀硫酸酸化的高锰酸钾溶液对银单质进行清洗。实验现象如下:在试管中加入酸性高锰酸钾溶液,振荡,银溶解,溶液紫色褪去,转为无色,但略显浑浊。
上述实验过程中,银被氧化为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求完成下列方程式。
(1)已知在酸性介质中FeSO4能将+6价铬还原成+3价铬。写出 与FeS溶液在酸性条件下反应的离子方程式:
与FeS溶液在酸性条件下反应的离子方程式:_______ 。
(2)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中 (B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和
(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和 ,其反应的离子方程式为
,其反应的离子方程式为_______ 。
(3)Na2S溶液长期放置有硫析出,原因为_______ (用离子方程式表示)。
(4)生产硫化钠大多采用无水芒硝(Na2SO4)—碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:_______ 。
(5)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其反应的离子方程式为_______ 。
(1)已知在酸性介质中FeSO4能将+6价铬还原成+3价铬。写出
 与FeS溶液在酸性条件下反应的离子方程式:
与FeS溶液在酸性条件下反应的离子方程式:(2)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中
 (B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和
(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和 ,其反应的离子方程式为
,其反应的离子方程式为(3)Na2S溶液长期放置有硫析出,原因为
(4)生产硫化钠大多采用无水芒硝(Na2SO4)—碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:
(5)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其反应的离子方程式为
您最近一年使用:0次

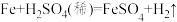

 .
. 电子时,消耗
电子时,消耗 的质量是
的质量是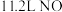 气体(标准状况下)时,被还原的
气体(标准状况下)时,被还原的 的物质的量是
的物质的量是

