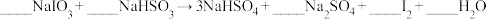(一)储氢纳米碳管研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应的化学方程式如下: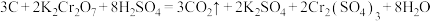
回答下列问题:
(1)该反应中,氧化产物是___________ (填化学式),被还原的元素是___________ (填元素符号), 发生了
发生了___________ (填“氧化反应”或“还原反应”)。
(2) 在该反应中表现出___________。
在该反应中表现出___________。
(3)用单线桥表示出上述反应电子转移的方向和数目___________ 。
(二)次磷酸( )是一种精细磷化工产品,是一元弱酸,具有较强还原性。回答下列问题:
)是一种精细磷化工产品,是一元弱酸,具有较强还原性。回答下列问题:
(4)从分类来看, 属于
属于___________
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5) 的工业制法是:将白磷(
的工业制法是:将白磷( )与
)与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应。配平白磷与
反应。配平白磷与 溶液反应的化学方程式
溶液反应的化学方程式___________ 。

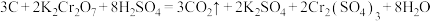
回答下列问题:
(1)该反应中,氧化产物是
 发生了
发生了(2)
 在该反应中表现出___________。
在该反应中表现出___________。| A.只有酸性 | B.只有氧化性 | C.酸性和氧化性 | D.酸性和还原性 |
(二)次磷酸(
 )是一种精细磷化工产品,是一元弱酸,具有较强还原性。回答下列问题:
)是一种精细磷化工产品,是一元弱酸,具有较强还原性。回答下列问题:(4)从分类来看,
 属于
属于a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)
 的工业制法是:将白磷(
的工业制法是:将白磷( )与
)与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应。配平白磷与
反应。配平白磷与 溶液反应的化学方程式
溶液反应的化学方程式
更新时间:2023-12-16 10:08:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是_______ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置会产生沉淀
b.分散质粒子可通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的_______ (填序号),该提纯方法名称是_______ 。
A.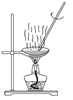 B.
B. C.
C. 
(4)实验室常用向煮沸的蒸馏水中滴加饱和FeCl3溶液制备Fe(OH)3胶体,证明实验是否成功最常用的方法是_______ 。向制备的Fe(OH)3胶体中逐滴滴入过量稀硫酸,出现的现象是_______ 。
(5)现有10 mL明胶的水溶液与5 mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_______ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置会产生沉淀
b.分散质粒子可通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的
A.
 B.
B. C.
C. 
(4)实验室常用向煮沸的蒸馏水中滴加饱和FeCl3溶液制备Fe(OH)3胶体,证明实验是否成功最常用的方法是
(5)现有10 mL明胶的水溶液与5 mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有以下几种物质:①金刚石;②生石灰;③稀硫酸;④干冰;⑤铜;⑥高锰酸钾;⑦碳酸钠;⑧无水乙醇。
(1)①的一种同素异形体是___________ (填物质的名称);
(2)属于氧化物的有___________ (填物质的序号,下同);
(3)属于电解质的有___________ ;
(4)能够导电的物质有___________ ;
(1)①的一种同素异形体是
(2)属于氧化物的有
(3)属于电解质的有
(4)能够导电的物质有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
①生石灰属于哪种类型的物质?_______ 。
②生石灰可做干燥剂的理由是(用化学方程式表示)_______ 。
③生石灰还可以跟哪些类别的物质发生化学反应?列举两例,并写出化学方程式:_______ 。
(2)氮化钠(Na3N)是科学家制备的一种重要化合物。它与水作用可产生氨气(NH3)。试回答下列问题:
①氮化钠(Na3N)中N元素化合价是_______ ,该化合物属于_______ 化合物(填“离子”或“共价”,下同),生成的NH3属于_______ 化合物。
②氮化钠(Na3N)与水反应的方程式是_______ 。
(1)同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
①生石灰属于哪种类型的物质?
②生石灰可做干燥剂的理由是(用化学方程式表示)
③生石灰还可以跟哪些类别的物质发生化学反应?列举两例,并写出化学方程式:
(2)氮化钠(Na3N)是科学家制备的一种重要化合物。它与水作用可产生氨气(NH3)。试回答下列问题:
①氮化钠(Na3N)中N元素化合价是
②氮化钠(Na3N)与水反应的方程式是
您最近一年使用:0次
【推荐1】氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)服用维生素C,可以使食物中的Fe3+转化为Fe2+,说明维生素C具有____ (填“氧化”或“还原”)性。
(2)我国古代四大发明之一的黑火药爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是____ (填化学式)。
(3)H2O2在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液(用硫酸酸化)可与H2O2反应,其化学方程式是:H2O2+KMnO4+H2SO4——X+MnSO4+O2↑+H2O(未配平)。
已知:稀MnSO4溶液几乎无色。
①X的化学式是____ 。
②被氧化的元素是____ (填元素符号)。
③请配平上述反应,写出离子方程式并用单桥法标出上述反应中电子转移的方向和数目____ 。
④向酸性KMnO4溶液中滴入双氧水,观察到的现象是____ 。
(1)服用维生素C,可以使食物中的Fe3+转化为Fe2+,说明维生素C具有
(2)我国古代四大发明之一的黑火药爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是
(3)H2O2在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液(用硫酸酸化)可与H2O2反应,其化学方程式是:H2O2+KMnO4+H2SO4——X+MnSO4+O2↑+H2O(未配平)。
已知:稀MnSO4溶液几乎无色。
①X的化学式是
②被氧化的元素是
③请配平上述反应,写出离子方程式并用单桥法标出上述反应中电子转移的方向和数目
④向酸性KMnO4溶液中滴入双氧水,观察到的现象是
您最近一年使用:0次
【推荐2】氧化还原反应是一类重要的化学反应,广泛存在于生产、生活中。回答下列问题:
(1)以乙烯(C2H4)脱硫的方法治理燃煤尾气中的SO2,其机理如图所示。过程ⅰ、ⅱ、ⅲ中涉及氧化还原反应的是___________ ,图中涉及的物质属于酸性氧化物的是___________ (填化学式)。

(2)某工业废水含有大些对人体健康有危害的 ,为了降低废水中
,为了降低废水中 的浓度,可以在碱性条件下用铅粉将
的浓度,可以在碱性条件下用铅粉将 还原为N2,其化学方程式为
还原为N2,其化学方程式为 。
。
①Na[Al(OH)4]中Al的化合价为___________ 。
②上述反应中,被氧化的元素是___________ (填元素符号),还原产物的化学式为___________ 。
③反应中每生成1 mol N2,转移___________ 个电子。
(3)“假黄金”实际上是铜合金,可用稀硝酸鉴别。配平该反应 化学方程式
化学方程式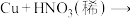
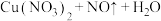 :
:___________ 。
(1)以乙烯(C2H4)脱硫的方法治理燃煤尾气中的SO2,其机理如图所示。过程ⅰ、ⅱ、ⅲ中涉及氧化还原反应的是

(2)某工业废水含有大些对人体健康有危害的
 ,为了降低废水中
,为了降低废水中 的浓度,可以在碱性条件下用铅粉将
的浓度,可以在碱性条件下用铅粉将 还原为N2,其化学方程式为
还原为N2,其化学方程式为 。
。①Na[Al(OH)4]中Al的化合价为
②上述反应中,被氧化的元素是
③反应中每生成1 mol N2,转移
(3)“假黄金”实际上是铜合金,可用稀硝酸鉴别。配平该反应
 化学方程式
化学方程式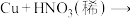
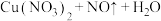 :
:
您最近一年使用:0次
【推荐3】已知下列反应:
①SO2+H2O═H2SO3
②C+H2O═H2+CO
③2A1+6H+═2Al3++3H2↑
④2Mg+CO2 2MgO+C
2MgO+C
⑤2Na2O2+2H2O═4NaOH+O2↑
⑥CaC2+2H2O═Ca(OH)2+C2H2↑
⑦8NH3+3Cl2═6NH4Cl+N2
(1)上述反应中不属于氧化还原反应的有____ (填各反应的序号,下同);反应物中H2O被还原的是____ :还原产物为单质的是____ 。
(2)用单线桥表示反应④中电子转移的方向和数目____ 。
(3)反应⑤中每生成1个氧气转移的电子数目为____ 。
(4)反应⑦中氧化剂与还原剂的分子个数比:____ 。
(5)氧化还原反应方程式的配平
① KI+ KIO3+ H2SO4═ I2+ K2SO4+ H2O____ 。
② MnO + H2O2+ ═ Mn2++ O2↑+ H2O
+ H2O2+ ═ Mn2++ O2↑+ H2O____ 。
①SO2+H2O═H2SO3
②C+H2O═H2+CO
③2A1+6H+═2Al3++3H2↑
④2Mg+CO2
 2MgO+C
2MgO+C⑤2Na2O2+2H2O═4NaOH+O2↑
⑥CaC2+2H2O═Ca(OH)2+C2H2↑
⑦8NH3+3Cl2═6NH4Cl+N2
(1)上述反应中不属于氧化还原反应的有
(2)用单线桥表示反应④中电子转移的方向和数目
(3)反应⑤中每生成1个氧气转移的电子数目为
(4)反应⑦中氧化剂与还原剂的分子个数比:
(5)氧化还原反应方程式的配平
① KI+ KIO3+ H2SO4═ I2+ K2SO4+ H2O
② MnO
 + H2O2+ ═ Mn2++ O2↑+ H2O
+ H2O2+ ═ Mn2++ O2↑+ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成溶液C,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D.
⑴写出下列物质的化学式:B______ E______ D______
⑵写出A→C的化学方程式,并标出电子转移的方向和数目:__________ 。
⑶写出C→D的离子方程式:_______________
⑷写出化学方程式:E+B D+C+O2↑:
D+C+O2↑:_____________ .
⑴写出下列物质的化学式:B
⑵写出A→C的化学方程式,并标出电子转移的方向和数目:
⑶写出C→D的离子方程式:
⑷写出化学方程式:E+B
 D+C+O2↑:
D+C+O2↑:
您最近一年使用:0次
【推荐2】请配平以下反应方程式并回答下列问题:_________
___K2Cr2O7+___HCl(浓)→___KCl+___Cl2↑+___CrCl3+___H2O
(1)K2Cr2O7 中Cr的化合价为______ ,该反应中被氧化的元素是_____ ,还原产物是_____ 。
(2)此反应中HCl表现出酸性和_____ 性,这两部分HCl的物质的量之比为______ ,该反应中氧化剂和还原剂物质的量之比为_____ 。
(3)若该反应在标准状况下收集到4.48 L的Cl2则转移的电子物质的量为_____ 。
(4)用双线桥法表示以下反应的电子转移方向和数目。_______
3NO2+H2O=2HNO3+NO
___K2Cr2O7+___HCl(浓)→___KCl+___Cl2↑+___CrCl3+___H2O
(1)K2Cr2O7 中Cr的化合价为
(2)此反应中HCl表现出酸性和
(3)若该反应在标准状况下收集到4.48 L的Cl2则转移的电子物质的量为
(4)用双线桥法表示以下反应的电子转移方向和数目。
3NO2+H2O=2HNO3+NO
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】除去烟气中的NO,能促进生态文明建设。
(1)含 和
和 的酸性吸收液可以处理烟气中NO,原理是:
的酸性吸收液可以处理烟气中NO,原理是: 催化
催化 产生
产生 ,后者将NO最终氧化成
,后者将NO最终氧化成 。
。
①写出 将NO氧化成
将NO氧化成 的离子方程式为:
的离子方程式为:_______ 。
②吸收液的初始pH和温度对 氧化NO的效果分别如图1和图2所示。
氧化NO的效果分别如图1和图2所示。

当吸收液的初始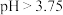 时,NO氧化率明显降低,原因可能是:
时,NO氧化率明显降低,原因可能是:
(i)pH较大时, 容易发生歧化反应,导致
容易发生歧化反应,导致 浓度降低,氧化能力减弱:
浓度降低,氧化能力减弱:
(ii)_______ 。
③当超过60℃时,NO的氧化率明显降低,原因可能是:_______ 。
(2) 可在
可在 催化下还原烟气中NO,温度对该反应的影响如图3所示。
催化下还原烟气中NO,温度对该反应的影响如图3所示。
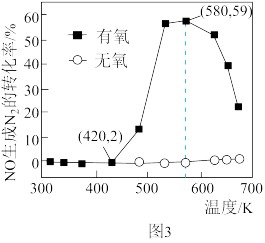
①在420~580K之间,有氧条件下NO生成 的转化率明显高于无氧条件,原因可能是
的转化率明显高于无氧条件,原因可能是_______ 。
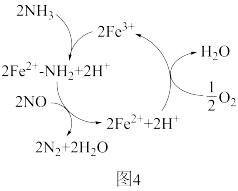
②进一步研究发现,以 为催化利时,
为催化利时, 在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:_______ 。
(1)含
 和
和 的酸性吸收液可以处理烟气中NO,原理是:
的酸性吸收液可以处理烟气中NO,原理是: 催化
催化 产生
产生 ,后者将NO最终氧化成
,后者将NO最终氧化成 。
。①写出
 将NO氧化成
将NO氧化成 的离子方程式为:
的离子方程式为:②吸收液的初始pH和温度对
 氧化NO的效果分别如图1和图2所示。
氧化NO的效果分别如图1和图2所示。
当吸收液的初始
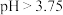 时,NO氧化率明显降低,原因可能是:
时,NO氧化率明显降低,原因可能是:(i)pH较大时,
 容易发生歧化反应,导致
容易发生歧化反应,导致 浓度降低,氧化能力减弱:
浓度降低,氧化能力减弱:(ii)
③当超过60℃时,NO的氧化率明显降低,原因可能是:
(2)
 可在
可在 催化下还原烟气中NO,温度对该反应的影响如图3所示。
催化下还原烟气中NO,温度对该反应的影响如图3所示。
①在420~580K之间,有氧条件下NO生成
 的转化率明显高于无氧条件,原因可能是
的转化率明显高于无氧条件,原因可能是②进一步研究发现,以
 为催化利时,
为催化利时, 在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与NO在加热和催化剂作用下生成N2O的化学方程式为___________ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为:
NO+NO2+2OH-=2 +H2O
+H2O
2NO2+2OH-= +
+ +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是___________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与NO在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为:
NO+NO2+2OH-=2
 +H2O
+H2O2NO2+2OH-=
 +
+ +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。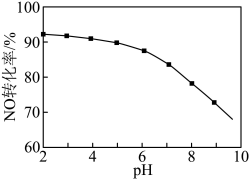
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知微粒间的相互作用有以下几种:
①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力(范德华力)
下面是某同学对一些变化过程破坏的微粒间的相互作用的判断(填序号)
A.硫酸氢钠溶于水__________ ; B.氢氧化钠溶于水__________ ;C.冰熔化__________________ 。
(2)用电子式表示MgBr2 的形成过程:_________________________________________ 。
(3)下列物质各原子都达8e-稳定结构的是_________ (填序号)
A.CH4 B.CS2 C.PCl5 D.PH3 E.N2 F.HCl
(4)向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:_____________________________________ 。
①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力(范德华力)
下面是某同学对一些变化过程破坏的微粒间的相互作用的判断(填序号)
A.硫酸氢钠溶于水
(2)用电子式表示MgBr2 的形成过程:
(3)下列物质各原子都达8e-稳定结构的是
A.CH4 B.CS2 C.PCl5 D.PH3 E.N2 F.HCl
(4)向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:
您最近一年使用:0次