 胶体具有良好的净水效果,某实验小组尝试制备
胶体具有良好的净水效果,某实验小组尝试制备 胶体并对其进行性质探究。
胶体并对其进行性质探究。(1)制备的实验操作:将
(2)胶体和溶液在外观上并无太大差异,为确认生成的物质是否为胶体,该小组同学用红光激光笔水平照射,若出现
(3)小红用如图所示的装置除去
 胶体中的杂质氯离子,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体中的杂质氯离子,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 溶液,若
溶液,若 胶体中的杂质氯离子已经完全除去。
胶体中的杂质氯离子已经完全除去。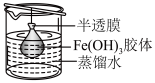
(4)小明同学将提纯后的
 胶体置于U型管中(如图),通入直流电一段时间后,观察到与电源
胶体置于U型管中(如图),通入直流电一段时间后,观察到与电源
更新时间:2023-12-19 14:58:52
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钛酸锰(MnTiO3)纳米材料是一种多用途催化剂。工业上用红钛锰矿(主要成分有MnTiO3,还含有少量FeO、Fe2O3、SiO2等杂质)来制备MnTiO3,其工艺流程如图所示:
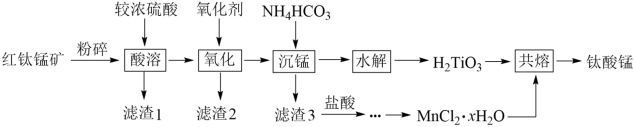
已知①红钛锰矿“酸溶”后Ti元素主要以TiO2+的形式存在;
②H2TiO3不溶于无机酸和碱,不溶于水;
③在空气中加热无水MnCl2分解放出HCl,生成Mn3O4。
回答下列问题:
(1)“粉碎”的目的是__ 。
(2)“酸溶”中发生的主要反应化学方程式为__ 。
(3)为了更好地把滤渣2分离出来,除搅拌外,还需要(填操作名称)___ 。
(4)“氧化”的氧化剂选用的是高锰酸钾,而不选择通常人们认可的绿色氧化剂“双氧水”,除了高锰酸钾氧化性强、反应快之外,还可能的原因是__ (写出一条即可)。
(5)“沉锰”的条件一般控制在45℃以下的原因是__ 。
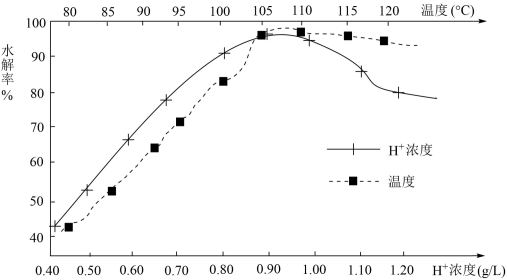
(6)TiO2+的水解率受温度和H+浓度的影响如图所示,TiO2+最适宜的水解条件是__ 。
(7)测定所得MnCl2·xH2O晶体中结晶水的含量。取29.70g样品加热分解,热重曲线(TG)如图所示。
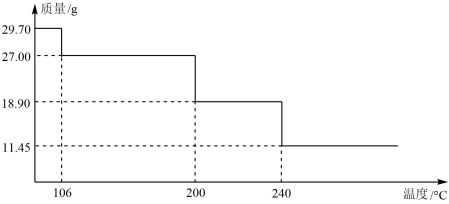
所得氯化锰晶体x的值是__ 。

已知①红钛锰矿“酸溶”后Ti元素主要以TiO2+的形式存在;
②H2TiO3不溶于无机酸和碱,不溶于水;
③在空气中加热无水MnCl2分解放出HCl,生成Mn3O4。
回答下列问题:
(1)“粉碎”的目的是
(2)“酸溶”中发生的主要反应化学方程式为
(3)为了更好地把滤渣2分离出来,除搅拌外,还需要(填操作名称)
(4)“氧化”的氧化剂选用的是高锰酸钾,而不选择通常人们认可的绿色氧化剂“双氧水”,除了高锰酸钾氧化性强、反应快之外,还可能的原因是
(5)“沉锰”的条件一般控制在45℃以下的原因是
(6)TiO2+的水解率受温度和H+浓度的影响如图所示,TiO2+最适宜的水解条件是

(7)测定所得MnCl2·xH2O晶体中结晶水的含量。取29.70g样品加热分解,热重曲线(TG)如图所示。

所得氯化锰晶体x的值是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用_______ 来区分Fe(OH)3胶体和FeCl3溶液。
(2)铁粉与水蒸气在高温条件下反应的化学方程式是_______ 。
(3)电子工业中,人们常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并从废液中回收 和FeCl3溶液。实验室模拟流程如图所示:
和FeCl3溶液。实验室模拟流程如图所示:

①请写出FeCl3溶液与铜反应的离子方程式_______ 。
②试剂X在反应中体现_______ (填“氧化性”或“还原性”)。
③Z可选用的试剂有_______ (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
(1)可利用
(2)铁粉与水蒸气在高温条件下反应的化学方程式是
(3)电子工业中,人们常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并从废液中回收
 和FeCl3溶液。实验室模拟流程如图所示:
和FeCl3溶液。实验室模拟流程如图所示:
①请写出FeCl3溶液与铜反应的离子方程式
②试剂X在反应中体现
③Z可选用的试剂有
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化钠溶液中混有硫酸钠、氯化钙溶液和淀粉胶体。选择适当的试剂和方法从中提纯出氯化钠晶体。相应的实验过程如图:
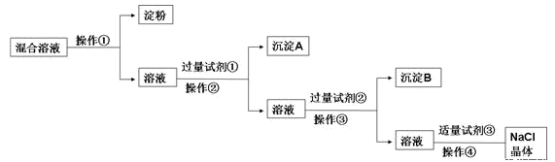
(1)写出上述实验过程中所用试剂(写化学式):试剂②_______ ;试剂③_______ 。
(2)判断试剂②已过量的方法是:_______ 。
(3)操作①时利用半透膜进行分离提纯。操作①的实验结果:淀粉_______ (填“能”或“不能”)透过半透膜;硫酸根离子_______ (填“能”或“不能”)透过半透膜。请用实验证明上述结果,完成表格(可不填满,也可增加)。限选试剂:1mol/L硝酸银溶液、1mol/L氯化钡溶液,1mol/L硝酸钡溶液、碘水、稀盐酸、稀硝酸

(1)写出上述实验过程中所用试剂(写化学式):试剂②
(2)判断试剂②已过量的方法是:
(3)操作①时利用半透膜进行分离提纯。操作①的实验结果:淀粉
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1 mol/L的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是________ 。
(2)利用胶体的____________________ 性质区分Fe(OH)3胶体和FeCl3溶液
(3)丁同学利用所制得的Fe(OH)3胶体进行实验:
①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体粒子带_____ (填“正”或“负”)电荷。
②向其中加入饱和Na2SO4溶液,产生的现象是____________________ 。
(4)写出甲同学的离子反应方程式_______________________________
甲同学:向1 mol/L的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)利用胶体的
(3)丁同学利用所制得的Fe(OH)3胶体进行实验:
①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体粒子带
②向其中加入饱和Na2SO4溶液,产生的现象是
(4)写出甲同学的离子反应方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】有下列词语:①渗析 ②盐析 ③聚沉 ④溶胶 ⑤凝胶 ⑥电泳 ⑦丁达尔效应 ⑧中和 ⑨水解,选出适当的词语将其序号填入下列空格中。
(1)往浓肥皂水中加入饱和食盐水(或固体食盐),肥皂凝聚,这种现象称为________ 。
(2)在肥皂水中透过强光,可看到光带,这种现象称为________ 。
(3)使热的浓肥皂水冷却并完全固化后的物质叫________ 。
(4)在肥皂水中加入酚酞变红色,说明高级脂肪酸根离子发生了________ 。
(5)在Fe(OH)3胶体中加入(NH4)2SO4产生红褐色沉淀,这种现象叫做________ 。
(6)用半透膜把制取Fe(OH)3胶体中生成的氯化钠分离出的方法叫做________ 。
(7)在水泥和冶金工厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染。这种做法应用的主要原理是________ 。
(1)往浓肥皂水中加入饱和食盐水(或固体食盐),肥皂凝聚,这种现象称为
(2)在肥皂水中透过强光,可看到光带,这种现象称为
(3)使热的浓肥皂水冷却并完全固化后的物质叫
(4)在肥皂水中加入酚酞变红色,说明高级脂肪酸根离子发生了
(5)在Fe(OH)3胶体中加入(NH4)2SO4产生红褐色沉淀,这种现象叫做
(6)用半透膜把制取Fe(OH)3胶体中生成的氯化钠分离出的方法叫做
(7)在水泥和冶金工厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染。这种做法应用的主要原理是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铁和铝是两种重要的金属,它们的单质及其化合物有着各自的性质。
(1)现配制100mL0.01mol∙L-1FeCl3溶液,配制过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需要_______ 。
(2)将饱和FeCl3溶液滴入沸水可得到红褐色液体,反应的化学方程式是_______ 。此液体具有的性质是_______ (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.将该液体进行过滤,可得到红褐色固体
c.将该液体加热、蒸干、灼烧后,有氧化物生成
d.向该液体中加入硝酸银溶液,无沉淀产生
(3)“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分 )氧化为
)氧化为 ,并使溶液酸性增强。
,并使溶液酸性增强。
①该过程反应的离子方程式为_______ 。
②人们可利用 作强氧化剂溶解铜矿石(
作强氧化剂溶解铜矿石( ),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:_______ 。
_______Cu2S+_______Fe3++_______H2O _______Fe2++_______Cu2++_______+_______
_______Fe2++_______Cu2++_______+_______
(4)羟胺(NH2OH)是一种还原剂,用50.00mL0.25mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与25.00mL0.5mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是_______ 。
(1)现配制100mL0.01mol∙L-1FeCl3溶液,配制过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需要
(2)将饱和FeCl3溶液滴入沸水可得到红褐色液体,反应的化学方程式是
a.光束通过该液体时形成光亮的“通路”
b.将该液体进行过滤,可得到红褐色固体
c.将该液体加热、蒸干、灼烧后,有氧化物生成
d.向该液体中加入硝酸银溶液,无沉淀产生
(3)“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分
 )氧化为
)氧化为 ,并使溶液酸性增强。
,并使溶液酸性增强。①该过程反应的离子方程式为
②人们可利用
 作强氧化剂溶解铜矿石(
作强氧化剂溶解铜矿石( ),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:_______Cu2S+_______Fe3++_______H2O
 _______Fe2++_______Cu2++_______+_______
_______Fe2++_______Cu2++_______+_______
(4)羟胺(NH2OH)是一种还原剂,用50.00mL0.25mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与25.00mL0.5mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成再加入过量的稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,写出生成该白色沉淀的离子方程式为_______ 。
(4)原溶液可能大量共存的阴离子是_______(填字母)。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成再加入过量的稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是_______(填字母)。
| A.OH— | B. | C. | D.Cl— |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①取少量白色固体粉末于烧杯中,加水搅拌,有白色不溶物生成,过滤,滤液无色透明。
②取①的白色不溶物少量于试管中,加入足量稀硝酸,固体完全溶解,并有无色气泡产生。
③取①所得的滤液2mL于试管中,滴入几滴稀硫酸,有白色沉淀产生。
④另取①得到的无色透明溶液少量于试管中,加入足量硝酸酸化的AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是___________ (写化学式,下同),一定不含有的物质是___________ 。
(2)写出各步变化的离子方程式。
①___________ ;
②___________ ;
③___________ ;
④___________ 。
①取少量白色固体粉末于烧杯中,加水搅拌,有白色不溶物生成,过滤,滤液无色透明。
②取①的白色不溶物少量于试管中,加入足量稀硝酸,固体完全溶解,并有无色气泡产生。
③取①所得的滤液2mL于试管中,滴入几滴稀硫酸,有白色沉淀产生。
④另取①得到的无色透明溶液少量于试管中,加入足量硝酸酸化的AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)写出各步变化的离子方程式。
①
②
③
④
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学活动小组设计如图所示实验装置(部分夹持装置已略去),以探究潮湿的Cl2与Na2CO3反应的产物。
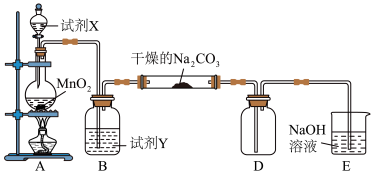
(1)写出装置A中发生反应的离子方程式_________ 。
(2)试剂Y是________ 。
(3)将C中(Na2CO3)反应后的固体物质分成两等份分装于两支试管中。
①向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,写出产生此现象的离子方程式________ ;由此现象推断固体产物中含有________ (填化学式,下同)。
②向另一支试管中滴加过量的稀硝酸,有无色无味的气体产生,溶液澄清,再向溶液中滴加过量的AgNO3溶液,溶液变浑浊,经过滤、洗涤、干燥,得到白色固体,由此现象推断固体产物中含有________ 。
(4)已知C中有Cl2、H2O参加反应,D中收集到的气体是氯的正一价氧化物。结合①和②中现象可推知,C中反应的化学方程式为_________ 。

(1)写出装置A中发生反应的离子方程式
(2)试剂Y是
(3)将C中(Na2CO3)反应后的固体物质分成两等份分装于两支试管中。
①向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,写出产生此现象的离子方程式
②向另一支试管中滴加过量的稀硝酸,有无色无味的气体产生,溶液澄清,再向溶液中滴加过量的AgNO3溶液,溶液变浑浊,经过滤、洗涤、干燥,得到白色固体,由此现象推断固体产物中含有
(4)已知C中有Cl2、H2O参加反应,D中收集到的气体是氯的正一价氧化物。结合①和②中现象可推知,C中反应的化学方程式为
您最近一年使用:0次



