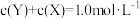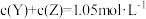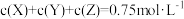在高温、高压和有催化剂的恒容密闭容器中进行反应: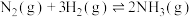 。下列叙述不正确的是
。下列叙述不正确的是
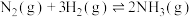 。下列叙述不正确的是
。下列叙述不正确的是A.若向容器中充入 和 和 ,最终将生成 ,最终将生成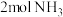 |
| B.向容器中充入He(不参与反应)对反应速率没有影响 |
| C.使用催化剂是为了加快反应速率 |
| D.增大氮气的浓度可加快反应速率 |
更新时间:2023/12/19 17:23:52
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】 还原钼矿(主要成分为
还原钼矿(主要成分为 )制备单质钼,能防止
)制备单质钼,能防止 污染,该反应原理为
污染,该反应原理为
 。向盛有一定比例
。向盛有一定比例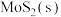 、
、 混合物的恒容密闭容器中通入
混合物的恒容密闭容器中通入 使其起始浓度为
使其起始浓度为 ,在一定条件下发生上述反应,测得容器中反应达到平衡状态时
,在一定条件下发生上述反应,测得容器中反应达到平衡状态时 的浓度为
的浓度为 。下列说法正确的是
。下列说法正确的是
 还原钼矿(主要成分为
还原钼矿(主要成分为 )制备单质钼,能防止
)制备单质钼,能防止 污染,该反应原理为
污染,该反应原理为
 。向盛有一定比例
。向盛有一定比例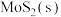 、
、 混合物的恒容密闭容器中通入
混合物的恒容密闭容器中通入 使其起始浓度为
使其起始浓度为 ,在一定条件下发生上述反应,测得容器中反应达到平衡状态时
,在一定条件下发生上述反应,测得容器中反应达到平衡状态时 的浓度为
的浓度为 。下列说法正确的是
。下列说法正确的是A.若达到平衡所需时间为t s,则0~t s内用CO表示的平均反应速率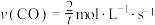 |
B.达到平衡状态时, |
| C.升高温度、使用催化剂均能加快该反应的反应速率 |
D.平衡后,再充入 ,反应速率不会改变 ,反应速率不会改变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
| A.凡是放热反应均能自发进行 |
B.N2(g)+3H2(g) 2NH3(g) Δ H<0,当升高温度,该反应的 v(正)减小、v(逆)增大 2NH3(g) Δ H<0,当升高温度,该反应的 v(正)减小、v(逆)增大 |
| C.钠投入水中,熔化成小球,说明钠和水的反应,反应物的总能量大于生成物的总能量 |
| D.中和热测定时环形玻璃搅拌棒要不断顺时针搅拌,目的是为了混合均匀,充分反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组将下表中所给的混合溶液分别加入到6个盛有过量 粒的反应瓶中,以研究硫酸铜的浓度对稀硫酸与锌反应生成氢气速率的影响。下列判断不正确的是
粒的反应瓶中,以研究硫酸铜的浓度对稀硫酸与锌反应生成氢气速率的影响。下列判断不正确的是
 粒的反应瓶中,以研究硫酸铜的浓度对稀硫酸与锌反应生成氢气速率的影响。下列判断不正确的是
粒的反应瓶中,以研究硫酸铜的浓度对稀硫酸与锌反应生成氢气速率的影响。下列判断不正确的是 实验组别 混合溶液 |  |  |  |  |  |  |
 | 30 |  |  |  | 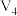 | 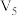 |
饱和 溶液/ 溶液/ | 0 | 0.5 | 2.5 | 5 |  | 20 |
 |  |  |  |  | 10 | 0 |
A. , , , , |
B.本实验利用了控制变量思想,变量为 浓度 浓度 |
C.反应一段时间后,实验 的金属表面可能呈现红色 的金属表面可能呈现红色 |
| D.该小组的实验结论是硫酸铜对稀硫酸与锌反应生成氢气有催化作用 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】100 mL 6 mol·L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量
| A.碳酸钠溶液 | B.氨水 | C.硫酸钾溶液 | D.硝酸钠溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列实验内容能达到相应实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 向1mL  ,溶液中加入5mL ,溶液中加入5mL  溶液,充分反应后,加入2mL苯,充分振荡、静置,分液后将水层分装于两支小试管中,向其中一支小试管中滴加5~6滴15%的 溶液,充分反应后,加入2mL苯,充分振荡、静置,分液后将水层分装于两支小试管中,向其中一支小试管中滴加5~6滴15%的 溶液,观察并比较两支试管中溶液的颜色 溶液,观察并比较两支试管中溶液的颜色 | 证明 与 与 之间的反应属于可逆反应 之间的反应属于可逆反应 |
| B | 室温时,将等体积、等物质的量浓度的 、 、 ,溶液分别加入等体积的30%的 ,溶液分别加入等体积的30%的 溶液中,观察并比较两支试管中气泡产生的快慢 溶液中,观察并比较两支试管中气泡产生的快慢 | 探究 、 、 催化效果的优劣 催化效果的优劣 |
| C | 取两支试管,分别加入5mL4%、5mL12%的 溶液,向其中一支试管中加入少量 溶液,向其中一支试管中加入少量 粉末,观察并比较两支试管中气泡产生的快慢 粉末,观察并比较两支试管中气泡产生的快慢 | 探究浓度对反应速率的影响 |
| D | 将相同体积相同浓度的稀硫酸分别加入两支试管中,再向两支试管中分别加入不同体积、等浓度的 溶液,将两支试管分别放入盛有等温等量的热水的烧杯中,观察并比较两支试管中出现浑浊现象的快慢 溶液,将两支试管分别放入盛有等温等量的热水的烧杯中,观察并比较两支试管中出现浑浊现象的快慢 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】 可催化
可催化 分解,机理,Ⅰ:
分解,机理,Ⅰ: ;Ⅱ:
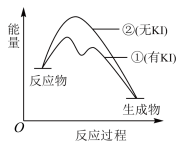
;Ⅱ: 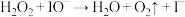 。反应过程中能量变化如图所示,下列判断正确的是
。反应过程中能量变化如图所示,下列判断正确的是
 可催化
可催化 分解,机理,Ⅰ:
分解,机理,Ⅰ: ;Ⅱ:
;Ⅱ: 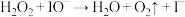 。反应过程中能量变化如图所示,下列判断正确的是
。反应过程中能量变化如图所示,下列判断正确的是
A. 是放热反应 是放热反应 | B. 分解反应的速率由机理Ⅰ决定 分解反应的速率由机理Ⅰ决定 |
C.KI能改变总反应的 | D. 不改变 不改变 分解反应的途径 分解反应的途径 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】2021年9月24日,中国科学家在国际学术期刊《科学》上发表一项重大成果:首次在实验室用二氧化碳人工合成淀粉,生物酶催化剂是这项技术的关键因素,以下说法错误的是
| A.淀粉和酶都属于有机高分子化合物 | B.使用生物酶大大提高了人工合成淀粉的速率 |
| C.催化剂能降低化学反应的反应热 | D.人工合成淀粉有利于推进“碳中和”目标的实现 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】设 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是
 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是A. 和 和 的混合气体中含有氧原子数为 的混合气体中含有氧原子数为 |
B.常温常压下,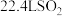 含有的分子数为 含有的分子数为 |
C.常温下, 氨水中 氨水中 浓度为 浓度为 |
D.一定条件下, 和 和 在密闭的容器中充分反应后,容器内的分子数为 在密闭的容器中充分反应后,容器内的分子数为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在一定条件下,向某密闭容器中充入2SO2+18O2⇌2SO3,以下叙述不正确的是
| A.开始反应时,正反应速率最大,逆反应速率为零 |
| B.化学反应的限度可以通过改变条件而改变 |
| C.平衡时,正反应速率与逆反应速率相等且为零 |
| D.达到平衡时,SO2、O2、SO3三者中均存在18O |
您最近一年使用:0次

 .已知反应过程中某一时刻X、Y、Z的浓度分别为
.已知反应过程中某一时刻X、Y、Z的浓度分别为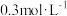 、
、 、
、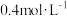 ,当反应达到平衡时,可能存在的是
,当反应达到平衡时,可能存在的是