研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
I.以下是硫元素形成物质的“价—类”二维图及含硫物质相互转化的部分信息。
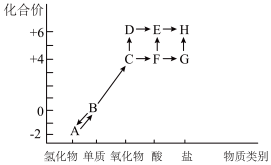
(1)G是一种由四种元素组成的钠盐,它的电离方程式是___________ 。
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的离子方程式是___________ 。
(3)检验H中阴离子的实验操作及现象是_____________ 。
(4)C→F→E是造成酸雨的可能途径,请写出其中的化学方程式___________ 。
II.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液②浓硫酸③Na2S溶液④稀硫酸⑤酸性KMnO4溶液⑥品红溶液⑦铜片
(5)实验i选择的试剂是①和___________ (填序号),证明实现转化的现象是___________ ,该转化利用了Na2SO3的___________ 性。
(6)实验ii实现了-2价S向0价S的转化,相应的离子方程式为_____________ 。
I.以下是硫元素形成物质的“价—类”二维图及含硫物质相互转化的部分信息。

(1)G是一种由四种元素组成的钠盐,它的电离方程式是
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的离子方程式是
(3)检验H中阴离子的实验操作及现象是
(4)C→F→E是造成酸雨的可能途径,请写出其中的化学方程式
II.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液②浓硫酸③Na2S溶液④稀硫酸⑤酸性KMnO4溶液⑥品红溶液⑦铜片
| 实验序号 | 预期转化 | 选择试剂(填序号) | 证明实现转化的现象 |
| i |  → → | ||
| ii | ①、③、④ | 淡黄色沉淀 | |
| iii |  → → | ②、⑦、⑥ |
(5)实验i选择的试剂是①和
(6)实验ii实现了-2价S向0价S的转化,相应的离子方程式为
22-23高一下·全国·课时练习 查看更多[3]
更新时间:2023-12-19 11:44:09
|
相似题推荐
【推荐1】有以下反应方程式,按要求回答下列问题:
A.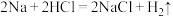
B.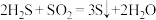
C.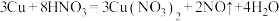
D.实验室制氯气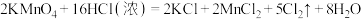
E.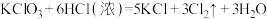
F.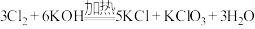
G.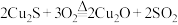
H.硫黄、硝石及木炭为黑火药成分,爆炸反应为
(1)上述有盐酸参加的反应中,盐酸体现氧化性的是______ ;有氯气生成的反应中,氯气仅做氧化产物的是______ (填代号);
(2)B反应中氧化产物与还原产物的质量比为______ ;
(3)C反应的离子方程式是____________ ;
(4)E反应中生成3个氯气分子时,转移电子的数目是______ 个;
(5)某温度时,将 通入NaOH溶液中,发生类似于F的反应,得到NaCl、NaClO、
通入NaOH溶液中,发生类似于F的反应,得到NaCl、NaClO、 混合液,经测定
混合液,经测定 与
与 物质的量之比为5:1,则参与反应的
物质的量之比为5:1,则参与反应的 与反应后溶液中
与反应后溶液中 的个数比为
的个数比为______ ;
(6)用单线桥标出G反应中电子转移的方向和数目______ ;
(7)H反应的氧化剂是______ 。
A.
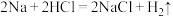
B.
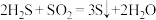
C.
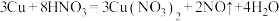
D.实验室制氯气
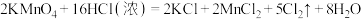
E.
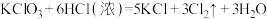
F.
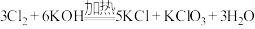
G.
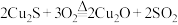
H.硫黄、硝石及木炭为黑火药成分,爆炸反应为

(1)上述有盐酸参加的反应中,盐酸体现氧化性的是
(2)B反应中氧化产物与还原产物的质量比为
(3)C反应的离子方程式是
(4)E反应中生成3个氯气分子时,转移电子的数目是
(5)某温度时,将
 通入NaOH溶液中,发生类似于F的反应,得到NaCl、NaClO、
通入NaOH溶液中,发生类似于F的反应,得到NaCl、NaClO、 混合液,经测定
混合液,经测定 与
与 物质的量之比为5:1,则参与反应的
物质的量之比为5:1,则参与反应的 与反应后溶液中
与反应后溶液中 的个数比为
的个数比为(6)用单线桥标出G反应中电子转移的方向和数目
(7)H反应的氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】黑火药爆炸时发生的反应是S+2KNO3+3C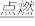 K2S+3CO2↑+N2↑,反应中的氧化剂是
K2S+3CO2↑+N2↑,反应中的氧化剂是____ ,每生成1mol CO2转移____ mol电子。分离黑火药中三种成分的方法是将黑火药溶于水,过滤,蒸发滤液得____ ;将滤纸上的物质溶于____ ,过滤,滤纸上留下的物质是___ 。
 K2S+3CO2↑+N2↑,反应中的氧化剂是
K2S+3CO2↑+N2↑,反应中的氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。
①湿法制备高铁酸钾反应体系中的氧化剂为:__________________ (填化学符号)。
②写出并配平湿法制高铁酸钾反应的离子方程式:_____________ 。每生成1 mol FeO42—转移____ mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为__ mol。
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为:____________ 。
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为___________ 。
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为:___________ 。
①湿法制备高铁酸钾反应体系中的氧化剂为:
②写出并配平湿法制高铁酸钾反应的离子方程式:
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为:
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸。请回答下列问题:
A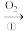 B
B C
C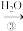 D
D
(1)①若A常温下为气体,C是红棕色气体,则C的化学式为___________ 。
②若A在常温下为黄色晶体,则C的化学式为___________ ,在D的稀溶液中滴入BaCl2溶液,产生白色沉淀,其反应的化学方程式为___________ 。
(2)工业法制硫酸中,有一步反应为SO2(g)+O2(g) 2SO3(g),一定条件下,将1molSO2和2molO2置于2L的密闭容器中,10min后测得SO2为0.4mol,则:
2SO3(g),一定条件下,将1molSO2和2molO2置于2L的密闭容器中,10min后测得SO2为0.4mol,则:
①用SO2表示该反应的速率为___________ mol/(L·min);
②其他条件不变时,将密闭容器的体积变为1L,该反应的速率将___________ (填“增大”或“减小”)
A
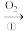 B
B C
C D
D(1)①若A常温下为气体,C是红棕色气体,则C的化学式为
②若A在常温下为黄色晶体,则C的化学式为
(2)工业法制硫酸中,有一步反应为SO2(g)+O2(g)
 2SO3(g),一定条件下,将1molSO2和2molO2置于2L的密闭容器中,10min后测得SO2为0.4mol,则:
2SO3(g),一定条件下,将1molSO2和2molO2置于2L的密闭容器中,10min后测得SO2为0.4mol,则:①用SO2表示该反应的速率为
②其他条件不变时,将密闭容器的体积变为1L,该反应的速率将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:

注:氢化物指的是由氢元素和另一种元素组成的化合物, CH4就是碳元素的一种氢化物。
(1)X的化学式为_______ 。
(2)已知SO3是一种酸性氧化物,请写出SO3与NaOH溶液反应的离子方程式为_______ 。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是_______ (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
(4)将X与Y混合,可生成硫单质。该反应的氧化剂与还原剂的个数之比为_______ 。

注:氢化物指的是由氢元素和另一种元素组成的化合物, CH4就是碳元素的一种氢化物。
(1)X的化学式为
(2)已知SO3是一种酸性氧化物,请写出SO3与NaOH溶液反应的离子方程式为
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
(4)将X与Y混合,可生成硫单质。该反应的氧化剂与还原剂的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硅、硫、氮等非金属元素在化工生产中扮演着重要角色。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1) 直接使用了硅单质的是(用序号填空)________________ ,
(2) 直接使用了二氧化硅的是(用序号填空)______________ ,
II.在学习了硫的转化后,某学生绘制了如图转化关系。
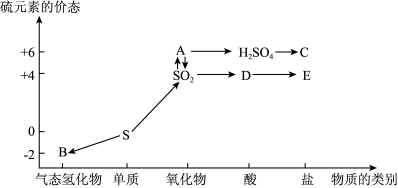
(1)写出简单气态氢化物B的结构式:______________ 。
(2)写出SO2转化为A的化学方程式:____________________________________ 。
(3)下列五种有色溶液与SO2作用均能褪色
①品红溶液 ②酸性KMnO4溶液 ③溴水 ④滴有酚酞的NaOH溶液 ⑤淀粉碘溶液
体现了SO2漂白性的是(用序号填空)____________________ 。
体现了SO2还原性的是(用序号填空)____________________ 。
写出SO2通入酸性KMnO4溶液反应的离子方程式:______________________ 。
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是__________________________________________
(5)若32.0 gCu与一定量的HNO3溶液反应,当Cu反应完时,共产生标准状况下的13.44 L气体(NO和NO2),则消耗的HNO3溶液中溶质的物质的量为________ 。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1) 直接使用了硅单质的是(用序号填空)
(2) 直接使用了二氧化硅的是(用序号填空)
II.在学习了硫的转化后,某学生绘制了如图转化关系。

(1)写出简单气态氢化物B的结构式:
(2)写出SO2转化为A的化学方程式:
(3)下列五种有色溶液与SO2作用均能褪色
①品红溶液 ②酸性KMnO4溶液 ③溴水 ④滴有酚酞的NaOH溶液 ⑤淀粉碘溶液
体现了SO2漂白性的是(用序号填空)
体现了SO2还原性的是(用序号填空)
写出SO2通入酸性KMnO4溶液反应的离子方程式:
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是
(5)若32.0 gCu与一定量的HNO3溶液反应,当Cu反应完时,共产生标准状况下的13.44 L气体(NO和NO2),则消耗的HNO3溶液中溶质的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】SO2和Cl2是中学化学中常见的气体,探究二者的制法和性质是十分重要的内容。
(1)实验室可通过铜与浓硫酸加热制SO2。请写出该反应的化学方程式_______ ,该反应中氧化剂与还原剂的物质的量之比为:_______ 。
(2)某同学用如图装置探究SO2、Cl2的化学性质。通过控制弹簧夹a、b,向X中分别通入不同气体:
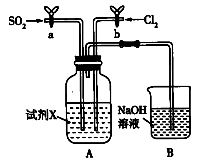
①若关闭b,打开a,X溶液为品红溶液,则X中的现象为_______ ,说明二氧化硫具有_______ 性。
②若关闭a,打开b,X溶液为紫色石蕊试液,则X中的现象为_______ 。
③若同时打开a、b,X溶液为紫色石蕊试液,同时通入体积比(同温同压)为1:1的气体,则X中的现象为_______ ,与②中现象不同的原因是_______ (用化学方程式表示)。
(1)实验室可通过铜与浓硫酸加热制SO2。请写出该反应的化学方程式
(2)某同学用如图装置探究SO2、Cl2的化学性质。通过控制弹簧夹a、b,向X中分别通入不同气体:

①若关闭b,打开a,X溶液为品红溶液,则X中的现象为
②若关闭a,打开b,X溶液为紫色石蕊试液,则X中的现象为
③若同时打开a、b,X溶液为紫色石蕊试液,同时通入体积比(同温同压)为1:1的气体,则X中的现象为
您最近一年使用:0次
【推荐3】高锰酸钾是一种强氧化剂,为紫黑色、细长的棱形结晶或颗粒,带蓝色的金属光泽,可溶于水。根据所学知识,回答下列问题:
(1)酸性条件下,高锰酸钾可与草酸( )溶液发生反应,其反应为
)溶液发生反应,其反应为 。
。
①补上产物,配平化学方程式___________ 。
②上述反应中 表现的性质有
表现的性质有___________ 。
(2)若将 通入硫酸酸化的
通入硫酸酸化的 溶液中,溶液褪色,生成
溶液中,溶液褪色,生成 ,此时溶液中仅有一种阴离子。写出发生反应的离子方程式:
,此时溶液中仅有一种阴离子。写出发生反应的离子方程式:___________ ,该反应中作还原剂的是___________ (填化学式)。
(3)高锰酸钾还可与浓盐酸反应,写出其化学方程式___________ ,其中浓盐酸表现酸性与还原性的物质的量之比为:___________ 。
(1)酸性条件下,高锰酸钾可与草酸(
 )溶液发生反应,其反应为
)溶液发生反应,其反应为 。
。①补上产物,配平化学方程式
②上述反应中
 表现的性质有
表现的性质有(2)若将
 通入硫酸酸化的
通入硫酸酸化的 溶液中,溶液褪色,生成
溶液中,溶液褪色,生成 ,此时溶液中仅有一种阴离子。写出发生反应的离子方程式:
,此时溶液中仅有一种阴离子。写出发生反应的离子方程式:(3)高锰酸钾还可与浓盐酸反应,写出其化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】新制的饱和氯水中含有多种做粒,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成。
(1)氯气能使湿润的红色布条褪色,使其褪色的微粒的化学式是__________ 。
(2)将氯水光照一段时间后,溶液颜色逐渐变浅,有关反应的化学方程式为__________ 、__________ 。
(3)新制的饱和氯水与碳酸钙的反应是制取较浓HClO 溶液 的 方 法 之一。
实验一 定性研究:

Ⅰ.如图所示,在试管中加入过量的块状碳酸钙,再加入约20 mL新制的饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去。
Ⅱ.过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强。
Ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体,
将第三份加热,观察到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
①反应后所得的溶液漂白性增强的原因是__________________________________________________ 。
②依据上述实验可推知:步骤Ⅱ的滤液中的溶质除CaCl2、HClO外,还有__________ 。
实验二 定量研究:
在仪器A内,放有塑料网包住的块状碳酸钙(过量)和150 mL新制的饱和氯水,按如图所示装置实验(实验前仪器B中充满了饱和NaHCO3溶液),待不再产生气泡后,将塑料网中剩余的碳酸钙提出液面,密封后再加热烧瓶中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。
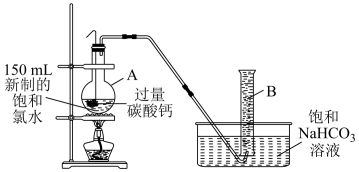
③仪器A的名称为__________ 。
④准确读出仪器B中气体体积的实验操作步骤依次是:a.等待仪器A冷却到室温;b.____________ ;c. 平视与刻度线相切的液面读数。
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL 新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为__________ 。(反应前后,溶液体积变化忽略不计)
(1)氯气能使湿润的红色布条褪色,使其褪色的微粒的化学式是
(2)将氯水光照一段时间后,溶液颜色逐渐变浅,有关反应的化学方程式为
(3)新制的饱和氯水与碳酸钙的反应是制取较浓HClO 溶液 的 方 法 之一。
实验一 定性研究:

Ⅰ.如图所示,在试管中加入过量的块状碳酸钙,再加入约20 mL新制的饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去。
Ⅱ.过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强。
Ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体,
将第三份加热,观察到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
①反应后所得的溶液漂白性增强的原因是
②依据上述实验可推知:步骤Ⅱ的滤液中的溶质除CaCl2、HClO外,还有
实验二 定量研究:
在仪器A内,放有塑料网包住的块状碳酸钙(过量)和150 mL新制的饱和氯水,按如图所示装置实验(实验前仪器B中充满了饱和NaHCO3溶液),待不再产生气泡后,将塑料网中剩余的碳酸钙提出液面,密封后再加热烧瓶中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。

③仪器A的名称为
④准确读出仪器B中气体体积的实验操作步骤依次是:a.等待仪器A冷却到室温;b.
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL 新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】C、Si是构成无机非金属材料的重要元素。
(1)Si在周期表中的位置为_____________ 。
(2)为比较C、Si的非金属性,某同学设计了如下实验:

装置①中盛放的试剂是________ ,装置②中发生反应的离子方程式是_____________ 。
(3)SiC是一种重要的高温耐磨材料。SiC中,C元素显________ (填“正”或“负”)化合价,从原子结构角度解释原因是__________________ 。
(1)Si在周期表中的位置为
(2)为比较C、Si的非金属性,某同学设计了如下实验:

装置①中盛放的试剂是
(3)SiC是一种重要的高温耐磨材料。SiC中,C元素显
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用化学变化的递变规律,常可对某些物质的化学性质作出合理的推测,请判断下列各推测是否合理(填合理、不合理或不一定合理),并说明判断的理由。
(1)从红热的铜丝能在氯气中燃烧的事实,推测红热的铁丝也能在氯气中燃烧。
(2)从铁粉和硫粉加热条件下能发生反应的事实,推测铜粉和硫粉在相同加热条件下也一定能发生反应。
(3)从SO2通入Ba(OH)2溶液能产生白色沉淀的事实,推测SO2通入BaCl2溶液也能产生白色沉淀。
(4)从反应2CO2+2Na2O2==2Na2CO3+O2的事实,推测二氧化硫也一定能发生反应:
2SO2 +2Na2O2==2Na2SO3+O2。
(1)从红热的铜丝能在氯气中燃烧的事实,推测红热的铁丝也能在氯气中燃烧。
(2)从铁粉和硫粉加热条件下能发生反应的事实,推测铜粉和硫粉在相同加热条件下也一定能发生反应。
(3)从SO2通入Ba(OH)2溶液能产生白色沉淀的事实,推测SO2通入BaCl2溶液也能产生白色沉淀。
(4)从反应2CO2+2Na2O2==2Na2CO3+O2的事实,推测二氧化硫也一定能发生反应:
2SO2 +2Na2O2==2Na2SO3+O2。
| 题号 | 是否合理 | 理 由 |
| (1) | ||
| (2) | ||
| (3) | ||
| (4) |
您最近一年使用:0次

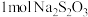 转移
转移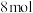 电子。该反应的离子方程式是
电子。该反应的离子方程式是

