某化学兴趣小组进行有关探究Cu、硝酸、硫酸化学性质的实验,实验过程如图所示。下列有关说法正确的是
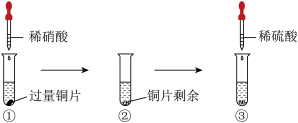

| A.①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO |
| B.③中反应的化学方程式:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O |
| C.③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强 |
| D.由上述实验可知Cu在常温下既可与稀硝酸反应,也可与稀硫酸反应 |
22-23高一下·全国·课时练习 查看更多[1]
更新时间:2023-12-20 10:32:06
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】“84”消毒液和洁厕灵是大多数家庭必备的生活用品。“84”消毒液的有效成分为次氯酸钠(NaClO,Cl为+1价),是一种高效消毒剂。洁厕灵主要成分是盐酸。若将二者混合后使用,就会对人体产生严重的危害,发生的反应如下:NaClO+2HCl=NaCl+Cl2↑+H2O,下列说法正确的是


| A.反应物盐酸只体现了还原性 |
| B.用双线桥法分析上述反应如图所示: |
| C.“84”消毒液中的NaClO在常温下比HClO稳定 |
| D.若Cl2+2Br-=2Cl-+Br2、Br2+2I-=2Br-+I2能发生,在NaBr和NaI的混合液中通入少量Cl2,一定能发生的反应是Cl2+2I-=2Cl-+I2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】常温下,在溶液中可发生以下反应:
①2Fe2++Br2=2Fe3++2Br-,
②2Br-+Cl2=Br2+2Cl-,
③2Fe3++2I-=2Fe2++I2;由此判断下列说法错误的是
①2Fe2++Br2=2Fe3++2Br-,
②2Br-+Cl2=Br2+2Cl-,
③2Fe3++2I-=2Fe2++I2;由此判断下列说法错误的是
| A.铁元素在反应①中被还原,在③中被氧化 |
| B.反应②中当有1molCl2被还原时,有2molBr-被氧化 |
| C.氧化性强弱顺序为:Cl2>I2>Br2>Fe3+ |
| D.反应2Fe2++Cl2=2Fe3++2Cl- |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】向重铬酸盐酸性溶液中加入乙醚和H2O2,水层发生反应:Cr2O +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
 +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是| A.CrO5•O(C2H5)2中存在非极性键 |
B.由水层反应可知,氧化性:H2O2>Cr2O |
| C.乙醚在检验过程中作稳定剂和萃取剂,不可用乙醇代替 |
| D.水相变为绿色的离子反应为4CrO5+12H+=4Cr3++6H2O+7O2↑ |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】高纯硝酸锶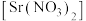 可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如图:
可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如图:
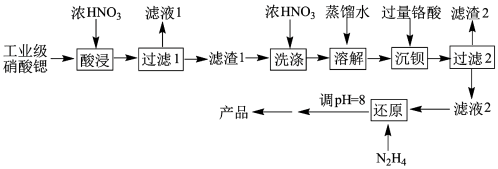
已知:①硝酸钙可溶于浓硝酸,而硝酸锶、硝酸钡不溶于浓硝酸
②铬酸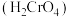 为二元弱酸
为二元弱酸
③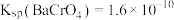
下列说法错误的是
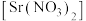 可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如图:
可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如图:
已知:①硝酸钙可溶于浓硝酸,而硝酸锶、硝酸钡不溶于浓硝酸
②铬酸
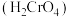 为二元弱酸
为二元弱酸③
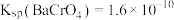
下列说法错误的是
| A.为了提高“酸浸”速率,可以采用粉碎,高温等措施 |
| B.洗涤操作所使用的玻璃仪器有:玻璃棒,漏斗,烧杯 |
C.“滤液1”的主要溶质是 ,“滤渣2”的主要成分为 ,“滤渣2”的主要成分为 |
D.“滤液2”中过量的 被 被 还原为 还原为 ,同时放出无污染的气体,发生反应的离子方程式为: ,同时放出无污染的气体,发生反应的离子方程式为: |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式书写正确的是
A.向苯酚钠溶液中通入少量二氧化碳气体 +CO2+H2O→ +CO2+H2O→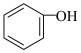 +HCO3- +HCO3- |
B.乙醛与银氨溶液的反应:CH3CHO+2Ag(NH3)2++2OH— CH3COO— +NH4++2Ag↓+3NH3+H2O CH3COO— +NH4++2Ag↓+3NH3+H2O |
| C.稀硝酸洗涤做过银镜反应的试管:Ag+2H++NO3—=Ag++NO↑+H2O |
| D.醋酸清洗水垢(主要成分为CaCO3):CaCO3+2H+=Ca2++CO2↑+H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】用以下三种途径来制取等质量的硝酸铜。
①铜与稀硝酸反应;②铜与浓硝酸反应;③铜先与氧气反应生成氧化铜,氧化铜再与硝酸反应。以下叙述不正确的是
①铜与稀硝酸反应;②铜与浓硝酸反应;③铜先与氧气反应生成氧化铜,氧化铜再与硝酸反应。以下叙述不正确的是
| A.三种途径所消耗铜的质量相等 |
| B.三种途径所消耗硝酸的物质的量是①>②>③ |
| C.途径③的制备方法最符合“绿色化学“理念 |
| D.途径①中还原剂与氧化剂的物质的量之比是3: 8 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】为了测定铜铁合金中铜的质量分数,在10.00g试样中加入200mL、0.6mol/L的稀硝酸,充分反应后剩余金属7.48g,再向其中加入50mL、0.4mol/L的稀硫酸,充分振荡后剩余金属6.60g。若硝酸的还原产物只有NO,下列说法正确的是
| A.上述测定不能达到实验目的 | B.剩余的7.48g金属为铜 |
| C.共生成NO气体 0.04mol | D.该合金中铜的质量分数为69.2% |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列实验操作、现象和所得结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将Cu(NO3)2加热产生的气体集满试管并倒扣到水槽中 | 红棕色气体消失,水充满试管 | 红棕色气体中n(NO2)与n(O2)之比为1:4 |
| B | 将Cl2和H2S气体在集气瓶中混合 | 瓶壁上出现黄色固体 | Cl2的氧化性比S强 |
| C | 向含有少量铜粉的Cu(NO3)2溶液中滴入稀硫酸 | 铜粉逐渐溶解 | 稀硫酸能与铜单质反应 |
| D | 向久置的Na2SO3溶液中加入足量BaCl2溶液;再加入足量稀盐酸 | 先出现白色沉淀,后部分沉淀溶解 | 久置的Na2SO3部分被氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】如图将氢气在空气中点燃后,迅速在冰块上降温,生成的物质进入烧杯后使得烧杯中的酸性KMnO4溶液颜色变浅甚至褪色。若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈血红色。判断下列说法中正确的是


| A.该条件下H2燃烧的产物中可能含有一定量的H2O2 |
| B.该实验说明相同的物质在不同条件下反应产物可能不一样 |
| C.含KSCN的FeSO4溶液变红可能是Fe2+被KMnO4溶液氧化导致的 |
| D.将烧杯中溶液换成KI-淀粉溶液也能验证生成物具有还原性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关实验存在不合理的装置是


| A.装置甲:用CCl4萃取碘水中的碘 |
| B.装置乙:加热碘的CCl4溶液,分离碘并回收CCl4 |
| C.装置丙:验证硫酸、碳酸、苯酚溶液的酸性 |
| D.用乙酸、乙醇制取乙酸乙酯 |
您最近一年使用:0次



