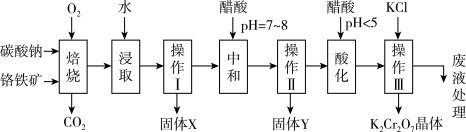
碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1)I2的一种制备方法如下图所示:
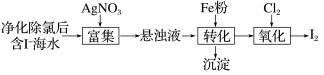
①加入Fe粉进行转化反应是一个置换反应,该反应的化学方程式为___________ ,生成的沉淀与硝酸反应,生成___________ 后可循环使用。
②通入Cl2的过程中,若氧化产物只有一种,反应的的离子方程式为___________ ;当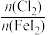 >1.5后,单质碘的收率会降低,原因是
>1.5后,单质碘的收率会降低,原因是___________ 。
(2)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为___________ mol。I2在KI溶液中可发生反应:I2+I- 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是___________ 。
(1)I2的一种制备方法如下图所示:

①加入Fe粉进行转化反应是一个置换反应,该反应的化学方程式为
②通入Cl2的过程中,若氧化产物只有一种,反应的的离子方程式为
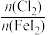 >1.5后,单质碘的收率会降低,原因是
>1.5后,单质碘的收率会降低,原因是(2)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为
 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
更新时间:2023-12-28 16:24:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A为常见的金属单质,根据下图所示的关系:
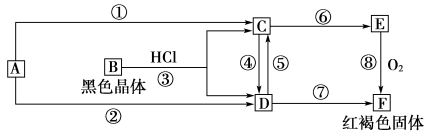
(1)确定A、B、C、D、E、F的化学式,A为________ ,B为________ ,C为________ ,D为________ ,E为________ ,F为________ 。
(2)写出①⑧的化学方程式,④、⑤的离子方程式。
①_________________________________________________ ,
⑧_________________________________________________ ,
④________________________________________________ ,
⑤___________________________________________________ 。

(1)确定A、B、C、D、E、F的化学式,A为
(2)写出①⑧的化学方程式,④、⑤的离子方程式。
①
⑧
④
⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】 、
、 、
、 、
、 、
、 、
、 、
、 和甲、乙、丙是中学化学常见物质,其中
和甲、乙、丙是中学化学常见物质,其中 、
、 、
、 为金属单质,甲、乙、丙为三种气体。它们之间能发生如下反应(部分反应的产物和反应条件未标出)。
为金属单质,甲、乙、丙为三种气体。它们之间能发生如下反应(部分反应的产物和反应条件未标出)。
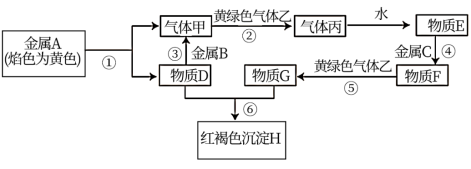
请根据以上信息回答下列问题:
(1)在反应①~⑥中,不属于氧化还原反应的是_______ (填编号),反应①中每消耗 金属
金属 时转移电子
时转移电子_______  。
。
(2)写出反应③的离子方程式:_______ 。
(3)写出反应⑤的离子方程式:_______ ;检验 溶液中阳离子的方法为:
溶液中阳离子的方法为:_______ 。
(4)向 溶液中加入
溶液中加入 溶液后的现象为
溶液后的现象为_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和甲、乙、丙是中学化学常见物质,其中
和甲、乙、丙是中学化学常见物质,其中 、
、 、
、 为金属单质,甲、乙、丙为三种气体。它们之间能发生如下反应(部分反应的产物和反应条件未标出)。
为金属单质,甲、乙、丙为三种气体。它们之间能发生如下反应(部分反应的产物和反应条件未标出)。
请根据以上信息回答下列问题:
(1)在反应①~⑥中,不属于氧化还原反应的是
 金属
金属 时转移电子
时转移电子 。
。(2)写出反应③的离子方程式:
(3)写出反应⑤的离子方程式:
 溶液中阳离子的方法为:
溶液中阳离子的方法为:(4)向
 溶液中加入
溶液中加入 溶液后的现象为
溶液后的现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯气是一种重要的工业原料。如图是一套制取并验证氯气部分化学性质的实验装置。
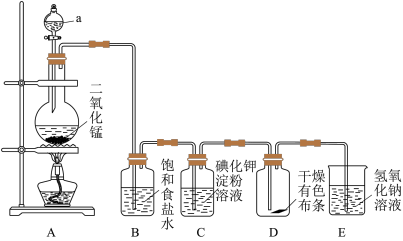
(1)写出实验室制取氯气反应的化学方程式_______ 。
(2)装置B的作用是_______ 。
(3)当有少量Cl2通过后,观察到装置C中溶液变成_______ 色。
(4)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?_______ 。
(5)若要证明Cl2无漂白性,则必须在装置D之前加一个装有_______ 的洗气瓶。
(6)装置E的作用是_______ ,该反应的离子方程式为_______ 。

(1)写出实验室制取氯气反应的化学方程式
(2)装置B的作用是
(3)当有少量Cl2通过后,观察到装置C中溶液变成
(4)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?
(5)若要证明Cl2无漂白性,则必须在装置D之前加一个装有
(6)装置E的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某澄清透明的溶液中可能有Fe2+、Fe3+、Al3+、Ba2+、SO42-、HCO3-、NO3-、Cl-等离子,对其进行下述实验:
(A)该溶液能使紫色石蕊试液变红;
(B)另取少量溶液浓缩后加入铜片和浓硫酸共热,可看到有红棕色的NO2气体生成;
(C)另取少量溶液加入氯化钡溶液,产生不溶于稀硝酸的白色沉淀,并过滤;
(D)在(C)所得滤液中加入硝酸银溶液,也产生不溶于稀硝酸的白色沉淀;
(E)另取滤液,逐滴加入氢氧化钠溶液至过量,开始时沉淀逐渐增加,随后沉淀部分溶解,最后仍然有固体残留;根据此实验现象,判断:
(1)溶液中肯定存在的离子有_____________ 。(2)溶液中肯定不存在的离子是___________ 。
(A)该溶液能使紫色石蕊试液变红;
(B)另取少量溶液浓缩后加入铜片和浓硫酸共热,可看到有红棕色的NO2气体生成;
(C)另取少量溶液加入氯化钡溶液,产生不溶于稀硝酸的白色沉淀,并过滤;
(D)在(C)所得滤液中加入硝酸银溶液,也产生不溶于稀硝酸的白色沉淀;
(E)另取滤液,逐滴加入氢氧化钠溶液至过量,开始时沉淀逐渐增加,随后沉淀部分溶解,最后仍然有固体残留;根据此实验现象,判断:
(1)溶液中肯定存在的离子有
您最近一年使用:0次
【推荐2】一、某同学欲探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铁、铜反应的实验中的有关问题。
(1)在常温下,分别向盛有等量铁片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能观察到发生明显反应的是__________ (填序号,下同),无明显现象的是____________
(2)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能观察到随即发生剧烈反应的是______ ;能缓慢发生反应的是______ ,反应的离子方程式为:___________________________ ;开始不反应,加热后发生反应的是______ ;加热也不发生反应的是______ 。
先将铜与浓硫酸反应产生的气体X持续通入如图装置中,一段时间后再将铜与浓硝酸反应产生的大量气体Y也持续通入该装置中,可观察到的现象包括______ 。
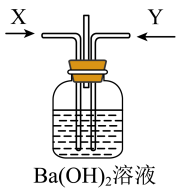
a.通入X气体后先产生白色沉淀后溶解 b.通入X气体后溶液中无明显现象
c.通入Y气体后有沉淀产生 d.通入Y气体后沉淀溶解
e.通入Y气体后溶液中无明显现象
二、从物质X出发有如下图所示的一系列变化。已知X为酸式盐,A、C为无色气体,反应的某些产物已经略去。
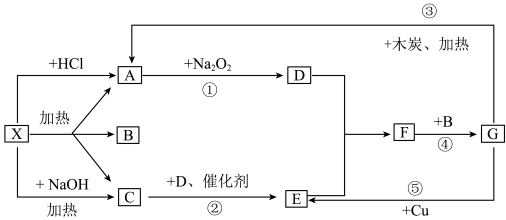
(1)写出下列物质的化学式:X:_______________________ ;G:____________________ 。
(2)写出反应②的化学方程式:____________________________________________ 。
(3)向X的溶液中加入过量的NaOH溶液,并加热,写出该反应的离子方程式:_______________ 。
(4)反应④中氧化剂与还原剂的质量之比为_______________ 。
(1)在常温下,分别向盛有等量铁片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能观察到发生明显反应的是
(2)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能观察到随即发生剧烈反应的是
先将铜与浓硫酸反应产生的气体X持续通入如图装置中,一段时间后再将铜与浓硝酸反应产生的大量气体Y也持续通入该装置中,可观察到的现象包括

a.通入X气体后先产生白色沉淀后溶解 b.通入X气体后溶液中无明显现象
c.通入Y气体后有沉淀产生 d.通入Y气体后沉淀溶解
e.通入Y气体后溶液中无明显现象
二、从物质X出发有如下图所示的一系列变化。已知X为酸式盐,A、C为无色气体,反应的某些产物已经略去。

(1)写出下列物质的化学式:X:
(2)写出反应②的化学方程式:
(3)向X的溶液中加入过量的NaOH溶液,并加热,写出该反应的离子方程式:
(4)反应④中氧化剂与还原剂的质量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:_______
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。
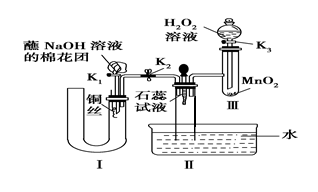
①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至____ 后,迅速关闭K1,观察到U形管内的现象是______ 。
②装置Ⅲ中发生反应的化学方程式为__________ 。
③蘸NaOH溶液的棉花团的作用是____________ 。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,关闭K2、K3,长玻璃管中并未充满液体。设计简单方法检验长玻璃管中的气体是否含NO______ 。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。

①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至
②装置Ⅲ中发生反应的化学方程式为
③蘸NaOH溶液的棉花团的作用是
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,关闭K2、K3,长玻璃管中并未充满液体。设计简单方法检验长玻璃管中的气体是否含NO
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。

(1)若加入的试剂①为NaOH溶液,加入试剂①的目的___________________ 。
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为烧杯、玻璃棒、_______ 。
(3)写出溶液C中加入试剂③发生反应的离子方程式为_______ 。
(4)写出固体E中加入试剂④发生反应的离子反应方程式为______________ 。
(5)从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为蒸发浓缩、______ 、过滤、洗涤、干燥。

(1)若加入的试剂①为NaOH溶液,加入试剂①的目的
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为烧杯、玻璃棒、
(3)写出溶液C中加入试剂③发生反应的离子方程式为
(4)写出固体E中加入试剂④发生反应的离子反应方程式为
(5)从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为蒸发浓缩、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要
成分是Al2O3和Fe2O3)和焦炭制备,流程如下:
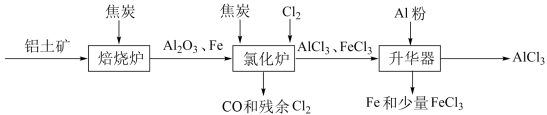
已知:AlCl3、FeCl3 分别在183℃、315℃时升华
(1)Cl2的电子式______________ 。
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为_____________ ;炉气中残余的少量Cl2,可用NaOH溶液吸收,其离子方程式为_____________ 。
(3)700℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围______ 。
a. 低于183℃ b. 介于183℃和315℃之间 c. 高于315℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。

计算该样品中AlCl3的质量分数_________ (结果用m、n表示,不必化简)。
成分是Al2O3和Fe2O3)和焦炭制备,流程如下:

已知:AlCl3、FeCl3 分别在183℃、315℃时升华
(1)Cl2的电子式
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为
(3)700℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围
a. 低于183℃ b. 介于183℃和315℃之间 c. 高于315℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。

计算该样品中AlCl3的质量分数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】碘是一种紫黑色固体,微溶于水,其单质及化合物被广泛用于医药、染料等方面。一种以海水为原料制备确单质的方法如下图所示:
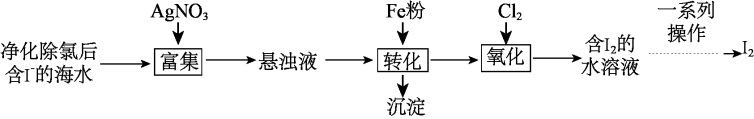
请回答下列问题:
(1)将海水中的 “富集”得到悬浊液,有关反应的离子方程式是
“富集”得到悬浊液,有关反应的离子方程式是_______ 。
(2)“转化”时用铁粉而不用铁片的原因是_______ 。
(3) 进入“氧化”环节,通过控制
进入“氧化”环节,通过控制 的用量生成
的用量生成 ,此反应的化学方程式是
,此反应的化学方程式是_______ ,反应中的氧化剂是_______ 。
(4)欲判断经一系列处理后的水溶液中是否含有 ,应进行的操作是
,应进行的操作是_______ 。

请回答下列问题:
(1)将海水中的
 “富集”得到悬浊液,有关反应的离子方程式是
“富集”得到悬浊液,有关反应的离子方程式是(2)“转化”时用铁粉而不用铁片的原因是
(3)
 进入“氧化”环节,通过控制
进入“氧化”环节,通过控制 的用量生成
的用量生成 ,此反应的化学方程式是
,此反应的化学方程式是(4)欲判断经一系列处理后的水溶液中是否含有
 ,应进行的操作是
,应进行的操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海洋是巨大的资源宝库,可以制取多种物质。
Ⅰ.海水提溴
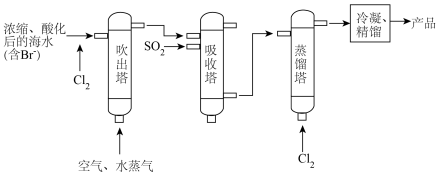
(1)该工艺流程中两次通入氯气的目的是______ 。
(2)请写出吸收塔中反应的离子方程式______ 。
(3)吹出塔中采用气-液逆流的方式(液体从顶喷淋,气体从塔底进入),其目的是______ 。
Ⅱ.提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如图:
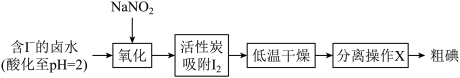
已知:pH=2时,Ⅰ.NaNO2溶液只能将I-氧化为I2,同时生成NO
Ⅱ.2MnO +I2+4H+=2IO
+I2+4H+=2IO +2Mn2++2H2O
+2Mn2++2H2O
(4)氧化过程的离子方程式为______ 。
(5)根据I2的特性,分离操作X为______ ,冷凝得到粗碘。
(6)酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2,原因是______ 。
(7)活性炭上吸附的I2还能用浓Na2CO3溶液吸收,每吸收3molI2转移5mol电子,该反应的离子方程式是______ 。
Ⅰ.海水提溴

(1)该工艺流程中两次通入氯气的目的是
(2)请写出吸收塔中反应的离子方程式
(3)吹出塔中采用气-液逆流的方式(液体从顶喷淋,气体从塔底进入),其目的是
Ⅱ.提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如图:

已知:pH=2时,Ⅰ.NaNO2溶液只能将I-氧化为I2,同时生成NO
Ⅱ.2MnO
 +I2+4H+=2IO
+I2+4H+=2IO +2Mn2++2H2O
+2Mn2++2H2O(4)氧化过程的离子方程式为
(5)根据I2的特性,分离操作X为
(6)酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2,原因是
(7)活性炭上吸附的I2还能用浓Na2CO3溶液吸收,每吸收3molI2转移5mol电子,该反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。
I.提取粗盐后的母液中含较高浓度的溴元素。某课外兴趣小组先将母液中的溴元素氧化成Br2,再获取液溴,流程如下:___________ 。萃取后静置,进行___________ (填操作名称),可得到溴的有机溶液。
(2)“反萃取”时,Br2与Na2CO3溶液反应生成NaBrO3与NaBr。该反应生成的BrO 与Br-物质的量之比为
与Br-物质的量之比为___________ 。
II.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:___________ (填字母)。
a.泥三角 b.坩埚 c.漏斗 d.250ml容量瓶 e.酒精灯
(4)步骤③的操作名称是___________ 。
(5)步骤④中反应的离子方程式为___________ 。
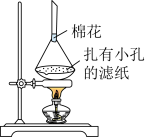
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。___________ ;棉花的作用是___________ 。
I.提取粗盐后的母液中含较高浓度的溴元素。某课外兴趣小组先将母液中的溴元素氧化成Br2,再获取液溴,流程如下:
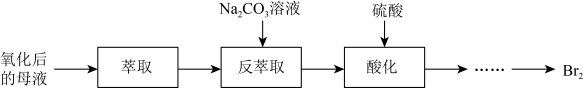
(2)“反萃取”时,Br2与Na2CO3溶液反应生成NaBrO3与NaBr。该反应生成的BrO
 与Br-物质的量之比为
与Br-物质的量之比为II.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
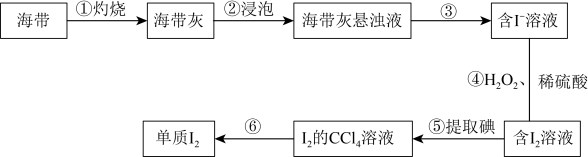
a.泥三角 b.坩埚 c.漏斗 d.250ml容量瓶 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。
您最近一年使用:0次