氨是化肥工业和基本有机化工的主要原料,合成氨的反应如下: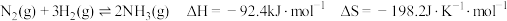
(1)判断合成氨的反应在_________ (选填“高温、低温”)能自发进行,推动反应在该条件下自发进行的主要因素是反应的_________ (选填“焓变、熵变”)。
(2)不同条件下,分别测得上述反应的反应速率,其中表示该反应进行得最快的是_______ 。
a.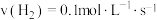 b.
b.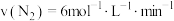
c.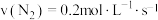 d.
d.
(3)一定温度下,向 密闭容器中加入
密闭容器中加入 和
和 ,发生上述反应,
,发生上述反应, 物质的量随时间的变化如下图所示。
物质的量随时间的变化如下图所示。
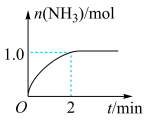
 内的平均反应速率
内的平均反应速率
________________ 。
根据反应条件,判断 内
内 变化趋势为
变化趋势为______ ,运用有效碰撞理论来解释该变化趋势:_______ 。
(4)在合成氨的实际生产过程中,常常加入含铁催化剂.请结合过渡态理论解释使用催化剂使反应速率加快的原因_______ 。
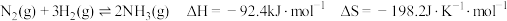
(1)判断合成氨的反应在
(2)不同条件下,分别测得上述反应的反应速率,其中表示该反应进行得最快的是
a.
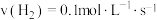 b.
b.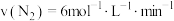
c.
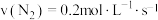 d.
d.
(3)一定温度下,向
 密闭容器中加入
密闭容器中加入 和
和 ,发生上述反应,
,发生上述反应, 物质的量随时间的变化如下图所示。
物质的量随时间的变化如下图所示。
 内的平均反应速率
内的平均反应速率
根据反应条件,判断
 内
内 变化趋势为
变化趋势为(4)在合成氨的实际生产过程中,常常加入含铁催化剂.请结合过渡态理论解释使用催化剂使反应速率加快的原因
更新时间:2023-12-29 16:36:23
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
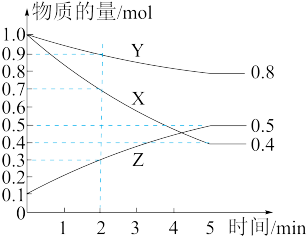
(1)该反应的化学方程式是_______ ;
(2)2min内Y的转化率为_______ ;
(3)5min内用X表示的化学反应速率为_______ ;
(4)该反应达到平衡状态的标志是_______ (填字母)。
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1 Y的同时消耗2
Y的同时消耗2 Z
Z
Ⅱ.在恒温、体积为1.0L的密闭容器中通入1.0
 和x
和x
 发生如下反应
发生如下反应 ,20min后达到平衡,测得反应放出的热量为18.4
,20min后达到平衡,测得反应放出的热量为18.4 ,混合气体的物质的量为1.6
,混合气体的物质的量为1.6 ,容器内的压强变为原来的80%,请回答下列问题∶
,容器内的压强变为原来的80%,请回答下列问题∶
(5)20min内,
_______ 。
(6)该反应的热化学方程式为_______ 。
(7)下列叙述中能表示该反应达到平衡状态的是_______ (填序号)。
① 体积分数保持不变 ②混合气体的密度不再改变
体积分数保持不变 ②混合气体的密度不再改变
③单位时间断裂0.3
 键,同时生成0.6
键,同时生成0.6
 键
键
④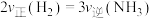 ⑤混合气体的平均摩尔质量不再改变
⑤混合气体的平均摩尔质量不再改变

(1)该反应的化学方程式是
(2)2min内Y的转化率为
(3)5min内用X表示的化学反应速率为
(4)该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1
 Y的同时消耗2
Y的同时消耗2 Z
ZⅡ.在恒温、体积为1.0L的密闭容器中通入1.0

 和x
和x
 发生如下反应
发生如下反应 ,20min后达到平衡,测得反应放出的热量为18.4
,20min后达到平衡,测得反应放出的热量为18.4 ,混合气体的物质的量为1.6
,混合气体的物质的量为1.6 ,容器内的压强变为原来的80%,请回答下列问题∶
,容器内的压强变为原来的80%,请回答下列问题∶(5)20min内,

(6)该反应的热化学方程式为
(7)下列叙述中能表示该反应达到平衡状态的是
①
 体积分数保持不变 ②混合气体的密度不再改变
体积分数保持不变 ②混合气体的密度不再改变③单位时间断裂0.3

 键,同时生成0.6
键,同时生成0.6
 键
键④
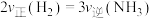 ⑤混合气体的平均摩尔质量不再改变
⑤混合气体的平均摩尔质量不再改变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.恒温下在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如下图。
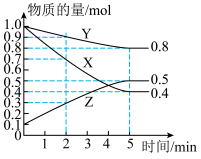
(1)该反应的化学方程式为___________ ;
(2)从开始至5min,Y的平均反应速率为___________ ;平衡时,Z的物质的量浓度为___________ ,X的转化率为___________ 。
(3)反应达平衡时体系的压强是开始时的___________ 倍;
(4)下列描述中能表明反应已达到平衡状态的是___________ 。(填序号)
①容器内温度不变
②混合气体的密度不变
③混合气体的压强不变
④混合气体的平均相对分子质量不变
⑤Z(g)的物质的量浓度不变
⑥容器内X、Y、Z三种气体的浓度之比为3∶1∶2
⑦某时刻 且不等于零
且不等于零
⑧单位时间内生成2n molZ,同时生成3n molX
Ⅱ.利用反应 可得到清洁能源
可得到清洁能源 。
。
(5)该反应化学平衡常数表达式
___________ 。
(6)该反应的平衡常数随温度的变化如表:
从上表可以推断:此反应是___________ (填“吸热”或“放热”)反应。
(7)830℃时,向容积为2L的密闭容器中充入1 mol CO与1 mol ,2 min时CO为0.6mol。2min内
,2 min时CO为0.6mol。2min内
___________ ,此时反应进行的方向是___________ 。

(1)该反应的化学方程式为
(2)从开始至5min,Y的平均反应速率为
(3)反应达平衡时体系的压强是开始时的
(4)下列描述中能表明反应已达到平衡状态的是
①容器内温度不变
②混合气体的密度不变
③混合气体的压强不变
④混合气体的平均相对分子质量不变
⑤Z(g)的物质的量浓度不变
⑥容器内X、Y、Z三种气体的浓度之比为3∶1∶2
⑦某时刻
 且不等于零
且不等于零⑧单位时间内生成2n molZ,同时生成3n molX
Ⅱ.利用反应
 可得到清洁能源
可得到清洁能源 。
。(5)该反应化学平衡常数表达式

(6)该反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(7)830℃时,向容积为2L的密闭容器中充入1 mol CO与1 mol
 ,2 min时CO为0.6mol。2min内
,2 min时CO为0.6mol。2min内
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】某温度下,2L的密闭容器中投入一定量的A、B,发生反应 ,两种气体的物质的量浓度随时间变化的曲线如图所示:
,两种气体的物质的量浓度随时间变化的曲线如图所示:

(1)4s时C的浓度为0.2mol/L,则该反应的化学方程式中c的值为_______
(2)并计算A气体的平衡转化率(达到平衡状态时转化的A的物质的量与A的起始物质的量的比值)
_______
(3)试计算平衡时气体C的物质的量n(C)=_______
(4)假设起始时反应体系的压强为p0,反应体系的体积保持不变,则反应达到平衡时反应体系的压强p=_______ (用含有p0的式子表示)
(5)下列描述能说明上述反应已达平衡状态的是_______(填序号)
(6)若将上述反应在恒容绝热容器中进行,已知开始阶段随着反应的进行化学反应速率逐渐增大。试判断反应物总能量E反与生成物总能量E生的相对大小关系并说明理由_______
(7)假设用 表示物质X在
表示物质X在 时间段内的平均反应速率,试比较
时间段内的平均反应速率,试比较 ,
, ,
,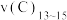 大小关系并排序
大小关系并排序_______
 ,两种气体的物质的量浓度随时间变化的曲线如图所示:
,两种气体的物质的量浓度随时间变化的曲线如图所示:
(1)4s时C的浓度为0.2mol/L,则该反应的化学方程式中c的值为
(2)并计算A气体的平衡转化率(达到平衡状态时转化的A的物质的量与A的起始物质的量的比值)

(3)试计算平衡时气体C的物质的量n(C)=
(4)假设起始时反应体系的压强为p0,反应体系的体积保持不变,则反应达到平衡时反应体系的压强p=
(5)下列描述能说明上述反应已达平衡状态的是_______(填序号)
| A.单位时间内生成cmolC的同时,生成1molB |
| B.反应体系的压强不再改变 |
C.气体A的物质的量浓度不再变化,即 |
| D.反应体系中气体的密度不再变化 |
(7)假设用
 表示物质X在
表示物质X在 时间段内的平均反应速率,试比较
时间段内的平均反应速率,试比较 ,
, ,
,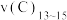 大小关系并排序
大小关系并排序
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】CO的处理、回收利用是环境科学研究的热点课题。请回答下列问题:
(1)CO用于处理大气污染物 过程的能量变化情况如图甲。
过程的能量变化情况如图甲。

写出反应 的热化学方程式:
的热化学方程式:_______ 。
(2)某研究团队采用B3LYP/ce-pVTZ理论水平系统研究了 催化
催化 的二重态反应势能面示意图(如图乙,图中将反应物的总能量设为零点能量;IM表示中间体,TS表示过渡态)。
的二重态反应势能面示意图(如图乙,图中将反应物的总能量设为零点能量;IM表示中间体,TS表示过渡态)。
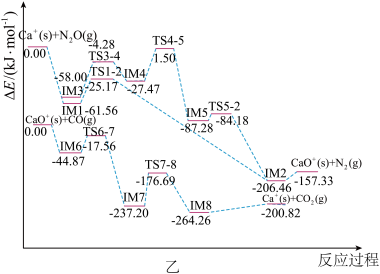
①由图乙可知, 和
和 反应的过程中,比较有利的途径为
反应的过程中,比较有利的途径为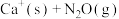 →
→_______ →IM2→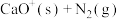 ,
,

_______  。
。
②由图乙可知, 和CO反应的过程中,正反应中活化能较大的一步的活化能为
和CO反应的过程中,正反应中活化能较大的一步的活化能为_______  。
。
(3)已知: 的速率方程为
的速率方程为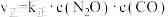 ,
,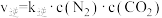 ,
, 、
、 分别是反应速率常数,只与温度有关。向容积为1L的某恒容密闭容器中,起始充入
分别是反应速率常数,只与温度有关。向容积为1L的某恒容密闭容器中,起始充入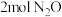 和2mol CO,保持温度为T℃不变,20min后反应达到平衡,此时CO的转化率为60%,则0~20min内,
和2mol CO,保持温度为T℃不变,20min后反应达到平衡,此时CO的转化率为60%,则0~20min内,
_______  ,当CO的转化率为25%时,
,当CO的转化率为25%时,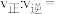
_______ 。
(4)在总压为100kPa的恒容密闭容器中,充入一定量的 和
和 发生反应
发生反应 ,在不同条件下达到平衡。
,在不同条件下达到平衡。 时
时 的平衡转化率与
的平衡转化率与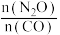 的变化曲线和
的变化曲线和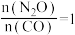 时
时 的平衡转化率与
的平衡转化率与 的变化曲线如图丙所示。
的变化曲线如图丙所示。
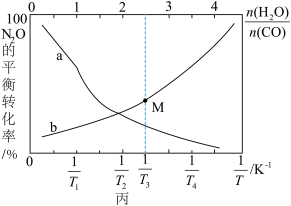
①
_______ (填“>”或“<”) ,表示
,表示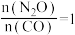 时,
时, 的平衡转化率与
的平衡转化率与 的变化曲线为
的变化曲线为_______ (填“a”或“b”)曲线。
②已知:该反应的标准平衡常数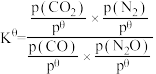 ,其中
,其中 为标准压强 (
为标准压强 (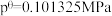 ),
),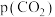 、
、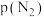 、
、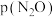 、
、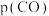 为各组分的平衡分压,M点时
为各组分的平衡分压,M点时 的平衡转化率为40%,则M点对应温度下该反应的标准平衡常数
的平衡转化率为40%,则M点对应温度下该反应的标准平衡常数
_______ (计算结果保留两位有效数字, 物质的量分数)。
物质的量分数)。
(1)CO用于处理大气污染物
 过程的能量变化情况如图甲。
过程的能量变化情况如图甲。
写出反应
 的热化学方程式:
的热化学方程式:(2)某研究团队采用B3LYP/ce-pVTZ理论水平系统研究了
 催化
催化 的二重态反应势能面示意图(如图乙,图中将反应物的总能量设为零点能量;IM表示中间体,TS表示过渡态)。
的二重态反应势能面示意图(如图乙,图中将反应物的总能量设为零点能量;IM表示中间体,TS表示过渡态)。
①由图乙可知,
 和
和 反应的过程中,比较有利的途径为
反应的过程中,比较有利的途径为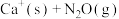 →
→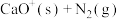 ,
,

 。
。②由图乙可知,
 和CO反应的过程中,正反应中活化能较大的一步的活化能为
和CO反应的过程中,正反应中活化能较大的一步的活化能为 。
。(3)已知:
 的速率方程为
的速率方程为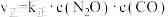 ,
,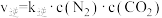 ,
, 、
、 分别是反应速率常数,只与温度有关。向容积为1L的某恒容密闭容器中,起始充入
分别是反应速率常数,只与温度有关。向容积为1L的某恒容密闭容器中,起始充入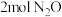 和2mol CO,保持温度为T℃不变,20min后反应达到平衡,此时CO的转化率为60%,则0~20min内,
和2mol CO,保持温度为T℃不变,20min后反应达到平衡,此时CO的转化率为60%,则0~20min内,
 ,当CO的转化率为25%时,
,当CO的转化率为25%时,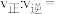
(4)在总压为100kPa的恒容密闭容器中,充入一定量的
 和
和 发生反应
发生反应 ,在不同条件下达到平衡。
,在不同条件下达到平衡。 时
时 的平衡转化率与
的平衡转化率与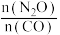 的变化曲线和
的变化曲线和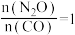 时
时 的平衡转化率与
的平衡转化率与 的变化曲线如图丙所示。
的变化曲线如图丙所示。
①

 ,表示
,表示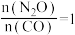 时,
时, 的平衡转化率与
的平衡转化率与 的变化曲线为
的变化曲线为②已知:该反应的标准平衡常数
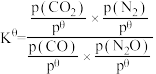 ,其中
,其中 为标准压强 (
为标准压强 (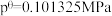 ),
),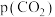 、
、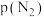 、
、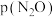 、
、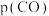 为各组分的平衡分压,M点时
为各组分的平衡分压,M点时 的平衡转化率为40%,则M点对应温度下该反应的标准平衡常数
的平衡转化率为40%,则M点对应温度下该反应的标准平衡常数
 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】习近平主席在第75届联合国大会提出,我国要在2030年前实现碳达峰,2060年前实现碳中和的目标。因此二氧化碳的固定和转化成为科学家研究的重要课题。在适当的条件下, 可发生以下两个反应:
可发生以下两个反应:
反应①: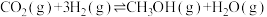
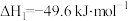
反应②: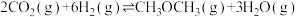
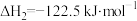
(1)反应①的活化能Ea(正)_______ Ea(逆)(填“>”“<”或“=”)。
(2)已知反应①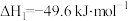 ,在
,在_______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)反应①在起始物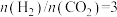 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x( ),在t=250℃时,x(
),在t=250℃时,x( )随压强(p)的变化及在p=5×103Pa时x(
)随压强(p)的变化及在p=5×103Pa时x( )随温度(t)的变化,如图所示。
)随温度(t)的变化,如图所示。

①上图中表示在恒压条件下进行反应的曲线是_______ (填“a”或“b”)。
②t=250℃时,改变压强达到平衡时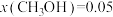 ,
, 的平衡转化率α=
的平衡转化率α=_______ %(保留三位有效数字)
(4)一定温度下,在某一恒容密闭容器中充入一定量的 和
和 ,进行反应
,进行反应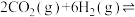
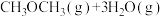 。下列能说明该反应已达到平衡状态的是
。下列能说明该反应已达到平衡状态的是_______ (填序号)。
A.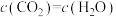
B.气体的平均相对分子量不再随时间变化而改变
C.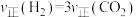
D.K不变
E.单位时间内每形成3mol H-H键,同时形成3mol O-H键
(5)在T温度下,将3.5mol 和10mol
和10mol  充入2L的恒容密闭容器中发生反应①和②,达到平衡状态时
充入2L的恒容密闭容器中发生反应①和②,达到平衡状态时 (g)和
(g)和 (g)的物质的量分别为2mol和0.5mol。则T温度时反应①的平衡常数K为
(g)的物质的量分别为2mol和0.5mol。则T温度时反应①的平衡常数K为_______ 。
(6)向2L密闭容器中充入1mol 和3mol
和3mol  ,在一定条件下,发生反应:
,在一定条件下,发生反应: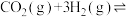
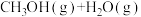 △H<0。
△H<0。 的浓度随时间(0~
的浓度随时间(0~ )变化如图所示。其他条件不变,在
)变化如图所示。其他条件不变,在 时间将容器体积缩小至原来的一半,
时间将容器体积缩小至原来的一半,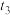 时重新达到平衡。请画出
时重新达到平衡。请画出 ~
~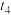 时段内
时段内 浓度的变化曲线
浓度的变化曲线_______ 。(在答题卷对应区域作图)

 可发生以下两个反应:
可发生以下两个反应:反应①:
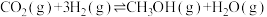
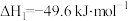
反应②:
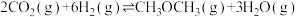
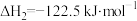
(1)反应①的活化能Ea(正)
(2)已知反应①
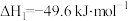 ,在
,在(3)反应①在起始物
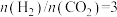 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x( ),在t=250℃时,x(
),在t=250℃时,x( )随压强(p)的变化及在p=5×103Pa时x(
)随压强(p)的变化及在p=5×103Pa时x( )随温度(t)的变化,如图所示。
)随温度(t)的变化,如图所示。
①上图中表示在恒压条件下进行反应的曲线是
②t=250℃时,改变压强达到平衡时
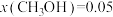 ,
, 的平衡转化率α=
的平衡转化率α=(4)一定温度下,在某一恒容密闭容器中充入一定量的
 和
和 ,进行反应
,进行反应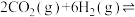
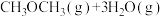 。下列能说明该反应已达到平衡状态的是
。下列能说明该反应已达到平衡状态的是A.
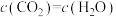
B.气体的平均相对分子量不再随时间变化而改变
C.
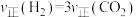
D.K不变
E.单位时间内每形成3mol H-H键,同时形成3mol O-H键
(5)在T温度下,将3.5mol
 和10mol
和10mol  充入2L的恒容密闭容器中发生反应①和②,达到平衡状态时
充入2L的恒容密闭容器中发生反应①和②,达到平衡状态时 (g)和
(g)和 (g)的物质的量分别为2mol和0.5mol。则T温度时反应①的平衡常数K为
(g)的物质的量分别为2mol和0.5mol。则T温度时反应①的平衡常数K为(6)向2L密闭容器中充入1mol
 和3mol
和3mol  ,在一定条件下,发生反应:
,在一定条件下,发生反应: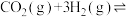
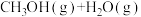 △H<0。
△H<0。 的浓度随时间(0~
的浓度随时间(0~ )变化如图所示。其他条件不变,在
)变化如图所示。其他条件不变,在 时间将容器体积缩小至原来的一半,
时间将容器体积缩小至原来的一半,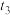 时重新达到平衡。请画出
时重新达到平衡。请画出 ~
~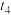 时段内
时段内 浓度的变化曲线
浓度的变化曲线
您最近一年使用:0次
【推荐3】氨元素和硫元素存在多种氧化物。回答下列问题:
(1)部分氮氧化合物之间的转化所发生的化学反应如下:
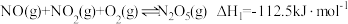
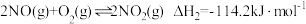
则反应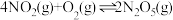 的
的
_______  。
。
(2)已知 的反应历程分两步:
的反应历程分两步:
第一步: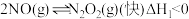 ;
; ;
;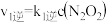
第二步: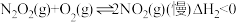 ;
;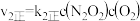 ;
;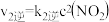
 的反应速率主要是由
的反应速率主要是由_______ (填“第一步”或“第二步”)反应决定,该反应的平衡常数K=_______ (用k表示)。
(3)常温常压下, 与
与 间的反应极慢,但向二者的混合物中加入适量的
间的反应极慢,但向二者的混合物中加入适量的 后,
后, 很快就会转化为
很快就会转化为 。反应过程中,反应体系的能量变化可用图1中的某一曲线表示(图中曲线a表示没有使用
。反应过程中,反应体系的能量变化可用图1中的某一曲线表示(图中曲线a表示没有使用 时的能量变化)。
时的能量变化)。

①最可能表示使用了 的能量变化曲线是
的能量变化曲线是_______ (填“b”或“c”), 表示的意义是
表示的意义是_______ 。
②若维持其他条件不变,用催化剂 代替
代替 ,下列物理量中不可能变化的是
,下列物理量中不可能变化的是_______ (填标号)。
A.反应的活化能 B.反应速率 C.反应热 D.平衡常数K
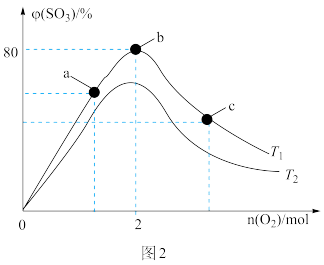
(4)2L恒容密闭容器中最初存在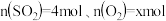 的混合物,分别在温度为
的混合物,分别在温度为 、
、 条件下发生反应
条件下发生反应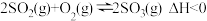 。控制其他条件不变,改变
。控制其他条件不变,改变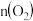 ,测得平衡时
,测得平衡时 的体积分数 [
的体积分数 [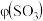 ]与
]与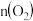 的关系如图2所示。
的关系如图2所示。
①
_______  (填“>”或“<”),a、b、c三点时,
(填“>”或“<”),a、b、c三点时, 转化率最大的是
转化率最大的是_______ 。
②若 ,计算温度为
,计算温度为 时反应
时反应 的平衡常数K=
的平衡常数K=_______ 。
(1)部分氮氧化合物之间的转化所发生的化学反应如下:
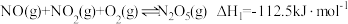
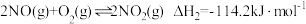
则反应
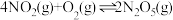 的
的
 。
。(2)已知
 的反应历程分两步:
的反应历程分两步:第一步:
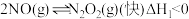 ;
; ;
;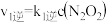
第二步:
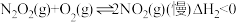 ;
;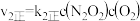 ;
;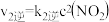
 的反应速率主要是由
的反应速率主要是由(3)常温常压下,
 与
与 间的反应极慢,但向二者的混合物中加入适量的
间的反应极慢,但向二者的混合物中加入适量的 后,
后, 很快就会转化为
很快就会转化为 。反应过程中,反应体系的能量变化可用图1中的某一曲线表示(图中曲线a表示没有使用
。反应过程中,反应体系的能量变化可用图1中的某一曲线表示(图中曲线a表示没有使用 时的能量变化)。
时的能量变化)。
①最可能表示使用了
 的能量变化曲线是
的能量变化曲线是 表示的意义是
表示的意义是②若维持其他条件不变,用催化剂
 代替
代替 ,下列物理量中不可能变化的是
,下列物理量中不可能变化的是A.反应的活化能 B.反应速率 C.反应热 D.平衡常数K
(4)2L恒容密闭容器中最初存在
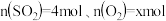 的混合物,分别在温度为
的混合物,分别在温度为 、
、 条件下发生反应
条件下发生反应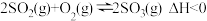 。控制其他条件不变,改变
。控制其他条件不变,改变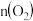 ,测得平衡时
,测得平衡时 的体积分数 [
的体积分数 [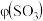 ]与
]与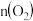 的关系如图2所示。
的关系如图2所示。
①

 (填“>”或“<”),a、b、c三点时,
(填“>”或“<”),a、b、c三点时, 转化率最大的是
转化率最大的是②若
 ,计算温度为
,计算温度为 时反应
时反应 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察______ 的快慢,定性比较得出结论。有同学提出将0.1mol/L FeCl3改为____ mol/L Fe2(SO4)3更为合理,其理由是____ 。
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是_____ 。
(3)查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度 分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和__________ 。
II.欲用下图所示实验来证明MnO2是H2O2分解反应的催化剂。
(1)该实验不能达到目的,若想证明MnO2是催化剂还需要确认__________ 。

加入0.10mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如下图所示。
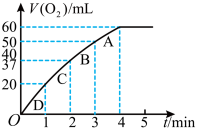
(2)写出H2O2在二氧化锰作用下发生反应的化学方程式_________ 。
(3)A、B、C、D各点反应速率快慢的顺序为______ >______ >______ >______ ,解释反应速率变化的原因__________ 。

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(3)查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从
II.欲用下图所示实验来证明MnO2是H2O2分解反应的催化剂。
(1)该实验不能达到目的,若想证明MnO2是催化剂还需要确认

加入0.10mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如下图所示。

(2)写出H2O2在二氧化锰作用下发生反应的化学方程式
(3)A、B、C、D各点反应速率快慢的顺序为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】利用DNA折纸技术进行多酶定向固定化,可显著提高糖类催化反应的酶活性。有关所做的葡萄糖的转化关系如下:
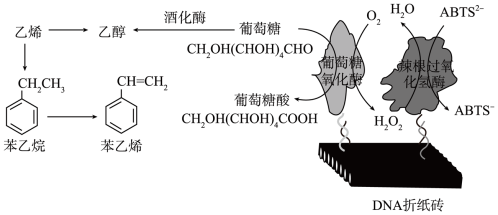
(1)乙烯转化为乙醇的反应类型为___________ 。
(2)苯乙烯共平面的原子最多有___________ 个,苯乙烯生成聚苯乙烯的化学方程式为___________ 。
(3)与苯乙烷互为同分异构体且含苯环的所有有机物的结构简式有___________ 。
(4)葡萄糖酸与锌反应生成葡萄糖酸锌的化学方程式为___________ ,该反应中葡萄糖酸表现出酸性或___________ 性。
(5)在葡萄糖氧化酶的作用下O2可选择性氧化葡萄糖中的___________ (填“-CHO”或“-OH”)
(6)下列有关DNA折纸技术进行多酶定向固定化的过程说法错误的是___________(填标号)。

(1)乙烯转化为乙醇的反应类型为
(2)苯乙烯共平面的原子最多有
(3)与苯乙烷互为同分异构体且含苯环的所有有机物的结构简式有
(4)葡萄糖酸与锌反应生成葡萄糖酸锌的化学方程式为
(5)在葡萄糖氧化酶的作用下O2可选择性氧化葡萄糖中的
(6)下列有关DNA折纸技术进行多酶定向固定化的过程说法错误的是___________(填标号)。
| A.H2O2在反应过程中做催化剂 |
| B.两种酶间距过小会导致堆积重叠,酶活性位点减少 |
| C.通过调节两种酶的比例,可提高化学反应限度 |
| D.通过测定ABTS2-的反应速率,可测试酶活性 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
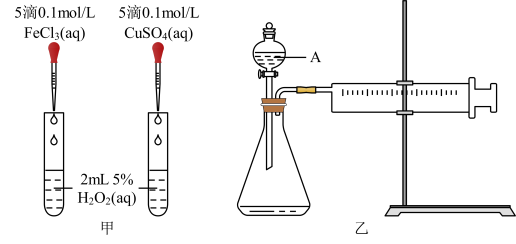
(1)定性分析:如图甲可通过观察________________ 现象,定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是________________
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为________________ ,实验中需要测量的数是________________
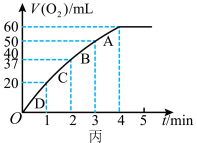
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。A、B、C、D各点反应速率由快到慢的顺序为________ 。

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。A、B、C、D各点反应速率由快到慢的顺序为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】环戊二烯(C5H6)是一种重要的有机化工原料。
Ⅰ.环戊二烯容易二聚生成双环戊二烯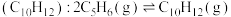 。不同温度下,溶液中环戊二烯的浓度(初始浓度为
。不同温度下,溶液中环戊二烯的浓度(初始浓度为 )与反应时间的关系如图所示。
)与反应时间的关系如图所示。
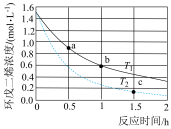
(1)反应开始至b点时,用双环戊二烯表示的平均速率为______  。
。
(2)T1______ T2(填“>”“<”或“=”)。
(3)a点的正反应速率______ b点的逆反应速率(填“>”“<”或“=”)。
Ⅱ.环戊二烯(C5H6)与环戊烯(C5H8)可发生相互转化。有如下反应:
反应ⅰ:
反应ⅱ: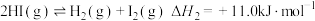
反应ⅲ: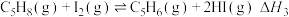
(4)反应i在______ (填“高温”或“低温”)下可自发进行。
(5)反应ⅲ的焓变
______  。
。
(6)某温度时,在1L恒容密闭容器中充入碘和环戊烯各1mol,只发生反应ⅲ,平衡时总压是起始总压的1.25倍。
①平衡时环戊烯的体积分数为______ 。
②该温度下,反应ⅲ的化学平衡常数K=______ 。
③保持温度和体积不变,向平衡体系中再充入1mol环戊二烯和1mol环戊烯,平衡______ 移动(填“向正反应方向”“向逆反应反向”或“不”)。
Ⅰ.环戊二烯容易二聚生成双环戊二烯
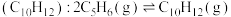 。不同温度下,溶液中环戊二烯的浓度(初始浓度为
。不同温度下,溶液中环戊二烯的浓度(初始浓度为 )与反应时间的关系如图所示。
)与反应时间的关系如图所示。
(1)反应开始至b点时,用双环戊二烯表示的平均速率为
 。
。(2)T1
(3)a点的正反应速率
Ⅱ.环戊二烯(C5H6)与环戊烯(C5H8)可发生相互转化。有如下反应:
反应ⅰ:

反应ⅱ:
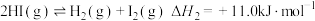
反应ⅲ:
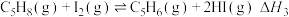
(4)反应i在
(5)反应ⅲ的焓变

 。
。(6)某温度时,在1L恒容密闭容器中充入碘和环戊烯各1mol,只发生反应ⅲ,平衡时总压是起始总压的1.25倍。
①平衡时环戊烯的体积分数为
②该温度下,反应ⅲ的化学平衡常数K=
③保持温度和体积不变,向平衡体系中再充入1mol环戊二烯和1mol环戊烯,平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】(1)已知下列热化学方程式:
a.H2(g)+ O2(g)═H2O(l);△H=-285.8kJ•mol-1
O2(g)═H2O(l);△H=-285.8kJ•mol-1
b.H2(g)+ O2(g)═H2O(g);△H=-241.8kJ•mol-1
O2(g)═H2O(g);△H=-241.8kJ•mol-1
c.CO(g)═C(s)+ O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1
d.C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
①上述反应中属于吸热反应的是________
②CO的燃烧热△H=________ 。表示CO燃烧热的热化学方程式为________ 。
③燃烧10g H2生成液态水,放出的热量为________ 。
(2)可以用反应的△H和△S的正、负来判断该反应自发进行的可能性和自发进行的条件。函数△G就是一个判断的依据:△G=△H-T△S式中T为反应的温度(开尔文温度,没有负值)。
①当一个反应的△G___________ 0(填“>”、“<”或“=”)时,反应一定能自发进行。
②当△H<0,△S<0,温度___________ (填“较高”或“较低”)时能自发反应。
a.H2(g)+
 O2(g)═H2O(l);△H=-285.8kJ•mol-1
O2(g)═H2O(l);△H=-285.8kJ•mol-1b.H2(g)+
 O2(g)═H2O(g);△H=-241.8kJ•mol-1
O2(g)═H2O(g);△H=-241.8kJ•mol-1c.CO(g)═C(s)+
 O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1d.C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
①上述反应中属于吸热反应的是
②CO的燃烧热△H=
③燃烧10g H2生成液态水,放出的热量为
(2)可以用反应的△H和△S的正、负来判断该反应自发进行的可能性和自发进行的条件。函数△G就是一个判断的依据:△G=△H-T△S式中T为反应的温度(开尔文温度,没有负值)。
①当一个反应的△G
②当△H<0,△S<0,温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。
Ⅰ.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气: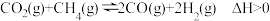
(1)此反应的活化能Ea(正)___________ Ea(逆)(填“>”、“=”或“<”),利于反应自发进行的条件是___________ (填“高温”或“低温”)。
(2)某温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=___________ (kPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应A: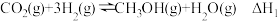
反应B: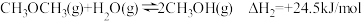
反应C: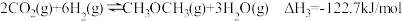
(3) =
=___________ kJ/mol。
(4)已知:某温度下,反应B的平衡常数的值为4,向密闭容器中加入CH3OCH3(g)和H2O(g)各2mol,则平衡时CH3OCH3的转化率为___________ 。
(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应A和反应C,在相同的时间段内CH3OH的产率、选择性随温度的变化如图所示。
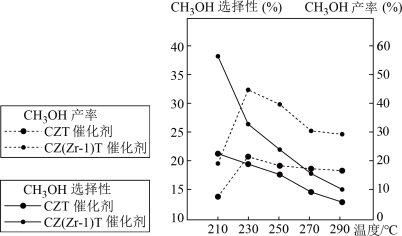
其中的CH3OH选择性
①当温度高于230℃时,CH3OH产率下降的可能原因是___________ 。
②在上述条件下合成甲醇的工业条件是___________ (填序号)。
A.210℃ B.230℃ C.CZT催化剂 D.CZ(Zr-1)T催化剂
Ⅲ.以铅蓄电池为电源可将CO2转化为乙烯,其原理如图所示,电解所用电极材料均为惰性电极。已知铅蓄电池总反应式为: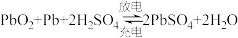

(6)理论上每消耗铅蓄电池中0.3mol硫酸,生成乙烯质量为___________ g。
Ⅰ.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:
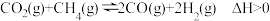
(1)此反应的活化能Ea(正)
(2)某温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=
Ⅱ.CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应A:
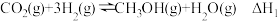
反应B:
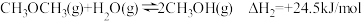
反应C:
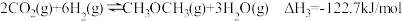
(3)
 =
=(4)已知:某温度下,反应B的平衡常数的值为4,向密闭容器中加入CH3OCH3(g)和H2O(g)各2mol,则平衡时CH3OCH3的转化率为
(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应A和反应C,在相同的时间段内CH3OH的产率、选择性随温度的变化如图所示。

其中的CH3OH选择性

①当温度高于230℃时,CH3OH产率下降的可能原因是
②在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C.CZT催化剂 D.CZ(Zr-1)T催化剂
Ⅲ.以铅蓄电池为电源可将CO2转化为乙烯,其原理如图所示,电解所用电极材料均为惰性电极。已知铅蓄电池总反应式为:
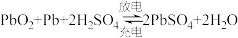

(6)理论上每消耗铅蓄电池中0.3mol硫酸,生成乙烯质量为
您最近一年使用:0次



