某化学自主实验小组通过实验探究 、
、 的性质。
的性质。
探究Ⅰ:利用如图所示装置探究 能否被
能否被 还原(
还原( 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。 的化学方程式是
的化学方程式是___________ 。
(2)甲、乙分别是___________ (填字母)。
a.浓硫酸、碱石灰 b.碱石灰、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若 能够被
能够被 还原,预期C装置中能观察到的现象是
还原,预期C装置中能观察到的现象是___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
探究Ⅱ:探究 、
、 混合气体的喷泉实验。
混合气体的喷泉实验。___________ 。
(6)G装置中浓硫酸有三种作用:混合 、
、 气体;干燥
气体;干燥 、
、 ;
;___________ 。
(7)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则所得溶液物质的量浓度为___________  (标准状况下,保留两位有效数字)。
(标准状况下,保留两位有效数字)。
 、
、 的性质。
的性质。探究Ⅰ:利用如图所示装置探究
 能否被
能否被 还原(
还原( 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。
 的化学方程式是
的化学方程式是(2)甲、乙分别是
a.浓硫酸、碱石灰 b.碱石灰、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若
 能够被
能够被 还原,预期C装置中能观察到的现象是
还原,预期C装置中能观察到的现象是(4)此实验装置存在一个明显的缺陷是
探究Ⅱ:探究
 、
、 混合气体的喷泉实验。
混合气体的喷泉实验。
(6)G装置中浓硫酸有三种作用:混合
 、
、 气体;干燥
气体;干燥 、
、 ;
;(7)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则所得溶液物质的量浓度为
 (标准状况下,保留两位有效数字)。
(标准状况下,保留两位有效数字)。
更新时间:2023-12-26 19:23:52
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】亚硝酰氯(NOCl)可作为有机合成试剂。
已知:①
②沸点:NOCl为-6℃, 为-34℃,NO为-152℃。
为-34℃,NO为-152℃。
③NOCl易水解,能与 反应。
反应。
某研究小组用NO和 在如图所示装置中制备NOCl,并分离回收未反应的原料。
在如图所示装置中制备NOCl,并分离回收未反应的原料。
(1)通入 和NO前先通入氩气,作用是
和NO前先通入氩气,作用是___________ ;仪器D的名称是___________ 。
(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是___________ 。
(3)实验所需的NO可用 和
和 溶液在稀
溶液在稀 中反应制得,离子反应方程式为
中反应制得,离子反应方程式为___________ 。
(4)为分离产物和未反应的原料,低温浴槽A的温度区间应控制在___________ ,仪器C收集的物质是___________ 。
(5)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应: ;
; 。若33.6mL(标况下)氮氧化物(只含NO和
。若33.6mL(标况下)氮氧化物(只含NO和 )与VmL 0.1mol/L NaOH溶液恰好完全反应,则
)与VmL 0.1mol/L NaOH溶液恰好完全反应,则
___________ 。
已知:①

②沸点:NOCl为-6℃,
 为-34℃,NO为-152℃。
为-34℃,NO为-152℃。③NOCl易水解,能与
 反应。
反应。某研究小组用NO和
 在如图所示装置中制备NOCl,并分离回收未反应的原料。
在如图所示装置中制备NOCl,并分离回收未反应的原料。
(1)通入
 和NO前先通入氩气,作用是
和NO前先通入氩气,作用是(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是
(3)实验所需的NO可用
 和
和 溶液在稀
溶液在稀 中反应制得,离子反应方程式为
中反应制得,离子反应方程式为(4)为分离产物和未反应的原料,低温浴槽A的温度区间应控制在
(5)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应:
 ;
; 。若33.6mL(标况下)氮氧化物(只含NO和
。若33.6mL(标况下)氮氧化物(只含NO和 )与VmL 0.1mol/L NaOH溶液恰好完全反应,则
)与VmL 0.1mol/L NaOH溶液恰好完全反应,则
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮是动植物生长过程中不可缺少的元素,其单质及其化合物有着广泛的用途。回答下列问题:
(1)肼(N2H4)、偏二甲肼(C2H8N2)、四氧化二氮(N2O4)都可用作火箭的燃料。
①N2H4、C2H8N2、N2O4中氮元素的质量分数由小到大的顺序为__ 。
②液态肼与液态四氧化二氨发生反应生成空气中含量最多的气体和水蒸气,写出该反应的化学方程式:___ 。
(2)将28gFe完全溶于一定量的HNO3溶液中,若只产生N2O、NO两种气体,该混合气体体积为5.6L(标准状况下),并且检测到溶液中金属阳离子只有Fe2+。
①与N2O互为等电子体的一种分子为__ ,其空间构型为___ 。
②写出上述Fe与HNO3反应生成N2O的离子方程式:___ 。
③生成的N2O、NO的物质的量之比为___ 。
(1)肼(N2H4)、偏二甲肼(C2H8N2)、四氧化二氮(N2O4)都可用作火箭的燃料。
①N2H4、C2H8N2、N2O4中氮元素的质量分数由小到大的顺序为
②液态肼与液态四氧化二氨发生反应生成空气中含量最多的气体和水蒸气,写出该反应的化学方程式:
(2)将28gFe完全溶于一定量的HNO3溶液中,若只产生N2O、NO两种气体,该混合气体体积为5.6L(标准状况下),并且检测到溶液中金属阳离子只有Fe2+。
①与N2O互为等电子体的一种分子为
②写出上述Fe与HNO3反应生成N2O的离子方程式:
③生成的N2O、NO的物质的量之比为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。
①铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为___________ 。
②PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_________ 。
③PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式__________ ;PbO2也可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生的电极反应式__________ 。
(2)钾长石(K2Al2Si6O16)通常也称正长石,主要用于生产玻璃、陶瓷制品,还可用于制取钾肥。
①请以氧化物组成的形式表示钾长石的化学式为___________
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的KAlO2和NaAlO2,写出Al2O3转化为NaAlO2的化学方程式___________ 。
(3)据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸的电子式:___________ ;若将84消毒液长期露置于空气中,溶液中的主要成分将变为___________ (填化学式)。
(1)铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。
①铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为
②PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
③PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式
(2)钾长石(K2Al2Si6O16)通常也称正长石,主要用于生产玻璃、陶瓷制品,还可用于制取钾肥。
①请以氧化物组成的形式表示钾长石的化学式为
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的KAlO2和NaAlO2,写出Al2O3转化为NaAlO2的化学方程式
(3)据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸的电子式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:___ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是___ (填字母)。
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是___ (填字母)。
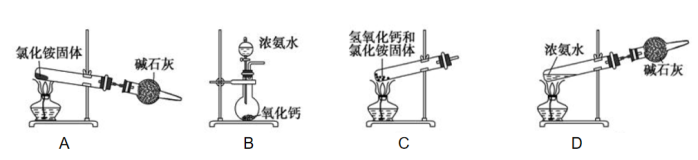
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验 的方法是
的方法是___ 。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
(3)如图是实验室制取氨气的装置和选用的试剂,其中错误的是

(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放氨气而降低肥效。检验
 的方法是
的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某兴趣小组同学探究了下列两类实验课题:
Ⅰ.利用下图实验装置进行气体的制备实验

(1)实验室制取 ,可选用的装置为
,可选用的装置为___________ (填标号)。
(2)用装置C制取 的化学方程式为
的化学方程式为___________ 。
Ⅱ.铜及其化合物在实验中的应用
(3)铜与浓硝酸反应的装置如下图,仪器D的名称为___________ ,该反应的离子方程式为___________ 。

(4)按下图实验装置(部分装置略)对有机化合物进行C、H元素分析。

①将装有样品的 坩埚和
坩埚和 放入石英管中,先
放入石英管中,先___________ ,而后将已称重的U型管K、L与石英管连接,检查___________ ,依次点燃煤气灯进行实验。
② 的作用是
的作用是___________ (举1例,用化学方程式表示)。
③K和L中的试剂分别是___________ 、___________ (填标号)。
A.无水 B.
B. C.碱石灰 D.
C.碱石灰 D.
Ⅰ.利用下图实验装置进行气体的制备实验

(1)实验室制取
 ,可选用的装置为
,可选用的装置为(2)用装置C制取
 的化学方程式为
的化学方程式为Ⅱ.铜及其化合物在实验中的应用
(3)铜与浓硝酸反应的装置如下图,仪器D的名称为

(4)按下图实验装置(部分装置略)对有机化合物进行C、H元素分析。

①将装有样品的
 坩埚和
坩埚和 放入石英管中,先
放入石英管中,先②
 的作用是
的作用是③K和L中的试剂分别是
A.无水
 B.
B. C.碱石灰 D.
C.碱石灰 D.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氮和硫是高中化学的核心元素。
(一)氮及其化合物是重要的化工原料。
(1)利用下图所示装置及药品制取氨气。

①A中制氨气的化学方程式是___________ 。
②C处是用集气瓶收集氨气的装置,请绘出装置图___________ 。
(2)氨经催化氧化可制备硝酸,其过程中涉及如下反应 ,若反应中消耗了2 mol
,若反应中消耗了2 mol  ,则转移电子的物质的量为
,则转移电子的物质的量为___________ mol。
(二)实验室中用下图装置(夹持装置已略去)研究不同价态硫元素之间的转化。

(3)A中产生的气体能使品红溶液褪色,A中反应的化学方程式为___________ 。
(4)B处实验现象是___________ ,由此推测硫元素从+4价变为+6价。
(5)C处观察到蘸有 溶液的棉花上出现黄色的固体,该反应的氧化剂为
溶液的棉花上出现黄色的固体,该反应的氧化剂为___________ (填化学式),氧化产物为___________ (填化学式)。
(6)D装置的作用是___________ ,发生反应的离子方程式为___________ 。
(7)将A中产生的气体通入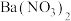 稀溶液,生成白色沉淀,发生反应的离子方程式为
稀溶液,生成白色沉淀,发生反应的离子方程式为___________ 。
(一)氮及其化合物是重要的化工原料。
(1)利用下图所示装置及药品制取氨气。

①A中制氨气的化学方程式是
②C处是用集气瓶收集氨气的装置,请绘出装置图
(2)氨经催化氧化可制备硝酸,其过程中涉及如下反应
 ,若反应中消耗了2 mol
,若反应中消耗了2 mol  ,则转移电子的物质的量为
,则转移电子的物质的量为(二)实验室中用下图装置(夹持装置已略去)研究不同价态硫元素之间的转化。

(3)A中产生的气体能使品红溶液褪色,A中反应的化学方程式为
(4)B处实验现象是
(5)C处观察到蘸有
 溶液的棉花上出现黄色的固体,该反应的氧化剂为
溶液的棉花上出现黄色的固体,该反应的氧化剂为(6)D装置的作用是
(7)将A中产生的气体通入
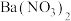 稀溶液,生成白色沉淀,发生反应的离子方程式为
稀溶液,生成白色沉淀,发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】按下图要求完成实验,并回答问题:
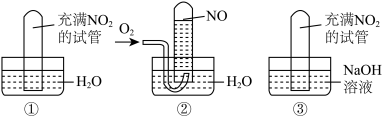
(1)实验①将充满二氧化氮的试管倒立水中,观察到的现象是__________________________ 。
(2)实验②将充满二氧化氮的试管倒立水中,再通入氧气时观察到的现象是_________ 。
(3)实验③将充满二氧化氮的试管倒立氢氧化钠溶液中,观察到的现象是_______________ 。

(1)实验①将充满二氧化氮的试管倒立水中,观察到的现象是
(2)实验②将充满二氧化氮的试管倒立水中,再通入氧气时观察到的现象是
(3)实验③将充满二氧化氮的试管倒立氢氧化钠溶液中,观察到的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W为电子数相同的分子或离子。X有5个原子核。通常状况下,W为无色液体。它们之间转化关系如图所示,请回答:
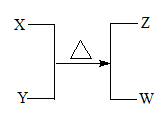
(1)工业上每制取1molZ要放出46.2 kJ的热量,写出该反应的热化学方程式:_____ 。
(2)实验室制取Z的方法不止一种,写出其中一种方法的化学方程式:_______ 。
(3)某化学小组同学模拟工业生产制取HNO3,设计如图所示装置,其中a为一个可持续鼓入空气的橡皮球。
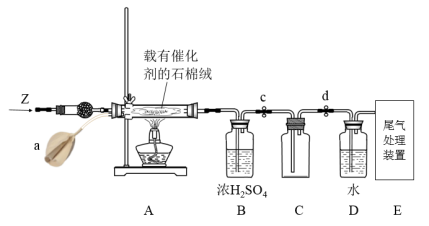
①A中发生反应的化学方程式是_______ 。
②B中浓H2SO4的作用是_______ 。
(4)写出D装置中反应的化学方程式_______ 。
(5)向含有ag HNO3的稀溶液中,加入bg铁粉充分反应,铁粉全部溶解。已知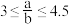 ,则被还原的HNO3的质量为
,则被还原的HNO3的质量为_______ g。

(1)工业上每制取1molZ要放出46.2 kJ的热量,写出该反应的热化学方程式:
(2)实验室制取Z的方法不止一种,写出其中一种方法的化学方程式:
(3)某化学小组同学模拟工业生产制取HNO3,设计如图所示装置,其中a为一个可持续鼓入空气的橡皮球。

①A中发生反应的化学方程式是
②B中浓H2SO4的作用是
(4)写出D装置中反应的化学方程式
(5)向含有ag HNO3的稀溶液中,加入bg铁粉充分反应,铁粉全部溶解。已知
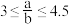 ,则被还原的HNO3的质量为
,则被还原的HNO3的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】非金属单质A经如图所示的过程转化为含氧酸D, 已知D为强酸,请回答下列问题:

(1)若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
①A的电子式是:___________ 。
②写出C →D的化学方程式___________ 。
③A中所含元素的非金属性___________ 碳(填强于,弱于或等于),请用一个化学方程式证明___________ 。
(2)若A在常温下为非金属气态氢化物,B遇到空气变成红棕色。
①写出工业上制取A气体的化学方程式___________ 。
②写出A到B的化学方程式___________ 。
(3)若A为淡黄色晶体:
①将C气体通入BaCl2溶液产生的白色沉淀化学式为___________ 。
②将B直接通入BaCl2溶液不会产生白色沉淀。但与另一种气体X一起通入时则会产生一种不同于①但元素组成与①相同的白色沉淀,则气体X的分子式___________ 。
③将B与一种黄绿色气体一起通入BaCl2溶液,会产生与①相同的白色沉淀,该反应的化学方程式为___________ 。

(1)若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的

①A的电子式是:
②写出C →D的化学方程式
③A中所含元素的非金属性
(2)若A在常温下为非金属气态氢化物,B遇到空气变成红棕色。
①写出工业上制取A气体的化学方程式
②写出A到B的化学方程式
(3)若A为淡黄色晶体:
①将C气体通入BaCl2溶液产生的白色沉淀化学式为
②将B直接通入BaCl2溶液不会产生白色沉淀。但与另一种气体X一起通入时则会产生一种不同于①但元素组成与①相同的白色沉淀,则气体X的分子式
③将B与一种黄绿色气体一起通入BaCl2溶液,会产生与①相同的白色沉淀,该反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】有机化合物的元素定量分析最早是由德国化学家李比希提出的,装置如下图,他用CuO作氧化剂,在750℃左右使有机物在氧气流中全部转化为 和
和 ,用盛有NaOH固体和无水
,用盛有NaOH固体和无水 的吸收管分别吸收
的吸收管分别吸收 和
和 。
。

试回答下列问题:
(1)甲装置中盛放的是___________ (填化学式)。
(2)将7.4g有机物A进行实验,测得生成 和
和 ,则A的实验式(最简式)为
,则A的实验式(最简式)为___________ 。
(3)已知A的最简式能否确定A的分子式(填“能”或“不能”)___________ 。也可以通过___________ 法快速、精确测定其相对分子质量,进而确定分子式。
(4)①若A为醇,且A的核磁共振氢谱图中有两组峰,则A的结构简式为___________ 。
②若A的红外光谱如图所示,则其官能团的名称为___________ 。

 和
和 ,用盛有NaOH固体和无水
,用盛有NaOH固体和无水 的吸收管分别吸收
的吸收管分别吸收 和
和 。
。
试回答下列问题:
(1)甲装置中盛放的是
(2)将7.4g有机物A进行实验,测得生成
 和
和 ,则A的实验式(最简式)为
,则A的实验式(最简式)为(3)已知A的最简式能否确定A的分子式(填“能”或“不能”)
(4)①若A为醇,且A的核磁共振氢谱图中有两组峰,则A的结构简式为
②若A的红外光谱如图所示,则其官能团的名称为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I.亚硫酰氯( )又名氯化亚砜,其熔点
)又名氯化亚砜,其熔点 ,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成
,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成 和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、染料工业及有机合成工业。
和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、染料工业及有机合成工业。
(1)氯化亚砜的保存方法是_______ 。
Ⅱ.实验室合成 的原理之一为
的原理之一为 ,可选用装置如图所示。
,可选用装置如图所示。

(2)实验室用二氧化锰制备氯气,应选用的发生装置为_______ (填标号);发生反应的离子方程式为_______ 。
(3)仪器a为球形冷凝管,起冷凝回流的作用。冷凝水的进口应为_______ (填③或④);装置b的作用为_______ 。
(4)实验室常用亚硫酸钠和浓硫酸反应制取 气体。制取干燥
气体。制取干燥 气体的装置与装置A的连接顺序为:②→
气体的装置与装置A的连接顺序为:②→_______ →⑦。
(5)写出亚硫酰氯( )与水反应的化学方程式
)与水反应的化学方程式_______ 。
 )又名氯化亚砜,其熔点
)又名氯化亚砜,其熔点 ,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成
,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成 和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、染料工业及有机合成工业。
和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、染料工业及有机合成工业。(1)氯化亚砜的保存方法是
Ⅱ.实验室合成
 的原理之一为
的原理之一为 ,可选用装置如图所示。
,可选用装置如图所示。
(2)实验室用二氧化锰制备氯气,应选用的发生装置为
(3)仪器a为球形冷凝管,起冷凝回流的作用。冷凝水的进口应为
(4)实验室常用亚硫酸钠和浓硫酸反应制取
 气体。制取干燥
气体。制取干燥 气体的装置与装置A的连接顺序为:②→
气体的装置与装置A的连接顺序为:②→(5)写出亚硫酰氯(
 )与水反应的化学方程式
)与水反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】铁是人体必需的微量元素,在肺部,血红蛋白中血红素的Fe2+与O2结合,把O2送到各个组织器官。铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】 称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。在坩埚中高温灼烧黑木耳,使之完全灰化。用酸充分溶解,过滤,滤液备用。
①浸泡液检测不出铁元素的原因是________ 。
②滤液中铁元素的存在形式是Fe2+、________ 。
(2)【配制溶液】 将滤液配制成100 mL 溶液。选择合适的仪器完成“铁元素的分离”、
“配制溶液”2个实验,下列仪器不必使用的是_______ 。

(3)【铁元素含量测定】 研学小组提出如下测量方案:
Ⅰ.沉淀法:向溶液中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。评价该测量方案是否可行________ 。
Ⅱ.比色法:流程示意如下:

① 用离子方程式解释加入H2O2的目的是________ 。
② 溶液a的颜色是________ 。
③ 溶液颜色越深,光的透过能力越差,即透光率越小。若不加H2O2,测出黑木耳中铁元素的含量________ (填“偏大”或“偏小”)。
(4)亚铁盐易被氧化,但在体内Fe2+参与O2的运输却不被氧化。蛋白质是一种既有亲水部分、又有疏水部分的大分子,为血红素提供了疏水环境。

可见,氧化还原反应能否发生与_________ 有关。
(1)【铁元素的分离】 称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。在坩埚中高温灼烧黑木耳,使之完全灰化。用酸充分溶解,过滤,滤液备用。
①浸泡液检测不出铁元素的原因是
②滤液中铁元素的存在形式是Fe2+、
(2)【配制溶液】 将滤液配制成100 mL 溶液。选择合适的仪器完成“铁元素的分离”、
“配制溶液”2个实验,下列仪器不必使用的是

(3)【铁元素含量测定】 研学小组提出如下测量方案:
Ⅰ.沉淀法:向溶液中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。评价该测量方案是否可行
Ⅱ.比色法:流程示意如下:

① 用离子方程式解释加入H2O2的目的是
② 溶液a的颜色是
③ 溶液颜色越深,光的透过能力越差,即透光率越小。若不加H2O2,测出黑木耳中铁元素的含量
(4)亚铁盐易被氧化,但在体内Fe2+参与O2的运输却不被氧化。蛋白质是一种既有亲水部分、又有疏水部分的大分子,为血红素提供了疏水环境。

可见,氧化还原反应能否发生与
您最近一年使用:0次



