设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下, 与等体积 与等体积 混合所得分子数为 混合所得分子数为 |
B. 盐酸中含有阴阳离子总数为 盐酸中含有阴阳离子总数为 |
C. 与足量铁粉反应转移的电子数为 与足量铁粉反应转移的电子数为 |
D.电解熔融 ,阴极增重 ,阴极增重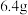 ,外电路中通过电子的数目为 ,外电路中通过电子的数目为 |
更新时间:2023-12-30 21:46:14
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.18gD2O中含有的质子数为10NA |
| B.25℃,pH=13的NaOH溶液中含有OH-的数目为 0.1NA |
| C.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氮原子数目为0.2NA |
| D.密闭容器中2 mol NO与1 mol O2充分反应,产物分子的数目为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.标准状况下,22.4 L乙烯含有的共用电子对数为5NA |
| B.3.36 L NO2与水充分反应转移的电子数目为0.1NA |
| C.常温常压下,5.6g环丙烷和聚乙炔的混合物中含有的碳原子数为0.4NA |
| D.2.0gH218O与D2O的混合物中所含中子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏伽德罗常数的值,下列有关叙述正确的是
| A.标准状况下,22.4LHF中含有的分子数为NA |
| B.常温常压下,硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA |
| C.标准状况下,8.96L平均相对分子质量为3.5的H2与D2含有的中子数为0.3NA |
| D.0.1L18mol/L浓硫酸与足量金属铜在加热条件下充分反应,生成0.9NA个SO2分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将5.0CaCO3加入到足量盐酸中,并将生成的气体全部通入足量的红热的炭中充分反应,得到气体的体积(标准状况下)为)
| A.1.12L | B.2.24L | C.11.2L | D.22.4L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】VL Fe2(SO4)3溶液中含有ag SO ,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量浓度为( )
,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量浓度为( )
 ,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量浓度为( )
,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量浓度为( )A.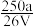 mol·L-1 mol·L-1 | B.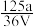 mol·L-1 mol·L-1 | C.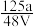 mol·L-1 mol·L-1 | D.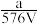 mol·L-1 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知NA是阿伏加德罗常数的值,下列说法错误的是
| A.22.4L(标准状况)氩气含有的电子数为18NA |
| B.1L0.1mol•L-1碳酸钠溶液含有的Na+数目0.1NA |
| C.标准状况下,2.24LN2和O2的混合气体中分子数为0.1NA |
| D.16gCH4中含有的原子总数为5NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,在避光的容器中,将下列各组气体充分混合后能发生明显反应的是
| A.H2和Cl2 | B.SO2和H2S | C.H2和O2 | D.N2和H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于一氧化氮( )性质的描述中,
)性质的描述中,不正确 的是
 )性质的描述中,
)性质的描述中,| A.红棕色气体 | B.能与氧气反应 |
| C.相同条件下密度比空气的略大 | D.不能与水反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 盛有某气体的集气瓶敞口后,变成红棕色 | 该气体中肯定只有 |
| B | 向 溶液中滴加维生素 溶液中滴加维生素 溶液,溶液变为浅绿色 溶液,溶液变为浅绿色 | 维生素C有氧化性 |
| C | 向两支盛有 的双氧水溶液的试管中,分别滴加几滴 的双氧水溶液的试管中,分别滴加几滴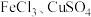 溶液,前者气泡产生速率快 溶液,前者气泡产生速率快 | 催化能力: |
| D | 将用导线、灵敏电流计相连的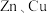 片放入盛有稀硫酸的烧杯中,电流计指针偏转 片放入盛有稀硫酸的烧杯中,电流计指针偏转 | 形成了原电池 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】CO2催化加氢制备甲醇的反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g);ΔH=-49 kJ·mol-1,CO2电化学还原法制备甲醇的电解原理如图所示。下列说法错误的是
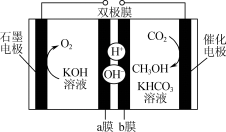
| A.CO2催化加氢法在低温自发进行主要受ΔH的影响 |
| B.a膜为阴离子交换膜,石墨电极上的电极反应式为4OH-4e-= 2H2O+O2↑ |
C.电解过程中,右室溶液中HCO 的物质的量几乎不变 的物质的量几乎不变 |
| D.产生等量CH3OH时,催化加氢法消耗的H2与电化学还原法产生的O2的物质的量之比为1∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】电解法可以对含亚硝酸盐(如亚硝酸钠)的污水进行处理(工作原理如下图所示)。通电后,左极区产生浅绿色溶液,随后生成无色气体。下列说法错误的是
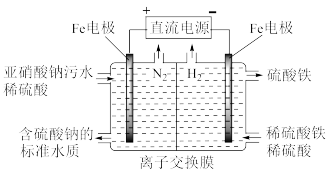

| A.阳极电极反应式为Fe-2e-=Fe2+ |
B.阳极附近溶液中反应的离子方程式为6Fe2++2NO +8H+=6Fe3++N2↑+4H2O +8H+=6Fe3++N2↑+4H2O |
| C.该电解装置所使用的离子交换膜为阴离子交换膜 |
| D.当阳极(铁电极)质量减轻56g时,理论上可处理NaNO2含量4.6%的污水500g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】2020年6月,清华大学发现了一种新型的钾离子电池正极材料,比过去使用的任何材料都更加稳定。电池示意图如下,总反应为FeC2O4F+KC6 C6+KFeC2O4F。下列有关说法错误的是
C6+KFeC2O4F。下列有关说法错误的是

 C6+KFeC2O4F。下列有关说法错误的是
C6+KFeC2O4F。下列有关说法错误的是
| A.放电时,负极反应为:KC6-e-=K++C6 |
| B.充电时,阳极反应:KFeC2O4F-e-=FeC2O4F+K+ |
| C.充电时,当电路中通过的电子为0.02mol时,碳电极增加的质量为0.78g |
| D.用该电池电解饱和食盐水,阴极产生4.48L气体时,通过隔膜的K+为0.2mol |
您最近一年使用:0次



