按要求回答问题
(1)工业上利用甲酸的能量关系转换图如下:
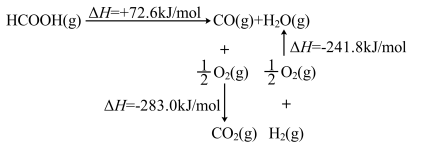
则反应 的焓变
的焓变
_______  。
。
(2)乙烷燃料电池,当电解质溶液为KOH时,写出负极的电极反应式_______ 。
(3)Cu做电极,电解 溶液,阳极反应式
溶液,阳极反应式_______ ;阴极反应式_______ 。
(4)铅蓄电池总反应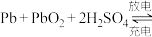
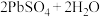 ,写出充电时阴极的电极反应式
,写出充电时阴极的电极反应式_______ 。
(5)一种心脏起搏器电解质为等物质的量的LiCl、 溶解在
溶解在 中形成的溶液,这种电池的总反应为
中形成的溶液,这种电池的总反应为 ,则该电池的正极反应为
,则该电池的正极反应为_______ 。
(1)工业上利用甲酸的能量关系转换图如下:

则反应
 的焓变
的焓变
 。
。(2)乙烷燃料电池,当电解质溶液为KOH时,写出负极的电极反应式
(3)Cu做电极,电解
 溶液,阳极反应式
溶液,阳极反应式(4)铅蓄电池总反应
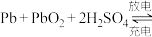
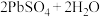 ,写出充电时阴极的电极反应式
,写出充电时阴极的电极反应式(5)一种心脏起搏器电解质为等物质的量的LiCl、
 溶解在
溶解在 中形成的溶液,这种电池的总反应为
中形成的溶液,这种电池的总反应为 ,则该电池的正极反应为
,则该电池的正极反应为
更新时间:2024/01/07 08:35:04
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】明矾石经处理后得到明矾(KAl(SO4)2·12H2O)。由明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
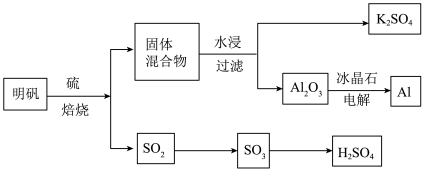
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比为_______ 。
(2)从水浸后的滤液中得到K2SO4晶体的操作方法是_______ 。
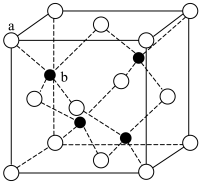
(3)A12O3在一定条件下可制得AIN,AlN的晶体结构与金刚石相似,晶胞结构如图所示。每个晶胞中含有_______ 个铝原子,若Al与N原子最近距离为apm,则该晶体的密度为_______ g/cm3。(阿伏加 德罗常数用NA表示)
(4)SO2分子的空间构型为_______
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时
2SO2(g)+O2(g) 2SO3(g)△H1=一197kJ/mol;
2SO3(g)△H1=一197kJ/mol;
2H2O(g)=2H2O(1)△H2=一44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是_______ 。

焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比为
(2)从水浸后的滤液中得到K2SO4晶体的操作方法是
(3)A12O3在一定条件下可制得AIN,AlN的晶体结构与金刚石相似,晶胞结构如图所示。每个晶胞中含有

(4)SO2分子的空间构型为
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时
2SO2(g)+O2(g)
 2SO3(g)△H1=一197kJ/mol;
2SO3(g)△H1=一197kJ/mol;2H2O(g)=2H2O(1)△H2=一44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲烷和水蒸气催化制氢主要有如下两个反应:
①CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41kJ·mol-1
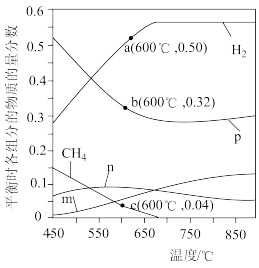
恒定压强为100kPa时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示,回答下列问题:_______ 。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是_______(填字母)。
(3)系统中H2的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
①低于700℃,_______ ;
②高于700℃,_______ 。
①CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41kJ·mol-1
恒定压强为100kPa时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示,回答下列问题:
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是_______(填字母)。
| A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快 |
| B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快 |
| C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快 |
| D.加入合适的催化剂,降低反应温度也能实现单位时间转化率不变 |
(3)系统中H2的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
①低于700℃,
②高于700℃,
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】利用 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。
(1)20世纪初,工业上以 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
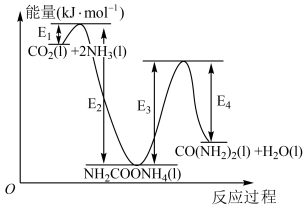
①反应物液氨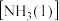 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在___________ (填作用力名称)。
②写出在该条件下由 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:___________ 。
(2)近年研究发现,电催化 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
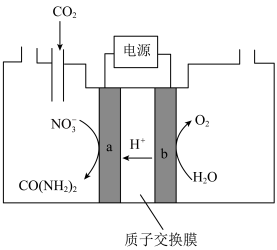
①电解过程中生成尿素的电极反应式为___________ 。
②目前以 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到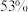 的法拉第效率
的法拉第效率 。已知:
。已知: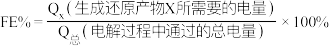 ,其中,
,其中,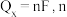 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下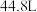 的
的 ,可获得尿素的质量为
,可获得尿素的质量为___________ 。(尿素的相对分子质量:60)
(3)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。

①消化液中的含氮粒子是___________ 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。
 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。(1)20世纪初,工业上以
 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
①反应物液氨
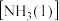 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在②写出在该条件下由
 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:(2)近年研究发现,电催化
 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
①电解过程中生成尿素的电极反应式为
②目前以
 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到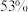 的法拉第效率
的法拉第效率 。已知:
。已知: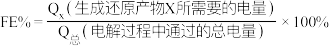 ,其中,
,其中,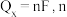 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下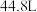 的
的 ,可获得尿素的质量为
,可获得尿素的质量为(3)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。请按要求回答相关问题:
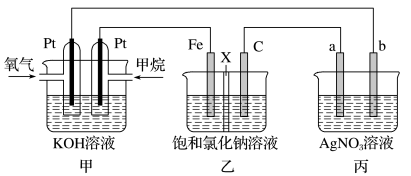
(1)甲装置电池负极发生的电极反应式是:___________ 。
(2)乙中X是___________ (阴、阳)离子交换膜,向乙中加入几滴酚酞溶液,工作一段时间后______ 电极(填Fe或C)附近溶液变红,请用化学用语解释相关原因___________ 。
(3)若在标准状况下,有 氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
氧气参加反应,则乙装置中C电极上生成的气体的物质的量为___________ 。
(4)若丙装置中a、b电极均为 ,则丙池电解的总反应离子方程式是
,则丙池电解的总反应离子方程式是___________ 。
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解 的原理如图所示
的原理如图所示

 电极上的电极反应式为
电极上的电极反应式为___________ 。

(1)甲装置电池负极发生的电极反应式是:
(2)乙中X是
(3)若在标准状况下,有
 氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
氧气参加反应,则乙装置中C电极上生成的气体的物质的量为(4)若丙装置中a、b电极均为
 ,则丙池电解的总反应离子方程式是
,则丙池电解的总反应离子方程式是(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解
 的原理如图所示
的原理如图所示
 电极上的电极反应式为
电极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】碳氧化物、氮氧化物及含氮化合物的处理与利用是世界各国研究的热点问题。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1162kJ·mol-1。
写出CH4将NO2还原为N2的热化学方程式:___ 。
(2)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.4molCO,在催化剂存在的条件下发生反应2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH<0,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后c(CO)=
2CO2(g)+N2(g) ΔH<0,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后c(CO)=___ mol/L,关于该平衡的下列说法正确的是___ 。
a.达到平衡后v正(NO)=2v逆(N2)
b.其他条件不变,升高温度,化学反应速率一定增大
c.其他条件不变,增大CO浓度,该反应平衡常数增大
d.增大压强,平衡一定向右移动
e.其他条件不变,若改为在恒压容器中进行,CO的平衡转化率比恒容条件下大
(3)其他条件相同,tmin时不同温度下测得NO的转化率如图所示。

A点的反应速度v正___ (填“>”、“<”或“=”)v逆,A、B两点反应的平衡常数较大的是___ (填“A”或“B”)。
(4)肼(N2H4)是一种良好的火箭燃料,与适当的氧化剂配合,可组成比冲最高的可贮存液体推进剂。在一定条件下也可与氧气构成燃料电池,图中甲池的总反应式为N2H4+O2=N2+2H2O。
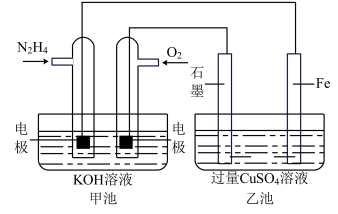
①甲池中负极上的电极反应式为___ 。
②要使乙池恢复到电解前的状态,可向溶液中加入适量的___ 。
A.CuSO4 B.CuO C.CuCO3 D.Cu(OH)2
③若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗3.2gN2H4时,乙池中两个电极质量差为___ g。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1162kJ·mol-1。
写出CH4将NO2还原为N2的热化学方程式:
(2)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.4molCO,在催化剂存在的条件下发生反应2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH<0,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后c(CO)=
2CO2(g)+N2(g) ΔH<0,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后c(CO)=a.达到平衡后v正(NO)=2v逆(N2)
b.其他条件不变,升高温度,化学反应速率一定增大
c.其他条件不变,增大CO浓度,该反应平衡常数增大
d.增大压强,平衡一定向右移动
e.其他条件不变,若改为在恒压容器中进行,CO的平衡转化率比恒容条件下大
(3)其他条件相同,tmin时不同温度下测得NO的转化率如图所示。

A点的反应速度v正
(4)肼(N2H4)是一种良好的火箭燃料,与适当的氧化剂配合,可组成比冲最高的可贮存液体推进剂。在一定条件下也可与氧气构成燃料电池,图中甲池的总反应式为N2H4+O2=N2+2H2O。

①甲池中负极上的电极反应式为
②要使乙池恢复到电解前的状态,可向溶液中加入适量的
A.CuSO4 B.CuO C.CuCO3 D.Cu(OH)2
③若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗3.2gN2H4时,乙池中两个电极质量差为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】CO2是一种温室气体,对人类的生存环境产生巨大的影响,将CO2作为原料转化为有用化学品,对实现碳中和及生态环境保护有着重要意义。
I、工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为2NH3(1)+CO2(l)=H2O(l)+NH2CONH2(1) ΔH=_____ kJ/mol。
(2)在恒容密闭容器中发生反应: 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH<0。下列说法错误的是
Ⅱ.由CO2与H2制备甲醇是当今研究的热点之一。
(3)在一定条件下,向0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH3=- 50kJ·mol-1
CH3OH(g)+H2O(g) ΔH3=- 50kJ·mol-1

①若x=1、y=3, 测得在相同时间内,不同温度下H2的转化率如图1所示,点a_____ 填“是”或“否”)达到平衡。T2时,若起始压强为10atm, Kp=_____ atm-2(结果保留一位小数,Kp为以分压表示的平衡常数,分压=总压 ×物质的量分数)。
②已知速率方程v正 =k正 c(CO2)·c3(H2), v逆 =k逆c(CH3OH)·c(H2O), k正、k 逆是速率常数,只受温度影响,图2表示速率常数k正、k逆的对数lgk与温度的倒数 之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,其中点
之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,其中点_____ (填A或B或D或E)表示c点的lgk逆。

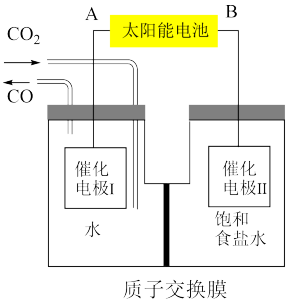
(4)我国科学家设计出如图装置实现CO2的转化,可有效解决温室效应及能源问题,总反应为CO2+NaCl CO+NaClO(忽略气体 在溶液中的溶解及溶液的体积变化)。
CO+NaClO(忽略气体 在溶液中的溶解及溶液的体积变化)。
电极Ⅱ的电极反应式为_______ 。电解结束后,电极Ⅱ所在电极室溶液pH ___________ (填“变大”或“变小”)
I、工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为2NH3(1)+CO2(l)=H2O(l)+NH2CONH2(1) ΔH=
(2)在恒容密闭容器中发生反应: 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH<0。下列说法错误的是
| A.反应在任何温度下都能自发进行 |
| B.增大CO2的浓度,有利于NH3的转化率增大 |
| C.当混合气体的密度不再发生改变时反应达平衡状态 |
| D.充入He,压强增大,平衡向正反应移动 |
Ⅱ.由CO2与H2制备甲醇是当今研究的热点之一。
(3)在一定条件下,向0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH3=- 50kJ·mol-1
CH3OH(g)+H2O(g) ΔH3=- 50kJ·mol-1
①若x=1、y=3, 测得在相同时间内,不同温度下H2的转化率如图1所示,点a
②已知速率方程v正 =k正 c(CO2)·c3(H2), v逆 =k逆c(CH3OH)·c(H2O), k正、k 逆是速率常数,只受温度影响,图2表示速率常数k正、k逆的对数lgk与温度的倒数
 之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,其中点
之间的关系, A、B、D、E分别代表图1中a点、c点的速率常数,其中点
(4)我国科学家设计出如图装置实现CO2的转化,可有效解决温室效应及能源问题,总反应为CO2+NaCl
 CO+NaClO(忽略气体 在溶液中的溶解及溶液的体积变化)。
CO+NaClO(忽略气体 在溶液中的溶解及溶液的体积变化)。电极Ⅱ的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】 是大气的主要污染物,工业上利用钠碱循环法可除去
是大气的主要污染物,工业上利用钠碱循环法可除去 。回答下列问题:
。回答下列问题:
(1)钠碱循环法中,吸收液为 溶液,其中各离子浓度由大到小的顺序为
溶液,其中各离子浓度由大到小的顺序为_______ 。
(2)可用 溶液吸收
溶液吸收 制备
制备 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(3)已知 的电离常数为
的电离常数为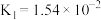 ,
,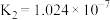 ;
; 的电离常数为
的电离常数为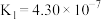 ,
,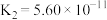 ,则下列各组微粒可以大量共存的是_______。(填字母)
,则下列各组微粒可以大量共存的是_______。(填字母)
(4)①写出 的水解常数表达式
的水解常数表达式_______ 。
②根据测定 溶液呈酸性,试用所学知识解释:
溶液呈酸性,试用所学知识解释:_______
则0.1mol/L 溶液中粒子浓度关系不正确的是
溶液中粒子浓度关系不正确的是_______ 。(填字母)
A.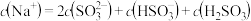
B.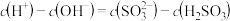
C.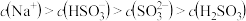
D.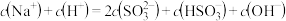
(5)当吸收液的pH降至约为6时,需送至电解槽再生回收液。再生示意图如下:
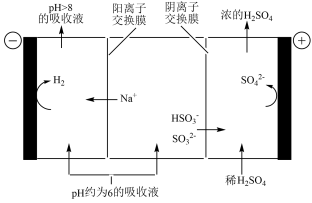
 在阳极放电的电极反应式是
在阳极放电的电极反应式是_______ 。
 是大气的主要污染物,工业上利用钠碱循环法可除去
是大气的主要污染物,工业上利用钠碱循环法可除去 。回答下列问题:
。回答下列问题:(1)钠碱循环法中,吸收液为
 溶液,其中各离子浓度由大到小的顺序为
溶液,其中各离子浓度由大到小的顺序为(2)可用
 溶液吸收
溶液吸收 制备
制备 ,该反应的离子方程式是
,该反应的离子方程式是(3)已知
 的电离常数为
的电离常数为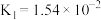 ,
,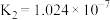 ;
; 的电离常数为
的电离常数为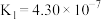 ,
,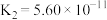 ,则下列各组微粒可以大量共存的是_______。(填字母)
,则下列各组微粒可以大量共存的是_______。(填字母)A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
 的水解常数表达式
的水解常数表达式②根据测定
 溶液呈酸性,试用所学知识解释:
溶液呈酸性,试用所学知识解释:则0.1mol/L
 溶液中粒子浓度关系不正确的是
溶液中粒子浓度关系不正确的是A.
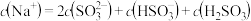
B.
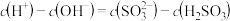
C.
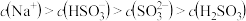
D.
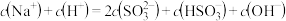
(5)当吸收液的pH降至约为6时,需送至电解槽再生回收液。再生示意图如下:

 在阳极放电的电极反应式是
在阳极放电的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】生产生活中排放的废气废水有一定量的氨氮化合物,必须通过处理后达到国家规定的排放标准再排放,以下为两种处理氨氮化合物的方法。
Ⅰ.催化氧化法:某学习小组模拟氨气的催化氧化,向恒温恒容密闭容器内充入4mol 和3mol
和3mol ,在加热和催化剂的作用下存在如下反应;
,在加热和催化剂的作用下存在如下反应;
反应①(主);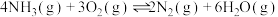
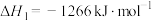
反应②(副):
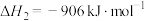
反应③(副):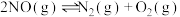

(1)反应③NO在催化剂作用下分解,也是一种消除污染的方法,其 为
为___________  。
。
(2)下列说法正确的是___________ (填标号)。
a.反应①在任何温度下均能自发进行
b.混合气体的密度不变说明体系已达到平衡
c.在实际中,需采用高压氧化,以利于提高 的生成量
的生成量
(3)体系平衡时, 的物质的量为amol,
的物质的量为amol, 的物质的量为bmol。此时,
的物质的量为bmol。此时, 的物质的量为
的物质的量为___________ mol(用含a、b的代数式表示,下同),反应③的平衡常数K=___________ 。
Ⅱ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。

(4)电解时,阳极的电极反应式为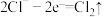 、
、___________ 。
(5)该装置可以生成大量氧化性更强的·OH,写出·OH去除 的离子方程式:
的离子方程式:______________________ 。
(6)相比于传统的二维电极反应系统,三维电极有哪些优点?试述其优点:___________ (答出一种,合理即可)。
Ⅰ.催化氧化法:某学习小组模拟氨气的催化氧化,向恒温恒容密闭容器内充入4mol
 和3mol
和3mol ,在加热和催化剂的作用下存在如下反应;
,在加热和催化剂的作用下存在如下反应;反应①(主);
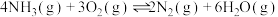
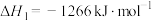
反应②(副):

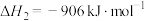
反应③(副):
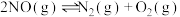

(1)反应③NO在催化剂作用下分解,也是一种消除污染的方法,其
 为
为 。
。(2)下列说法正确的是
a.反应①在任何温度下均能自发进行
b.混合气体的密度不变说明体系已达到平衡
c.在实际中,需采用高压氧化,以利于提高
 的生成量
的生成量(3)体系平衡时,
 的物质的量为amol,
的物质的量为amol, 的物质的量为bmol。此时,
的物质的量为bmol。此时, 的物质的量为
的物质的量为Ⅱ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的
 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。
(4)电解时,阳极的电极反应式为
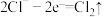 、
、(5)该装置可以生成大量氧化性更强的·OH,写出·OH去除
 的离子方程式:
的离子方程式:(6)相比于传统的二维电极反应系统,三维电极有哪些优点?试述其优点:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
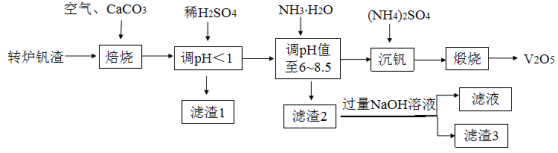
【推荐3】一种以转炉钒渣(主要成分为V2O3、FeO、SiO2及少量MgO、CaO、Al2O3)为原料实现低成本回收钒资源的生产工艺如下:
表一:相关金属离子[c0(Mn+)=0.01mol·L−1]形成氢氧化物沉淀的pH范围如下:
表二:部分含钒物质在水溶液中主要存在形式如下:
已知:①“焙烧”的主要反应为:CaCO3(s)=CaO(s)+CO2(g);
②在焙烧过程中产生Ca2V2O7;其中,Ca2V2O7在水中的溶解度小,易溶于稀硫酸和碱溶液。
回答下列问题:
(1)Ca2V2O7中V的化合价为_______ ,写出流程中氧化“钒”的化学方程式_______ 。
(2)“酸浸”后钒元素主要以VO 存在,生成VO
存在,生成VO 的离子方程式为
的离子方程式为_______ 。
(3)“滤渣2”的主要成分是_______ 。
(4)“调pH”中一般控制温度不超过40℃,原因是_______ 。
(5)利用上述表格数据,计算Fe(OH)3的Ksp=_______ 。
(6)已知“沉钒”得到NH4VO3,该环节通常需要加入过量(NH4)2SO4,其原因是_______ 。
(7)滤液经浓缩后,经电解后得到高纯度的氢氧化物,该反应阴极电极反应式为_______ 。

表一:相关金属离子[c0(Mn+)=0.01mol·L−1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 7.5 | 2.2 | 3.7 | 9.4 |
| 沉淀完全的pH | 9.0 | 3.2 | 4.7 | 10.9 |
| pH | <1 | 1~4 | 6~8.5 | >13 |
| 主要形式 | VO | V2O5 | VO | VO |
| 备注 | 多钒酸盐在水中溶解度较小 | |||
②在焙烧过程中产生Ca2V2O7;其中,Ca2V2O7在水中的溶解度小,易溶于稀硫酸和碱溶液。
回答下列问题:
(1)Ca2V2O7中V的化合价为
(2)“酸浸”后钒元素主要以VO
 存在,生成VO
存在,生成VO 的离子方程式为
的离子方程式为(3)“滤渣2”的主要成分是
(4)“调pH”中一般控制温度不超过40℃,原因是
(5)利用上述表格数据,计算Fe(OH)3的Ksp=
(6)已知“沉钒”得到NH4VO3,该环节通常需要加入过量(NH4)2SO4,其原因是
(7)滤液经浓缩后,经电解后得到高纯度的氢氧化物,该反应阴极电极反应式为
您最近一年使用:0次



