氧化还原反应在人类的生产、生活中有着重要的应用。回答下列问题:
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为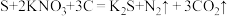 。该反应中,被还原的元素是
。该反应中,被还原的元素是________ (填元素符号),消耗的还原剂和氧化剂质量比为_________ 。
(2)实验室制备Cl2有三种常用方法:
a.
b.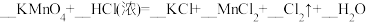
c.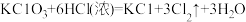
①配平反应b的方程式:___________ 。
②当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应_____ (填“a”“b”或“c”)。
(3)以MnO2为原料在加热熔融条件下可以制取K2MnO4,该反应中包含的所有物质为MnO2、K2 MnO4、KCl、KOH、KClO3、H2O。写出该反应的化学方程式:___________ 。
(4)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄(As2S3,As为+3价,S为-2价)褪色的主要原因是发生了以下两种化学反应:
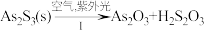 ,
,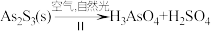 。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I
。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I______ Ⅱ(填“>”“<”或“=”),转移的电子数之比为_______ 。
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为
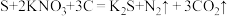 。该反应中,被还原的元素是
。该反应中,被还原的元素是(2)实验室制备Cl2有三种常用方法:
a.

b.
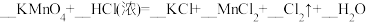
c.
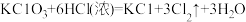
①配平反应b的方程式:
②当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应
(3)以MnO2为原料在加热熔融条件下可以制取K2MnO4,该反应中包含的所有物质为MnO2、K2 MnO4、KCl、KOH、KClO3、H2O。写出该反应的化学方程式:
(4)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄(As2S3,As为+3价,S为-2价)褪色的主要原因是发生了以下两种化学反应:
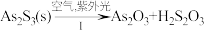 ,
,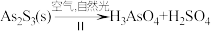 。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I
。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I
更新时间:2024-01-10 20:21:32
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】实验室也可用KMnO4固体和浓盐酸反应制氯气,反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑ 完成下列问题:
(1)该反应中氧化剂是___________ ,还原剂是____________ ,还原产物是_____________ 。
(2)用双线桥标出该反应的电子得失的方向和数目___________________________ ,每有1mol HCl参与反应,则所转移电子的物质的量是__________ mol。
(1)该反应中氧化剂是
(2)用双线桥标出该反应的电子得失的方向和数目
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
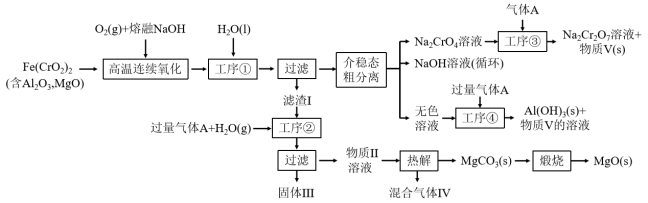
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是___________ (填元素符号)。
(2)工序③中发生反应的离子方程式为___________ 。
(3)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为___________

回答下列问题:
(1)高温连续氧化工序中被氧化的元素是
(2)工序③中发生反应的离子方程式为
(3)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】化学实验中,如使某步反应中的有害产物作为另一步反应的反应物,形成一个循环,就可不再向环境排放该种有害物质。如图所示。
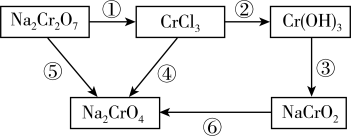
(1)配平反应方程式并回答问题,用单线桥标出两个反应的电子转移的方向和数目。
反应①: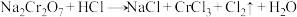 ,
,__________ ,氧化剂为__________ (填化学式,后同),氧化产物为__________ 。
反应⑥: ,
,__________ ,还原剂为__________ ,还原产物为__________ 。
(2)在上述有编号的步骤中,除了①⑥外,还需用到氧化剂的步骤是__________ (填编号)。

(1)配平反应方程式并回答问题,用单线桥标出两个反应的电子转移的方向和数目。
反应①:
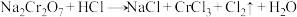 ,
,反应⑥:
 ,
,(2)在上述有编号的步骤中,除了①⑥外,还需用到氧化剂的步骤是
您最近一年使用:0次
【推荐1】
(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________________ 。当1 mol O2发生反应时,还原剂所失电子的物质的量为_________ mol。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是_____________ 。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________ 。
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:

向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_________________ ;该操作将I2还原为I-的目的是________________________ 。
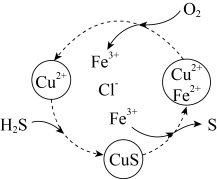
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是________________ 。
(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为________________ ,反应消耗1 mol NaBH4时转移的电子数目为_____________ 。
(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:

向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是

(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】I由FeO、Fe2O3、 Fe3O4 组成的混合物,测得其中铁元素与氧元素的质量比为21:8 ,则这种混合物中FeO、Fe2O3、 Fe3O4 的物质的之比可能为_______ 。
A.1:2:1 B.1:1:1 C.2:1:1 D.1:1:2
II常温下KMnO4氧化浓HCI的反应方程式如下: 2KMnO4 +16HCl (浓) =2KCI+ 2MnCl2十5CI2↑+8H20
(1)用“双线桥法”标明反应中电子转移的方向和数目_______ 。
(2)又已知MnO2 + 4HCI(浓) MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:
MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:______ 。
(3)若有63.2g高锰酸钾参加反应,则被氧化的HCI的物质的量为______ mol,产
生的Cl2在标准状况下的体积______ L。
A.1:2:1 B.1:1:1 C.2:1:1 D.1:1:2
II常温下KMnO4氧化浓HCI的反应方程式如下: 2KMnO4 +16HCl (浓) =2KCI+ 2MnCl2十5CI2↑+8H20
(1)用“双线桥法”标明反应中电子转移的方向和数目
(2)又已知MnO2 + 4HCI(浓)
 MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:
MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:(3)若有63.2g高锰酸钾参加反应,则被氧化的HCI的物质的量为
生的Cl2在标准状况下的体积
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】2010年8月7日甘肃舟曲发生特大泥石流灾害,专家指出,为防止大灾过后瘟疫发生,可用含氯消毒剂和过氧化物对环境消毒。
(1)气体二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:_______
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3•3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只作氧化剂的是_______ (填序号)。
A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温下于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子数是_______ 。
(4)物质的标准生成热是指由稳定的单质生成1mol指定物质时的热效应。如H2O(l)的生成热为-285.8 kJ•mol-1,用热化学方程式表示为 H2(g)+1/2O2(g)=H2O(l);△H= -285.8 kJ•mol-1。查表知ClO2的标准生成热是+102.5kJ•mol-1,则该反应用热化学方程式表示为_______ 。
(1)气体二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3•3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只作氧化剂的是
A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温下于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子数是
(4)物质的标准生成热是指由稳定的单质生成1mol指定物质时的热效应。如H2O(l)的生成热为-285.8 kJ•mol-1,用热化学方程式表示为 H2(g)+1/2O2(g)=H2O(l);△H= -285.8 kJ•mol-1。查表知ClO2的标准生成热是+102.5kJ•mol-1,则该反应用热化学方程式表示为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】硼及硼的化合物有着广泛的用途。请回答下列问题:
(1)已知硼既能与酸又能与碱反应,化学性质类似于铝,请写出硼与氢氧化钠反应的化学方程式___ ;
(2)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构____________ (填“相同”或“不相同”)。
②B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为_______ L。
(3)已知H3BO3是一种白色片状晶体,微溶于水,它的的电离类似于Al(OH)3,可用于制备储氢材料NaBH4涉及的主要反应为:
I.H3BO3+3CH3OH→B(OCH3)3+3H2O II.B(OCH3)3+4NaH→NaBH4+3CH3ONa
①H3BO3为____ (填“一元”、“二元”或“三元”)酸
②B(OCH3)3属于_____ (填序号)类。
A.烃 B.醇 C.酯 D.羧酸
③在碱性条件下,NaBH4与CuSO4溶液反应可得Cu和Na[B(OH)4],其中H元素由-1价升高为+1价,该反应的离子方程式为__ 。
(1)已知硼既能与酸又能与碱反应,化学性质类似于铝,请写出硼与氢氧化钠反应的化学方程式
(2)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构
②B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为
(3)已知H3BO3是一种白色片状晶体,微溶于水,它的的电离类似于Al(OH)3,可用于制备储氢材料NaBH4涉及的主要反应为:
I.H3BO3+3CH3OH→B(OCH3)3+3H2O II.B(OCH3)3+4NaH→NaBH4+3CH3ONa
①H3BO3为
②B(OCH3)3属于
A.烃 B.醇 C.酯 D.羧酸
③在碱性条件下,NaBH4与CuSO4溶液反应可得Cu和Na[B(OH)4],其中H元素由-1价升高为+1价,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】H2S是严重危害环境的气体,采取多种方法减少H2S的排放并加以资源利用。
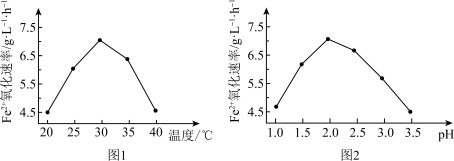
(1)用Fe2(SO4)3吸收H2S。在配制硫酸铁溶液时需要向溶液中加入一定量的硫酸,其目的是:________________ 。吸收时发生反应的离子方程式为_____________________ 。反应后的溶液在硫杆菌作用下进行再生,反应为:4FeSO4+O2+2H2SO4==2Fe2(SO4)3+2H2O。
图1、图2为再生时Fe2+的转化速率与反应条件的关系。再生的最佳条件为_______________ 。若反应温度过高,反应速率下降,其原因是_____________________ 。
(2)在一定条件下,用H2O2氧化H2S。
随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的化学式为________________ 。
(3)H2S与CO2在高温下反应可生成氧硫化碳(COS),其结构式为________________ 。
(4)加热条件下用O2氧化H2S,使硫元素转化为硫单质并回收,写出氧气氧化硫化氢的反应方程式:______ 。
(1)用Fe2(SO4)3吸收H2S。在配制硫酸铁溶液时需要向溶液中加入一定量的硫酸,其目的是:
图1、图2为再生时Fe2+的转化速率与反应条件的关系。再生的最佳条件为
(2)在一定条件下,用H2O2氧化H2S。
随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的化学式为
(3)H2S与CO2在高温下反应可生成氧硫化碳(COS),其结构式为
(4)加热条件下用O2氧化H2S,使硫元素转化为硫单质并回收,写出氧气氧化硫化氢的反应方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,请回答下列问题:
(1)该电池放电时生成+3价铁的化合物,则电池放电时正极的电极反应式为____________________ ;
(2)完成制备电池正极材料过程中某一反应的化学方程式:
________ FeCl3+________ NaOH+________ NaClO=________ Na2FeO4+________ +________
(3)FeO42-具有强氧化性,在其钾盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式为____________________ 。
(1)该电池放电时生成+3价铁的化合物,则电池放电时正极的电极反应式为
(2)完成制备电池正极材料过程中某一反应的化学方程式:
(3)FeO42-具有强氧化性,在其钾盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】防治环境污染,改善生态环境已成为全球的共识。
(1)向煤中加入石灰石作为脱硫剂,可以减少燃烧产物SO2的排放,生成CaSO4。写出SO2减少的化学方程式:___________________________________________ 。
(2)煤的气化和液化是高效、清洁利用煤炭的重要途径。将焦炭在高温下与水蒸气反应,得到CO和H2,发生该反应的化学方程式为:_______________________________ 。
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成CO2和N2,该反应的化学方程式为:___________________________________ 。
(4)天然水中杂质较多,常需加入明矾、漂白粉等物质处理后才能饮用。其中漂白粉的作用是杀菌消毒,其作用原理可用化学方程式表示为:_________________________ 。
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为______________ ,其中氨水转化Cr3+为Cr(OH)3的离子方程式为____________________________________________ ;该方案处理后的废水中因含有大量________ 元素,直接排放会导致水体富营养化。
(1)向煤中加入石灰石作为脱硫剂,可以减少燃烧产物SO2的排放,生成CaSO4。写出SO2减少的化学方程式:
(2)煤的气化和液化是高效、清洁利用煤炭的重要途径。将焦炭在高温下与水蒸气反应,得到CO和H2,发生该反应的化学方程式为:
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成CO2和N2,该反应的化学方程式为:
(4)天然水中杂质较多,常需加入明矾、漂白粉等物质处理后才能饮用。其中漂白粉的作用是杀菌消毒,其作用原理可用化学方程式表示为:
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为
您最近一年使用:0次
【推荐2】写出下列反应的离子方程式(已知还原性: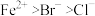 ):
):
(1)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):_________ ;
(2)向 溶液中通入足量
溶液中通入足量 :
:______ ;
(3)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:______ 。
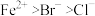 ):
):(1)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):(2)向
 溶液中通入足量
溶液中通入足量 :
:(3)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】硫及其化合物是重要的化学物质。回答下列问题:
(1)二氯化二硫(S2Cl2,无色液体)常用作贵稀金属的萃取剂,遇水会反应,生成S、SO2和刺鼻的酸雾,该反应的化学方程式为___________ ;将干燥的NH3通入S2Cl2的CCl4溶液中,可发生反应: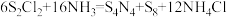 (已知S8是硫单质中最稳定的),该反应中,NH3体现的性质有还原性和
(已知S8是硫单质中最稳定的),该反应中,NH3体现的性质有还原性和___________ 。
(2)将SO2通入含有FeCl3和BaCl2的混合溶液中有白色沉淀产生,其原因是___________ (用离子方程式解释)。
(3)同种反应物,其反应产物与浓度、温度、反应物相对量等因素有关。影响SO2与NaOH反应产物的因素与下列反应相同的是___________ (填字母)。
a.Na与O2反应 b.H2S与O2反应
c.FeBr2溶液与Cl2反应 d.Fe与稀硝酸反应
(4)SOCl2(遇水产生刺激性气味的气体)是有机合成的氯化剂,与NaOH溶液反应可生成三种钠盐,写出三种钠盐的化学式:___________ 。
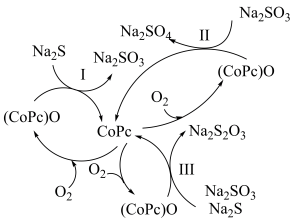
(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为Na2S),可用如图所示转化方式除去。
①当反应I和Ⅱ转移电子数相等时,还原剂的物质的量之比为___________ 。
②已知反应Ⅲ中Na2S与Na2SO3按等物质的量反应,反应的化学方程式为___________ (反应物有H2O参与)。
(1)二氯化二硫(S2Cl2,无色液体)常用作贵稀金属的萃取剂,遇水会反应,生成S、SO2和刺鼻的酸雾,该反应的化学方程式为
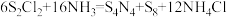 (已知S8是硫单质中最稳定的),该反应中,NH3体现的性质有还原性和
(已知S8是硫单质中最稳定的),该反应中,NH3体现的性质有还原性和(2)将SO2通入含有FeCl3和BaCl2的混合溶液中有白色沉淀产生,其原因是
(3)同种反应物,其反应产物与浓度、温度、反应物相对量等因素有关。影响SO2与NaOH反应产物的因素与下列反应相同的是
a.Na与O2反应 b.H2S与O2反应
c.FeBr2溶液与Cl2反应 d.Fe与稀硝酸反应
(4)SOCl2(遇水产生刺激性气味的气体)是有机合成的氯化剂,与NaOH溶液反应可生成三种钠盐,写出三种钠盐的化学式:
(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为Na2S),可用如图所示转化方式除去。

①当反应I和Ⅱ转移电子数相等时,还原剂的物质的量之比为
②已知反应Ⅲ中Na2S与Na2SO3按等物质的量反应,反应的化学方程式为
您最近一年使用:0次



