恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:2NH3(g) N2(g)+3H2(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是
N2(g)+3H2(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是
 N2(g)+3H2(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是
N2(g)+3H2(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是| 编号 | 时间/min c(NH3)/(10-3 mol/L) 表面积/cm2 | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
| A.相同条件下,增加氨气的浓度,反应速率增大 |
| B.实验②,40min时,v正(NH3)= v逆(NH3) |
| C.实验③达到平衡后,N2的体积分数约为32.7% |
| D.实验③,0~40min,v(N2)=2. 00×10-5mol /(L·min) |
更新时间:2024-01-13 18:21:17
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
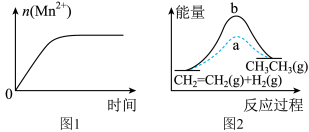
| A.如图1表示10 mL0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 |
| B.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| C.硫酸铁和二氧化锰均可作为过氧化氢分解的催化剂 |
| D.如图2中a、b曲线分别表示反应CH2=CH2(g) + H2(g)→ CH3CH3(g) ΔH< 0使用和未使用催化剂时,反应过程中的能量变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作能达到相应目的的是
| 选项 | 实验操作 | 目的 |
| A | 向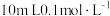 草酸溶液中分别滴加 草酸溶液中分别滴加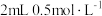 酸性 酸性 溶液、 溶液、 酸性 酸性 溶液 溶液 | 探究浓度对反应速率的影响 |
| B | 分别用pH计测定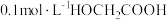 溶液在25℃、45℃时的pH 溶液在25℃、45℃时的pH | 探究温度对电离平衡的影响 |
| C | 常温下,将铁片、铜片插入浓硝酸中构成原电池,并连接电流计 | 探究原电池中较活泼金属为负极 |
| D | 向等物质的量浓度的 和 和 混合液中滴加 混合液中滴加 溶液 溶液 | 探究 和 和 的溶度积大小 的溶度积大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在加热、催化剤作用下2SO2(g)+O2(g) 2SO3(g)下列说法不正确的是( )
2SO3(g)下列说法不正确的是( )
 2SO3(g)下列说法不正确的是( )
2SO3(g)下列说法不正确的是( )| A.在相同条件下,该反应中分别用SO2和O2表示的v,数值不同,但该反应的快慢程度是一致的 |
| B.该反应加入催化剂的目的是为了加快反应速率 |
| C.为了提高SO2的转化率,减少污染物的排放,常常在实际生产中,O2和SO2的投入量之比大于1:2 |
| D.在密闭容器中,投入2 mol SO2和l mol O2,反应结束时生成的2 mol SO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向 20mL0.40mol·L-1H2O2 溶液中加入少量 KI 溶液,反应历程是:ⅰ.H2O2+I-=H2O+IO﹣;ⅱ.H2O2+IO﹣=H2O+O2↑+I﹣。H2O2分解反应过程中能量变化和不同时刻测得生成 O2 的体积(已折算为标准状况)如下图所示。
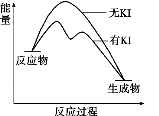
下列说法不正确的是
| t/min | 0 | 5 | 10 | 15 | 20 |
| V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |

下列说法不正确的是
| A.KI 是 H2O2 分解反应的催化剂 |
| B.KI 的加入改变了 H2O2 分解反应的反应历程 |
| C.KI 的加入降低了反应的活化能,因此提高了反应速率 |
| D.0~10min 的平均反应速率:v(H2O2)≈4.0×10-3mol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在容积均为1L的密闭容器中,分别进行水的催化分解实验: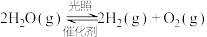
 ,水蒸气的浓度
,水蒸气的浓度 随时间
随时间 的变化如表所示:
的变化如表所示:
下列说法不正确 的是
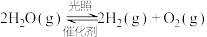
 ,水蒸气的浓度
,水蒸气的浓度 随时间
随时间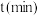 的变化如表所示:
的变化如表所示:| 序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min |
| ① |  | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② |  | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ |  | 0.100 | 0.0960 | 0.0930 | 0.0900 | 0.0900 | 0.0900 |
A.实验①比实验③达到平衡所需时间长,则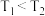 |
B.实验③前 的平均反应速率 的平均反应速率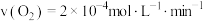 |
C.实验②中,若在 时再充入 时再充入 ,水的平衡转化率减少 ,水的平衡转化率减少 |
D.实验③中,若在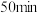 时同时充入 时同时充入 和 和 ,则此时 ,则此时 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知NO2和N2O4可以相互转化2NO2(g) N2O4(g),反应每生成l mol N2O4,放出24.2 kJ的热量。在恒温条件下,将一定量的NO2和N2O4混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图,下列说法正确的是
N2O4(g),反应每生成l mol N2O4,放出24.2 kJ的热量。在恒温条件下,将一定量的NO2和N2O4混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图,下列说法正确的是
 N2O4(g),反应每生成l mol N2O4,放出24.2 kJ的热量。在恒温条件下,将一定量的NO2和N2O4混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图,下列说法正确的是
N2O4(g),反应每生成l mol N2O4,放出24.2 kJ的热量。在恒温条件下,将一定量的NO2和N2O4混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图,下列说法正确的是
| A.前10 min内用v(NO2)表示的化学反应速率为0.02 mol/(L·min) |
| B.图中a、b、c、d四个点中,a、c两点的v正≠v逆 |
| C.反应进行到10 min时放出的热量为9.68 kJ |
| D.25 min时, 导致物质浓度变化的原因是将密闭容器的体积缩小为1 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
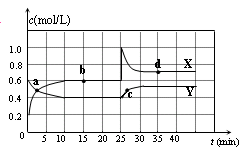
【推荐1】固定容积为2 L的密闭容器中发生反应xA(g)+yB(g)  zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是

 zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是

| A.200℃时,反应从开始到平衡的平均反应速率v(A)=0.08 mol·L-1·min-1 |
B.若0~5 min时容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A + B  C ΔH = +5m kJ/mol C ΔH = +5m kJ/mol |
| C.200℃时,若在第6 min再向体系中加入1molAr,A的转化率不变 |
| D.200℃时,平衡后再充入2 mol B和2 mol C时,v正>v逆 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
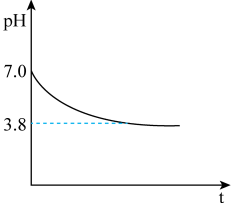
【推荐2】重铬酸钾(K2Cr2O7)有强氧化性,溶液中存在平衡:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+。取2.94 g重铬酸钾橙红色晶体,溶于100 mL水的同时利用数字传感器测定pH变化如图。下列说法正确的是
+2H+。取2.94 g重铬酸钾橙红色晶体,溶于100 mL水的同时利用数字传感器测定pH变化如图。下列说法正确的是
 +H2O⇌2CrO
+H2O⇌2CrO +2H+。取2.94 g重铬酸钾橙红色晶体,溶于100 mL水的同时利用数字传感器测定pH变化如图。下列说法正确的是
+2H+。取2.94 g重铬酸钾橙红色晶体,溶于100 mL水的同时利用数字传感器测定pH变化如图。下列说法正确的是
A.该溶液中含有Cr2O 离子数目为 0.01NA 离子数目为 0.01NA |
| B.Cr元素位于d区,基态原子有4个未成对电子 |
C.Cr2O +H2O⇌2CrO +H2O⇌2CrO +2H+的平衡常数K约为10-14.2 +2H+的平衡常数K约为10-14.2 |
| D.升高温度,溶液橙红色变浅,则该转化反应ΔH<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】硫化氢(H2S)是一种有毒气体,广泛存在于石油化工、冶金等行业的废气中,常用足量纯碱溶液吸收法、热分解法、Fe2(SO4)3溶液氧化脱除法、活性炭吸附氧化法脱除。同时,H2S也是一种重要的化工原料,可以用来制备硫磺、苯硫酚(C6H5SH)、H2S、NaHS还常用于脱除水体中的Cu2+,形成黑色、不溶于稀硫酸的CuS沉淀。H2S可以在高温下与氯苯(C6H5Cl)反应制备苯硫酚(C6H5SH),同时得到副产物苯(C6H6),发生反应的热化学方程式为:
反应I:C6H5Cl(g)+H2S(g) C6H5SH(g)+HCl(g) △H1
C6H5SH(g)+HCl(g) △H1
反应II: C6H5Cl(g)+H2S(g)=C6H6(g)+HCl(g)+ S8(g) △H2= - 45.8 kJ/mol
S8(g) △H2= - 45.8 kJ/mol
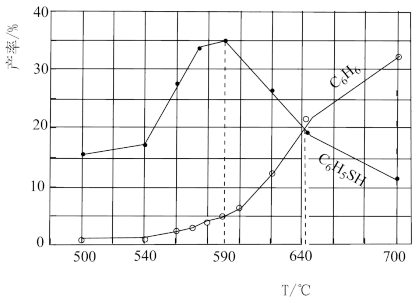
将H2S与C6H5Cl(体积比5:2)加入某恒容密闭容器中,反应20 min后测得混合气中C6H5SH和C6H6的产率(实际产量与理论产量之比)与温度的关系如图所示。下列说法不正确的是
反应I:C6H5Cl(g)+H2S(g)
 C6H5SH(g)+HCl(g) △H1
C6H5SH(g)+HCl(g) △H1反应II: C6H5Cl(g)+H2S(g)=C6H6(g)+HCl(g)+
 S8(g) △H2= - 45.8 kJ/mol
S8(g) △H2= - 45.8 kJ/mol将H2S与C6H5Cl(体积比5:2)加入某恒容密闭容器中,反应20 min后测得混合气中C6H5SH和C6H6的产率(实际产量与理论产量之比)与温度的关系如图所示。下列说法不正确的是

| A.由图可知△H1<0 |
| B.在500℃时,反应II处于平衡状态 |
C.在590℃时,反应I的平衡常数为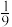 |
| D.在645℃时,延长反应时间,会提高C6H6的产率 |
您最近一年使用:0次



