下图是元素周期表前三周期,根据图中字母所代表元素,回答下列问题:
(1)化合物 ,
, 和
和 热稳定性最高的是
热稳定性最高的是___________ ,(填化学式,下同)酸性最强的是___________ 。
(2)元素d能分别与元素a和f均按原子个数比1:2形成化合物丙和红棕色气体丁,常温下,液体丙和气体丁反应生成两种无污染的物质,该反应的氧化产物与还原产物的质量之比为___________ 。
(3)在元素周期表中相邻周期位于“左上和右下对角线位置”的元素往往性质相似,根据g的性质可以推测b的性质,b在由f组成的双原子分子中加热得到主要产物为___________ (填化学式),b的碳酸盐与足量盐酸反应的离子反应方程式为 ___________ 。
(4)下列关于原子结构和元素周期表说法正确的有___________
a. 、
、 、
、 互为同素异形体
互为同素异形体
b.三种氢核素与O可组成9种不同组成的水分子
c.第二、三周期上下相邻的元素的原子核外电子数相差8
d. 的中子数与电子数相差17
的中子数与电子数相差17
a | ||||||||
b | c | d | f | h | ||||
g | i | j | ||||||
 ,
, 和
和 热稳定性最高的是
热稳定性最高的是(2)元素d能分别与元素a和f均按原子个数比1:2形成化合物丙和红棕色气体丁,常温下,液体丙和气体丁反应生成两种无污染的物质,该反应的氧化产物与还原产物的质量之比为
(3)在元素周期表中相邻周期位于“左上和右下对角线位置”的元素往往性质相似,根据g的性质可以推测b的性质,b在由f组成的双原子分子中加热得到主要产物为
(4)下列关于原子结构和元素周期表说法正确的有
a.
 、
、 、
、 互为同素异形体
互为同素异形体b.三种氢核素与O可组成9种不同组成的水分子
c.第二、三周期上下相邻的元素的原子核外电子数相差8
d.
 的中子数与电子数相差17
的中子数与电子数相差17
更新时间:2024-01-10 22:32:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】已知无水 在空气中遇水易潮解变质,加热易升华。实验室拟通过氯气与铁的反应来制备
在空气中遇水易潮解变质,加热易升华。实验室拟通过氯气与铁的反应来制备 。
。
(1)利用表中实验装置,不能达到相应实验目的的是图___________ 。
(2)图甲中盛装浓盐酸的仪器的名称是___________ ;将仪器连接好以后,必须进行的第一步操作是___________ 。
(3)图丙的试管中可观察到的实验现象为___________ 。
(4)图丁中浓硫酸的作用是___________ ,装有NaOH溶液(过量)的试剂瓶中发生反应的离子方程式为___________ 。
(5)电子工业常用30%的 溶液蚀刻绝缘板上的铜箔,制造印刷电路板。写出
溶液蚀刻绝缘板上的铜箔,制造印刷电路板。写出 溶液与金属铜发生反应的离子方程式:
溶液与金属铜发生反应的离子方程式:___________ 。
(6)高铁酸钠是一种新型绿色消毒剂,主要用于处理饮用水。可以通过反应: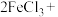
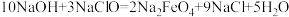 制取。该反应中氧化剂是
制取。该反应中氧化剂是___________ (填化学式,下同),氧化产物为___________ 。
 在空气中遇水易潮解变质,加热易升华。实验室拟通过氯气与铁的反应来制备
在空气中遇水易潮解变质,加热易升华。实验室拟通过氯气与铁的反应来制备 。
。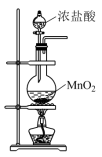 |  | 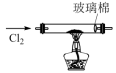 | 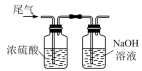 |
图甲:制备 | 图乙:净化 | 图丙: 与铁反应 与铁反应 | 图丁:尾气处理 |
(2)图甲中盛装浓盐酸的仪器的名称是
(3)图丙的试管中可观察到的实验现象为
(4)图丁中浓硫酸的作用是
(5)电子工业常用30%的
 溶液蚀刻绝缘板上的铜箔,制造印刷电路板。写出
溶液蚀刻绝缘板上的铜箔,制造印刷电路板。写出 溶液与金属铜发生反应的离子方程式:
溶液与金属铜发生反应的离子方程式:(6)高铁酸钠是一种新型绿色消毒剂,主要用于处理饮用水。可以通过反应:
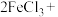
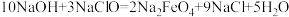 制取。该反应中氧化剂是
制取。该反应中氧化剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某小组将浓盐酸和 混合加热生成氯气,发现氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气,发现氯气不再逸出时,固液混合物A中仍存在盐酸和 ,回答下列问题。
,回答下列问题。
(1)写出反应中生成氯气的离子方程式___________ 。
(2)一个氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应),第(1)题中的离子方程式可分为下面两个反应式:
i.氧化反应: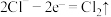
ii.还原反应:_______
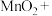 ___________
___________ ___________
___________
(3)根据两个半反应的反应式,分析A中仍存在盐酸和 的原因。
的原因。
i.随 降低,
降低, 还原性减弱
还原性减弱
ii.随 降低或
降低或 浓度升高,
浓度升高,___________ 。
(4)补充实验证实了(3)中的分析。
a是___________ ,b是___________ 。
(5)利用 浓度对
浓度对 氧化性的影响,探究同周期非金属元素阴离子的还原性。相同浓度的NaCl和
氧化性的影响,探究同周期非金属元素阴离子的还原性。相同浓度的NaCl和 溶液,能与
溶液,能与 反应所需
反应所需 较小的是
较小的是___________ 。
(6)该小组查资料得知:氧化还原反应电位传感器可以测量不同溶液的电位值。根据电位值大小可比较物质的氧化性或者还原性强弱:数值越大,氧化性越强;数值越小,还原性越强。由此推知 的以下物质溶液的电位值大小(填“<”“>”或“=”)
的以下物质溶液的电位值大小(填“<”“>”或“=”)
①KI___________ KBr
②
___________  (酸化)
(酸化)
 混合加热生成氯气,发现氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气,发现氯气不再逸出时,固液混合物A中仍存在盐酸和 ,回答下列问题。
,回答下列问题。(1)写出反应中生成氯气的离子方程式
(2)一个氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应),第(1)题中的离子方程式可分为下面两个反应式:
i.氧化反应:
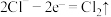
ii.还原反应:
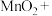 ___________
___________ ___________
___________(3)根据两个半反应的反应式,分析A中仍存在盐酸和
 的原因。
的原因。i.随
 降低,
降低, 还原性减弱
还原性减弱ii.随
 降低或
降低或 浓度升高,
浓度升高,(4)补充实验证实了(3)中的分析。
| 实验操作 | 试剂 | 产物 | |
| I | 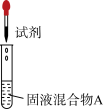 | 较浓 | 有氯气 |
| Ⅱ | a | 有氯气 | |
| Ⅲ | a和b | 无氯气 |
(5)利用
 浓度对
浓度对 氧化性的影响,探究同周期非金属元素阴离子的还原性。相同浓度的NaCl和
氧化性的影响,探究同周期非金属元素阴离子的还原性。相同浓度的NaCl和 溶液,能与
溶液,能与 反应所需
反应所需 较小的是
较小的是(6)该小组查资料得知:氧化还原反应电位传感器可以测量不同溶液的电位值。根据电位值大小可比较物质的氧化性或者还原性强弱:数值越大,氧化性越强;数值越小,还原性越强。由此推知
 的以下物质溶液的电位值大小(填“<”“>”或“=”)
的以下物质溶液的电位值大小(填“<”“>”或“=”)①KI
②

 (酸化)
(酸化)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ、中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是高效、安全的杀菌消毒剂。
(1)漂白粉主要用于游泳池水等的杀菌和消毒,久置空气中会呈稀粥状而失去漂白作用,用化学方程式表示漂白粉在空气中失效的原因________________________________ 。84消毒液是一种家用消毒剂,不能用于钢制器具的消毒,原因是NaClO具有____ 性。
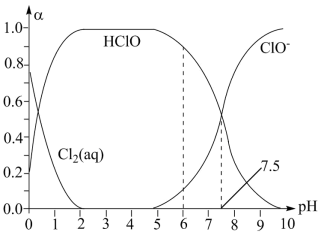
(2)新制氧水常用于杀菌消毒,在25°C时将氧气溶于水形成氯气-氯水体系。该体系中Cl2(aq)、HClO和ClO-的物质的量分数(a)能pH变化的关系如图所示。由图分析,用氯气处理饮用水时,pH=6 与pH=7.5两种情况下,pH=____ 时杀菌效果强。 当pH=7.5时,氯水中含氯元素的微粒有HClO、 ClO-和_______ 。
ClO2是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
(3)根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业上常用NaClO3溶液和Na2SO3溶液混合并加入H2SO4酸化制得ClO2且产物中有Na2SO4,则在该反应中,氧化产物和还原产物的物质的量之比为______ 。
(4)已知C1O2在进行饮用水消毒时转化为Cl-,则ClO2与Cl2的消毒能力之比为______ (写最简整数比,消毒能力用单位质量清毒剂得电子多少来衡量)
Ⅱ、化学方法在文物保护中有重要作用,某博物馆修复出土铁器的部分过程如下:
(5)检测锈蚀产物主要成分的化学式为Fe3O4、Fe2O3 •H2O、FeO(OH)、 FeOCl,由产物可推测,铁器可能与____________________ (填2种反应物化学式)发生反应而被腐蚀。
分析认为,铁经过了如下腐蚀循环:
Ⅰ. Fe转化为Fe2+;
Ⅱ. Fe2+在自然环境中形成FeO(OH);
Ⅲ. FeO(OH)和 Fe2+反应形成致密的Fe3O4保护层;
Ⅳ. Fe3O4保护层转化为FeO(OH),如此往复腐蚀。
(6)FeOCl中铁的化合价为___ ;上述反应中是氧化还原反应的为_______ (填序号)。
(7)FeO(OH)和Fe2+反应的离子方程式为______________________ 。
(8)Ⅳ反应为Fe3O4+O2+H2O→FeO(OH),还原剂为________ ,每反应 1mol还原剂,转移电子_____ mol。
(1)漂白粉主要用于游泳池水等的杀菌和消毒,久置空气中会呈稀粥状而失去漂白作用,用化学方程式表示漂白粉在空气中失效的原因
(2)新制氧水常用于杀菌消毒,在25°C时将氧气溶于水形成氯气-氯水体系。该体系中Cl2(aq)、HClO和ClO-的物质的量分数(a)能pH变化的关系如图所示。由图分析,用氯气处理饮用水时,pH=6 与pH=7.5两种情况下,pH=

ClO2是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
(3)根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业上常用NaClO3溶液和Na2SO3溶液混合并加入H2SO4酸化制得ClO2且产物中有Na2SO4,则在该反应中,氧化产物和还原产物的物质的量之比为
(4)已知C1O2在进行饮用水消毒时转化为Cl-,则ClO2与Cl2的消毒能力之比为
Ⅱ、化学方法在文物保护中有重要作用,某博物馆修复出土铁器的部分过程如下:
(5)检测锈蚀产物主要成分的化学式为Fe3O4、Fe2O3 •H2O、FeO(OH)、 FeOCl,由产物可推测,铁器可能与
分析认为,铁经过了如下腐蚀循环:
Ⅰ. Fe转化为Fe2+;
Ⅱ. Fe2+在自然环境中形成FeO(OH);
Ⅲ. FeO(OH)和 Fe2+反应形成致密的Fe3O4保护层;
Ⅳ. Fe3O4保护层转化为FeO(OH),如此往复腐蚀。
(6)FeOCl中铁的化合价为
(7)FeO(OH)和Fe2+反应的离子方程式为
(8)Ⅳ反应为Fe3O4+O2+H2O→FeO(OH),还原剂为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语 回答下列问题:
(1)元素⑨在元素周期表中的位置为_______ 。
(2)①、④、⑧三种元素按物质的量为1:1:1形成的化合物,写出该化合物的结构式_______ 。
(3)由②③④三种元素的原子按1:1:1构成负一价阴离子,利用等电子原理,写出该离子的电子式_______ 。
(4)①③形成的化合物极易溶于水,主要原因是_______ 。
(5)下列说法一定正确的是_______ 。
a.④、⑤、⑥的简单离子半径由大到小的顺序为④>⑤>⑥
b.②、③、⑦的含氧酸的酸性由强到弱的顺序为③>②>⑦
c.元素⑨位于元素周期表d区
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
| ⑨ |
(2)①、④、⑧三种元素按物质的量为1:1:1形成的化合物,写出该化合物的结构式
(3)由②③④三种元素的原子按1:1:1构成负一价阴离子,利用等电子原理,写出该离子的电子式
(4)①③形成的化合物极易溶于水,主要原因是
(5)下列说法一定正确的是
a.④、⑤、⑥的简单离子半径由大到小的顺序为④>⑤>⑥
b.②、③、⑦的含氧酸的酸性由强到弱的顺序为③>②>⑦
c.元素⑨位于元素周期表d区
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表为长式周期表的一部分,其中的编号代表对应的元素。请回答下列问题:

(1)表中属于ds区元素的是_______ (填元素符号)。
(2)③和⑦形成的一种常见溶剂的立体构型为_______ 。
(3)某元素原子的价层电子排布式为nsnnpn+1,该元素原子的未成对电子数为_______ ,该元素与元素①所形成化合物的水溶液显_______ (填“酸”或“碱”)。
(4)元素④的第一电离能_______ 元素⑤(填“>”、“=”、“<”,下同)的第一电离能;元素⑥的电负性_______ 元素⑦的电负性。
(5)元素⑨的基态原子核外电子排布式是_______ 。

(1)表中属于ds区元素的是
(2)③和⑦形成的一种常见溶剂的立体构型为
(3)某元素原子的价层电子排布式为nsnnpn+1,该元素原子的未成对电子数为
(4)元素④的第一电离能
(5)元素⑨的基态原子核外电子排布式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】几种元素在周期表中的位置如图所示,用化学用语(特殊标记的除外)回答下列问题:

(1)表中所列元素含三种金属元素,其中金属性最弱的元素所在周期表中的位置是______________ 。
(2)①有多种单质存在,如足球烯、金刚石等,它们之间互称为___________ 。
(3)⑦和⑨形成的化合物为离子化合物,用电子式表示该化合物的形成过程______________________ 。
(4)③和④的最高价氧化物对应的水化物之间反应的的离子方程式为______________________ 。
(5)元素⑤⑥⑦的最高价氧化物对应的水化物,按酸性从强到弱的顺序排列是______________________ (用化学式表示)。
(6)已知 与浓盐酸在常温下反应生成氯气,利用如图装置验证⑧和⑩两种元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证⑧和⑩两种元素的非金属性强弱。仪器A的名称为_______ ,仪器B中盛放淀粉-碘化钾溶液,所发生的离子反应方程式为_______________ ,当观察到B中溶液变蓝时,即可证明非金属性较强的元素是氯。


(1)表中所列元素含三种金属元素,其中金属性最弱的元素所在周期表中的位置是
(2)①有多种单质存在,如足球烯、金刚石等,它们之间互称为
(3)⑦和⑨形成的化合物为离子化合物,用电子式表示该化合物的形成过程
(4)③和④的最高价氧化物对应的水化物之间反应的的离子方程式为
(5)元素⑤⑥⑦的最高价氧化物对应的水化物,按酸性从强到弱的顺序排列是
(6)已知
 与浓盐酸在常温下反应生成氯气,利用如图装置验证⑧和⑩两种元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证⑧和⑩两种元素的非金属性强弱。仪器A的名称为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】原子序数依次增大的五种短周期元素X、Y、Z、Q、R,已知X与Q同主族,Y、Z原子序数之比为3:4,Z的最外层电子数是Q的最外层电子数的6倍,R为同周期中原子半径最小的元素(稀有气体元素除外),X与R形成的化合物常温下为气态。
(1)表示Y元素中质子数与中子数相等的同位素符号是 。
(2)Q与Z形成的原子个数比为1:1的化合物的电子式是 。
(3)A+B→C+D+H2O为中学化学中常见的反应形式,A、B、C、D均为由上述五种元素组成的单质或化合物。
①如A为NaOH、B为CO2时,可写成aNaOH + bCO2 = cNa2CO3 + d NaHCO3 + nH2O,a与b的物质的量之比应满足的关系是 。现向l00 mL、3 mol/L的NaOH溶液中缓慢通入标准状况下4.48 L的CO2气体,用l个化学方程式表示以上反应
(化学计量数为最简整数),此时溶液中各种离子物质的量浓度由高到低的排列顺序是_ _。
②请任写一个符合A+B→C+D+H2O形式的氧化还原反应方程式,其中C、D均为盐
。
(1)表示Y元素中质子数与中子数相等的同位素符号是 。
(2)Q与Z形成的原子个数比为1:1的化合物的电子式是 。
(3)A+B→C+D+H2O为中学化学中常见的反应形式,A、B、C、D均为由上述五种元素组成的单质或化合物。
①如A为NaOH、B为CO2时,可写成aNaOH + bCO2 = cNa2CO3 + d NaHCO3 + nH2O,a与b的物质的量之比应满足的关系是 。现向l00 mL、3 mol/L的NaOH溶液中缓慢通入标准状况下4.48 L的CO2气体,用l个化学方程式表示以上反应
(化学计量数为最简整数),此时溶液中各种离子物质的量浓度由高到低的排列顺序是_ _。
②请任写一个符合A+B→C+D+H2O形式的氧化还原反应方程式,其中C、D均为盐
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为______ .
(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是___ .
(3)元素Z能与氢元素形成−1价阴离子,该阴离子的电子总数是___ ,与该离子电子总数相等的Z与氢形成的微粒是___ .
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为___ .
(5)ZW3常温下呈液态,可与水反应生成一种酸和一种碱,反应的化学方程式为___ .
(6)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是___ (用酸的分子式表示).
(1)元素X原子结构示意图为
(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是
(3)元素Z能与氢元素形成−1价阴离子,该阴离子的电子总数是
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为
(5)ZW3常温下呈液态,可与水反应生成一种酸和一种碱,反应的化学方程式为
(6)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水,并将核废水主要辐射物质“氚 ”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。
”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。

(1)下列有关氚的说法正确的是_______。
| A.卡通形象中标“+”号的小球表示中子 | B.氚的核素符号为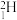 |
| C.氚和及其同位素性质完全相同 | D.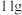 氚水 氚水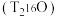 所含中子数为 所含中子数为 |
(2)有关
 和
和 的说法正确的是___________。
的说法正确的是___________。| A.互为同位素 | B.互为同素异形体 |
| C.电子数不同 | D.同温同压下密度之比为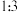 |
(3)在离子
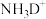 中,电子数、质子数和中子数之比为
中,电子数、质子数和中子数之比为(4)
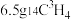 在标况下的体积约为
在标况下的体积约为(5)一个
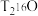 分子的质量是
分子的质量是
您最近一年使用:0次



