电化学知识与我们的生产、生活密切相关。回答下列问题:
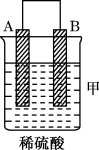
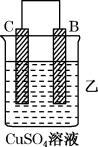
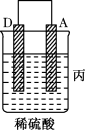
(1)某兴趣小组同学利用氧化还原反应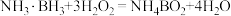 ,设计了如图所示原电池,其中甲、乙两烧杯中各物质的量浓度均为
,设计了如图所示原电池,其中甲、乙两烧杯中各物质的量浓度均为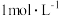 ,盐桥中装有饱和
,盐桥中装有饱和 溶液。
溶液。
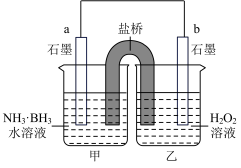
①发生还原反应的烧杯是______ (填“甲”或“乙”)。
②外电路的电流方向:_______ (填“ ”或“
”或“ ”)。
”)。
③电池工作时,盐桥中的 移向
移向_____ (填“甲”或“乙”)烧杯。
④甲烧杯中发生的电极反应式为___________ 。
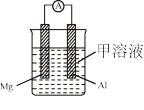
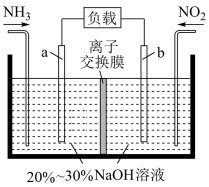
(2)利用反应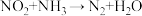 (未配平)消除
(未配平)消除 的简易装置如图所示,电极b的反应式为
的简易装置如图所示,电极b的反应式为___________ ,消耗标准状况下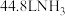 时,被消除的
时,被消除的 的物质的量为
的物质的量为_____  。
。
(1)某兴趣小组同学利用氧化还原反应
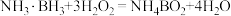 ,设计了如图所示原电池,其中甲、乙两烧杯中各物质的量浓度均为
,设计了如图所示原电池,其中甲、乙两烧杯中各物质的量浓度均为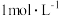 ,盐桥中装有饱和
,盐桥中装有饱和 溶液。
溶液。
①发生还原反应的烧杯是
②外电路的电流方向:
 ”或“
”或“ ”)。
”)。③电池工作时,盐桥中的
 移向
移向④甲烧杯中发生的电极反应式为
(2)利用反应
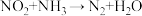 (未配平)消除
(未配平)消除 的简易装置如图所示,电极b的反应式为
的简易装置如图所示,电极b的反应式为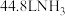 时,被消除的
时,被消除的 的物质的量为
的物质的量为 。
。
更新时间:2024-01-15 22:13:15
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d铜溶于浓硝酸 e氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
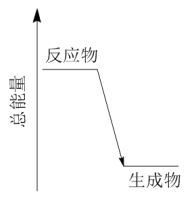
(2) 分解时的能量变化关系如图所示,则
分解时的能量变化关系如图所示,则 分解反应为
分解反应为___________ 反应(选填:吸热、放热)。
查阅资料得知:将作为催化剂的 溶液,加入
溶液,加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:
均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是: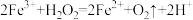 和
和___________ 。
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置:

①电极a为镁,电极b为铝,电解质溶液为氢氧化钠溶液时,该电池的负极为___________ (填名称)。
②若a为Cu,b为石墨,电解质为 溶液,工作时的总反应为
溶液,工作时的总反应为 。写出b电极反应式:
。写出b电极反应式:___________ 。
③质量相同的铜棒和铁棒用导线连接后插入 溶液中,一段时间后取出洗净、干燥、称量,二者质量差为12g,则导线中通过的电子的数目为
溶液中,一段时间后取出洗净、干燥、称量,二者质量差为12g,则导线中通过的电子的数目为___________ 。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d铜溶于浓硝酸 e氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)
 分解时的能量变化关系如图所示,则
分解时的能量变化关系如图所示,则 分解反应为
分解反应为
查阅资料得知:将作为催化剂的
 溶液,加入
溶液,加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:
均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是: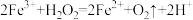 和
和(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置:

①电极a为镁,电极b为铝,电解质溶液为氢氧化钠溶液时,该电池的负极为
②若a为Cu,b为石墨,电解质为
 溶液,工作时的总反应为
溶液,工作时的总反应为 。写出b电极反应式:
。写出b电极反应式:③质量相同的铜棒和铁棒用导线连接后插入
 溶液中,一段时间后取出洗净、干燥、称量,二者质量差为12g,则导线中通过的电子的数目为
溶液中,一段时间后取出洗净、干燥、称量,二者质量差为12g,则导线中通过的电子的数目为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组拟设计如图所示电化学装置探究 和
和 的氧化性强弱(烧杯中溶液体积均为100mL)。
的氧化性强弱(烧杯中溶液体积均为100mL)。

(1)配制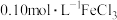 溶液时,先将一定量
溶液时,先将一定量 溶于盛有少量
溶于盛有少量_______ (填试剂名称)的烧杯中,然后进行移液、洗涤、定容等一系列操作。
(2)关闭K,电流表显示电流由银极流向铂极,由此可知银极为_______ 极。
(3)经过 ,测得银极质量净增0.432g,此时左侧溶液中
,测得银极质量净增0.432g,此时左侧溶液中
_______  (不考虑溶液体积变化、水解等因素)。
(不考虑溶液体积变化、水解等因素)。
(4)根据(2)、(3)的实验结果分析,铂极的电极反应式为_______ ;氧化性:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)一段时间后,向铂极附近溶液中加入适量无水 固体,电流表显示电流由铂极流向银极,这说明
固体,电流表显示电流由铂极流向银极,这说明 和
和 的氧化性相对强弱与
的氧化性相对强弱与_______ 有关。
 和
和 的氧化性强弱(烧杯中溶液体积均为100mL)。
的氧化性强弱(烧杯中溶液体积均为100mL)。
(1)配制
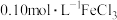 溶液时,先将一定量
溶液时,先将一定量 溶于盛有少量
溶于盛有少量(2)关闭K,电流表显示电流由银极流向铂极,由此可知银极为
(3)经过
 ,测得银极质量净增0.432g,此时左侧溶液中
,测得银极质量净增0.432g,此时左侧溶液中
 (不考虑溶液体积变化、水解等因素)。
(不考虑溶液体积变化、水解等因素)。(4)根据(2)、(3)的实验结果分析,铂极的电极反应式为

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)一段时间后,向铂极附近溶液中加入适量无水
 固体,电流表显示电流由铂极流向银极,这说明
固体,电流表显示电流由铂极流向银极,这说明 和
和 的氧化性相对强弱与
的氧化性相对强弱与
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】任何化学反应都伴随着能量的变化,通过化学反应,化学能可转化为热能、光能、电能等不同形式的能量。
(1)用图甲、乙所示装置进行实验,请回答下列问题:___________ 。
a.甲中锌片是负极,乙中铜片是正极 b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的pH均增大 d.乙中电流由铜片经过导线流向锌片
②若反应过程中有0.4mol电子转移,乙装置中生成的氢气在标况下的体积为___________ 。
(2)Mg,Al设计成如由图所示原电池装置:___________ 极;
②若溶液为氢氧化钠溶液,Mg电极发生的电极反应为___________ 。
(3)CO与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下: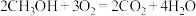 ,则c电极的反应方程式为
,则c电极的反应方程式为___________ ,若线路中转移2mol电子,则上述 燃料电池,消耗的
燃料电池,消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(1)用图甲、乙所示装置进行实验,请回答下列问题:
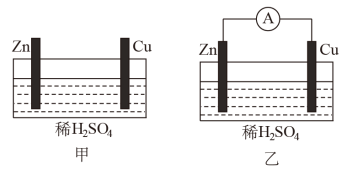
a.甲中锌片是负极,乙中铜片是正极 b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的pH均增大 d.乙中电流由铜片经过导线流向锌片
②若反应过程中有0.4mol电子转移,乙装置中生成的氢气在标况下的体积为
(2)Mg,Al设计成如由图所示原电池装置:
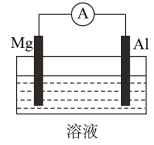
②若溶液为氢氧化钠溶液,Mg电极发生的电极反应为
(3)CO与
 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下: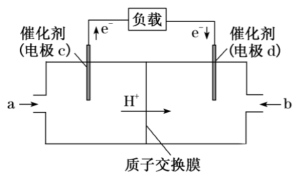
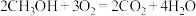 ,则c电极的反应方程式为
,则c电极的反应方程式为 燃料电池,消耗的
燃料电池,消耗的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氨浸菱锌矿制备活性氧化锌,成本低,选择性好,其工艺流程如下:
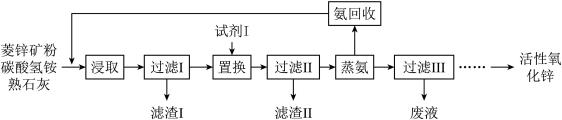
(1)滤渣Ⅰ主要成分的化学式为__________ 。
(2)浸取液中含少量Pb2+、Cu2+等重金属离子,可加入试剂Ⅰ除去,试剂Ⅰ为______________ ,但在实际操作过程中实际加入量远高于理论量,可能的原因是____________________________ 。
(3)过滤Ⅱ 后得到Zn(NH3)4CO3 溶液,经直接蒸汽加热可析出碱式碳酸锌[ZnCO3·2Zn(OH)2·H2O]沉淀,其反应化学方程式为____________________________ 。
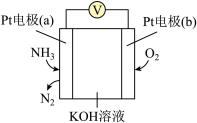
(4)蒸氨过程中会有部分氨气逸出,可用电化学气敏传感器监测环境中NH3 的含量,原理如图所示。负极的电极反应为________________________________ ,假设蒸氨过程中逸出氨气16.8L (标准状况) 进入传感器,另一极需要通入标准状况下O2的体积为____________________ 。
(5)蒸氨完成时,废液中残余氨含量需小于0.2mol/L,如果残余氨浓度过低,蒸汽用量增大,回收氨水中氨浓度降低,不利于循环使用;如果残余氨浓度过高,会导致____________________________ 。

(1)滤渣Ⅰ主要成分的化学式为
(2)浸取液中含少量Pb2+、Cu2+等重金属离子,可加入试剂Ⅰ除去,试剂Ⅰ为
(3)过滤Ⅱ 后得到Zn(NH3)4CO3 溶液,经直接蒸汽加热可析出碱式碳酸锌[ZnCO3·2Zn(OH)2·H2O]沉淀,其反应化学方程式为
(4)蒸氨过程中会有部分氨气逸出,可用电化学气敏传感器监测环境中NH3 的含量,原理如图所示。负极的电极反应为

(5)蒸氨完成时,废液中残余氨含量需小于0.2mol/L,如果残余氨浓度过低,蒸汽用量增大,回收氨水中氨浓度降低,不利于循环使用;如果残余氨浓度过高,会导致
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】应用原电池反应可以探究氧化还原反应进行的方向和程度。现连接如图装置并加入药品(盐桥中的物质不参与反应),进行实验:

i.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ii.随后向U形管左侧逐滴加入浓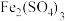 溶液,发现电流表指针的变化依次为偏移减小→回到0刻度→逆向偏移。
溶液,发现电流表指针的变化依次为偏移减小→回到0刻度→逆向偏移。
(1)实验i中银作___________ 极。
(2)综合实验i、ii的现象,得出 和
和 反应的离子方程式是
反应的离子方程式是___________ 。

i.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ii.随后向U形管左侧逐滴加入浓
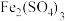 溶液,发现电流表指针的变化依次为偏移减小→回到0刻度→逆向偏移。
溶液,发现电流表指针的变化依次为偏移减小→回到0刻度→逆向偏移。(1)实验i中银作
(2)综合实验i、ii的现象,得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量), 当闭合该装置的电键 K 时,观察到电流计的指针发生了偏转。请回答下列问题:
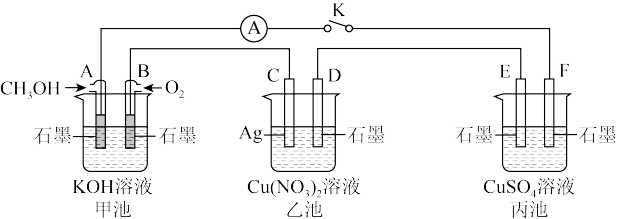
(1)乙池为_____ (填“原电池”、“电解池”或“电镀池”),B 电极的电极反应式为____ 。
(2)丙池中 E 电极为____ (填“正极”、“负极”、“阴极”或“阳极”),电极的电极反应式为____ 。该池总反应的化学方程式为____ 。
(3)当乙池中 C 极质量减轻 54 g 时,甲池中 B 电极理论上消耗 O2的为____ L(标准状况)。
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是____ (填选项字母)。
A Cu B CuO C Cu(OH)2 D Cu2(OH)2CO3

(1)乙池为
(2)丙池中 E 电极为
(3)当乙池中 C 极质量减轻 54 g 时,甲池中 B 电极理论上消耗 O2的为
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是
A Cu B CuO C Cu(OH)2 D Cu2(OH)2CO3
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】能源的开发和利用是当前科学研究的重要课题。
(1)原电池是将_____ 能转化为_____ 能的装置。
(2)下列不能用于设计成原电池的化学反应是_____ ,理由是_____ 。
A.2HCl+CaO=CaCl2+H2O
B.2CH3OH+3O2=2CO2+4H2O
C.4Fe(OH)2+2H2O+O2=4Fe(OH)3
D.2H2+O2=2H2O
(3)甲烷是天然气的主要成分。
①写出CH4燃烧的化学方程式_____ 。
②25℃,100kPa时生成或断裂1mol化学键所放出或吸收的能量称为键能。已知键能数据如下:
计算1mol甲烷完全燃烧放出的热量为_____ kJ。
(4)为提高能量转化效率,常将甲烷设计成燃料电池,装置示意图如图(其中A、B为石墨电极)。
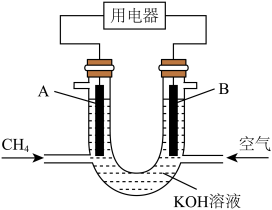
①B是该电池的_____ (填“正”或“负”)极。CH4在该装置中的作用是_____ ,KOH溶液的作用是_____ 。
②已知甲烷与氧气完全氧化时每生成1mol液态水释放能量约为400kJ,又知该甲烷燃料电池每发1kW·h电能生成216g水,则该电池的能量转化率为_____ (1kW·h=3.6×106J)。
(1)原电池是将
(2)下列不能用于设计成原电池的化学反应是
A.2HCl+CaO=CaCl2+H2O
B.2CH3OH+3O2=2CO2+4H2O
C.4Fe(OH)2+2H2O+O2=4Fe(OH)3
D.2H2+O2=2H2O
(3)甲烷是天然气的主要成分。
①写出CH4燃烧的化学方程式
②25℃,100kPa时生成或断裂1mol化学键所放出或吸收的能量称为键能。已知键能数据如下:
| 化学键 | C-H | O=O | C=O | O-H |
| 键能/kJ·mol-1 | 414 | 497 | 803 | 463 |
(4)为提高能量转化效率,常将甲烷设计成燃料电池,装置示意图如图(其中A、B为石墨电极)。

①B是该电池的
②已知甲烷与氧气完全氧化时每生成1mol液态水释放能量约为400kJ,又知该甲烷燃料电池每发1kW·h电能生成216g水,则该电池的能量转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】2022年2月在北京举办了冬季奥运会,冬奥会奖牌是金镶玉材料,而玉的成分是硅酸盐和二氧化硅,回答下面问题:
(1)向硅酸钠溶液中通入少量CO2,生成一种凝胶硅酸,写出反应的离子方程式:___________ 。此实验可以证明碳元素的非金属性___________ (填“大于”或“小于”)硅元素。
(2)碳纳米材料是一种新型无机非金属材料,下面不属于新型无机非金属材料的是___________。
(3)举办冬奥会需要低温环境,而氨气是一种很好的制冷剂。
①写出氨气的电子式___________ 。
②写出实验室制备氨气的化学方程式___________ 。
(4)北京冬奥会基本实现100%绿电供应和碳中和,利用 和
和 在光催化酶作用下可以高效合成甲醇
在光催化酶作用下可以高效合成甲醇 。
。
①写出甲醇燃烧的化学方程式:___________ ,该反应是___________ (填“吸热”或“放热”)反应。
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是___________ 极,b电极发生的电极反应式是___________ 。外电路中有电子流入的是___________ (填“a”或“b”)极。
③将上图中的 改为甲醇就构成了碱性甲醇燃料电池,其中发生还原反应的电极是
改为甲醇就构成了碱性甲醇燃料电池,其中发生还原反应的电极是___________ (填“a”或“b”)极,a电极发生的电极反应式是___________ 。
(1)向硅酸钠溶液中通入少量CO2,生成一种凝胶硅酸,写出反应的离子方程式:
(2)碳纳米材料是一种新型无机非金属材料,下面不属于新型无机非金属材料的是___________。
| A.碳纳米管 | B.石墨烯 | C.超导电动陶瓷 | D.滑雪刀刃用铬钼钢 |
①写出氨气的电子式
②写出实验室制备氨气的化学方程式
(4)北京冬奥会基本实现100%绿电供应和碳中和,利用
 和
和 在光催化酶作用下可以高效合成甲醇
在光催化酶作用下可以高效合成甲醇 。
。①写出甲醇燃烧的化学方程式:
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是
③将上图中的
 改为甲醇就构成了碱性甲醇燃料电池,其中发生还原反应的电极是
改为甲醇就构成了碱性甲醇燃料电池,其中发生还原反应的电极是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】一种湿法回收 技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂(
技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂( )。
)。
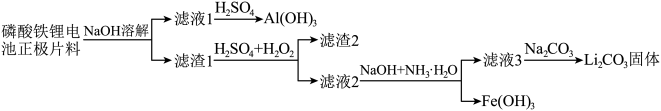
(1)①磷酸铁锂电池的内部结构如图a所示,充电时总反应是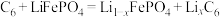 放电时,电池的正极反应为
放电时,电池的正极反应为______ 。
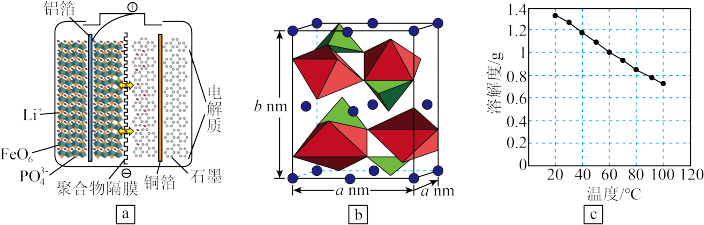
②下列分析合理的是______ (填序号)。
A.拆分前对废旧电池进行预放电,有利于释放残余能量,消除安全隐患
B.预放电时电池中的锂离子移向负极,有利于提高正极片中锂元素的回收率
C.对废旧锂离子电池进行热处理可以除去其中的难溶有机物、碳粉等
D.锂离子电池不含汞、镉、铅等有毒重金属,可直接深埋处理
③磷酸铁锂( )的晶胞结构如图b所示,其中“○”代表
)的晶胞结构如图b所示,其中“○”代表 。则磷酸铁锂晶体的摩尔体积
。则磷酸铁锂晶体的摩尔体积
______  (已知阿伏加德罗常数为
(已知阿伏加德罗常数为 )。
)。
(2)正极材料经过一系列预处理后粉碎,然后使用氢氧化钠溶液浸泡,请写出该过程发生的主要离子方程式:______ 。
(3)已知磷酸铁易溶于硫酸,请写出用硫酸和 ,与滤渣1作用的离子反应方程式:
,与滤渣1作用的离子反应方程式:______ 。
(4)碳酸锂的溶解度随温度变化如图c所示。向滤液3中加入 溶液,将温度升至90℃的目的是
溶液,将温度升至90℃的目的是______ ;得到碳酸锂沉淀的最佳操作为______ (填序号)。
a.静置,过滤 b.加热,趁热过滤 c.蒸发浓缩、冷却结晶 d.蒸发结晶
(5)取100mL滤液3,其中 ,为使锂元素的回收率不低于80%,则至少应加入
,为使锂元素的回收率不低于80%,则至少应加入 固体的物质的量为
固体的物质的量为______ mol。[已知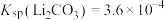 ]。
]。
 技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂(
技术如下图所示,已知正极废料中主要含有铝箔,碳黑,磷酸铁锂( )。
)。
(1)①磷酸铁锂电池的内部结构如图a所示,充电时总反应是
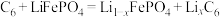 放电时,电池的正极反应为
放电时,电池的正极反应为
②下列分析合理的是
A.拆分前对废旧电池进行预放电,有利于释放残余能量,消除安全隐患
B.预放电时电池中的锂离子移向负极,有利于提高正极片中锂元素的回收率
C.对废旧锂离子电池进行热处理可以除去其中的难溶有机物、碳粉等
D.锂离子电池不含汞、镉、铅等有毒重金属,可直接深埋处理
③磷酸铁锂(
 )的晶胞结构如图b所示,其中“○”代表
)的晶胞结构如图b所示,其中“○”代表 。则磷酸铁锂晶体的摩尔体积
。则磷酸铁锂晶体的摩尔体积
 (已知阿伏加德罗常数为
(已知阿伏加德罗常数为 )。
)。(2)正极材料经过一系列预处理后粉碎,然后使用氢氧化钠溶液浸泡,请写出该过程发生的主要离子方程式:
(3)已知磷酸铁易溶于硫酸,请写出用硫酸和
 ,与滤渣1作用的离子反应方程式:
,与滤渣1作用的离子反应方程式:(4)碳酸锂的溶解度随温度变化如图c所示。向滤液3中加入
 溶液,将温度升至90℃的目的是
溶液,将温度升至90℃的目的是a.静置,过滤 b.加热,趁热过滤 c.蒸发浓缩、冷却结晶 d.蒸发结晶
(5)取100mL滤液3,其中
 ,为使锂元素的回收率不低于80%,则至少应加入
,为使锂元素的回收率不低于80%,则至少应加入 固体的物质的量为
固体的物质的量为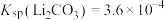 ]。
]。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】研究化学反应中的能量变化、化学反应的速率有重要意义。回答下列问题:
(1) ,
, 下列物质气态时的相对能量如下表:
下列物质气态时的相对能量如下表:
① 与足量
与足量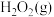 反应生成
反应生成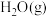
___________ (填吸收或释放)的能量为___________ kJ。
②可根据 计算出
计算出 中氢氢键断裂吸收的能量为
中氢氢键断裂吸收的能量为 ,
,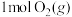 中氧氧键断裂所需能量
中氧氧键断裂所需能量___________ (填“ ”“
”“ ”或“
”或“ ”)
”)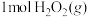 中氧氧键断裂所需能量。
中氧氧键断裂所需能量。
(2) 燃料电池的工作原理如图所示:
燃料电池的工作原理如图所示:
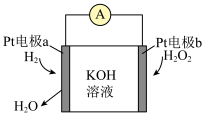
①写出Pt电极b上的电极反应式:___________ 。
②电池工作时,下列说法正确的是___________ (填标号)。
A.化学能全部转化为电能
B.Pt电极a的电势低于Pt电极b
C.离子导体中, 向Pt电极b移动
向Pt电极b移动
D.负极的电极反应为
(3)某实验小组利用数据采集系统探究 溶液对双氧水分解速率的影响。实验装置和所完成实验如下:
溶液对双氧水分解速率的影响。实验装置和所完成实验如下:
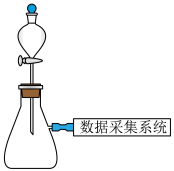
①表中a=___________ 。
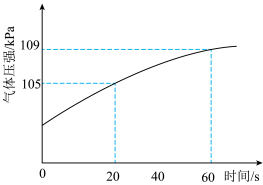
②实验2测定数据如图所示,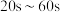 内用氧气压强变化表示的平均反应速率为
内用氧气压强变化表示的平均反应速率为___________  。
。
(1)
 ,
, 下列物质气态时的相对能量如下表:
下列物质气态时的相对能量如下表:| 物质 |  |  |  |  | O | H | HO |
相对能量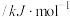 | 0 | 0 | 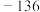 |  | 249 | 218 | 39 |
 与足量
与足量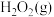 反应生成
反应生成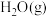
②可根据
 计算出
计算出 中氢氢键断裂吸收的能量为
中氢氢键断裂吸收的能量为 ,
,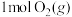 中氧氧键断裂所需能量
中氧氧键断裂所需能量 ”“
”“ ”或“
”或“ ”)
”)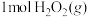 中氧氧键断裂所需能量。
中氧氧键断裂所需能量。(2)
 燃料电池的工作原理如图所示:
燃料电池的工作原理如图所示:
①写出Pt电极b上的电极反应式:
②电池工作时,下列说法正确的是
A.化学能全部转化为电能
B.Pt电极a的电势低于Pt电极b
C.离子导体中,
 向Pt电极b移动
向Pt电极b移动D.负极的电极反应为

(3)某实验小组利用数据采集系统探究
 溶液对双氧水分解速率的影响。实验装置和所完成实验如下:
溶液对双氧水分解速率的影响。实验装置和所完成实验如下:
| 编号 | 温度/℃ |  溶液的体积 溶液的体积 |  溶液的体积 溶液的体积 | 蒸馏水的体积 |
| 1 | 25 | 4 | 0 | a |
| 2 | 25 | 4 | 2 | 0 |
②实验2测定数据如图所示,
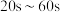 内用氧气压强变化表示的平均反应速率为
内用氧气压强变化表示的平均反应速率为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】化学电池的发明,是贮能和供能技术的巨大进步。

(1)如图所示装置中,Cu片是_______ (填“正极”或“负极”)。
(2)如图所示装置,能证明产生电能的实验现象是_______ 、_______ 。
(3)写出锌电极上的电极反应_______ 。
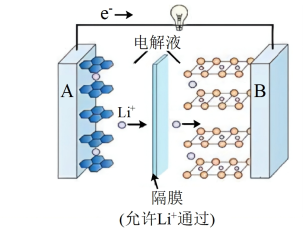
(4)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
下列说法正确的是_______ (填序号)。
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动

(1)如图所示装置中,Cu片是
(2)如图所示装置,能证明产生电能的实验现象是
(3)写出锌电极上的电极反应
(4)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。

下列说法正确的是
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次