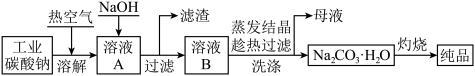
工业碳酸钠(纯度约为98%)中含有Mg2+、Fe2+、Cl-和 等杂质,提纯工艺流程如下:
等杂质,提纯工艺流程如下:
下列说法不正确的是
 等杂质,提纯工艺流程如下:
等杂质,提纯工艺流程如下:
下列说法不正确的是
A.通入热空气可加快溶解速率并氧化 |
B.产生滤渣的离子反应为: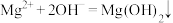 , ,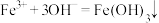 |
C.为检验母液中是否含有 ,加入的试剂为少量的 ,加入的试剂为少量的 溶液 溶液 |
| D.灼烧时用到的主要仪器有铁坩埚、泥三角、三脚架、酒精灯 |
更新时间:2024-01-18 21:44:21
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】某无色透明的强酸性溶液中,能大量共存的离子组是
A.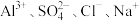 | B.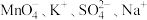 |
C.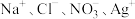 | D.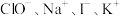 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法不正确 的是
A.取一支试管,向其中加入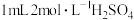 溶液,再滴加 溶液,再滴加 滴 滴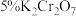 溶液,然后滴入乙醇,振荡,观察到溶液由橙红色变为浅绿色 溶液,然后滴入乙醇,振荡,观察到溶液由橙红色变为浅绿色 |
| B.检验牙膏中是否含有甘油,可选用新制的氢氧化铜悬浊液,观察是否产生绛蓝色沉淀 |
C.可用 和稀硝酸鉴别 和稀硝酸鉴别 和 和 液,最终有白色沉淀的是 液,最终有白色沉淀的是 溶液 溶液 |
| D.二氯化钴的结晶水合物在加热时逐步失水,会呈现粉红色→紫色→蓝紫色→蓝色的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某澄清透明的溶液中可能含有:Na+、Mg2+、Fe2+、Cu2+、I-、 、
、 、Cl-中的几种,各离子浓度均为0.1mol/L,现进行如图实验(所加试剂均过量):
、Cl-中的几种,各离子浓度均为0.1mol/L,现进行如图实验(所加试剂均过量):

下列说法正确的是( )
 、
、 、Cl-中的几种,各离子浓度均为0.1mol/L,现进行如图实验(所加试剂均过量):
、Cl-中的几种,各离子浓度均为0.1mol/L,现进行如图实验(所加试剂均过量):
下列说法正确的是( )
A.样品溶液中肯定存在Na+、Fe2+、 |
| B.沉淀B中肯定有氢氧化铁,可能含有氢氧化镁 |
| C.取1L黄色溶液D,能恰好溶解铁1.4g |
| D.该样品溶液中是否存在Cl-可取滤液C,滴加硝酸银和稀硝酸进行确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关物质的转化或应用说法不正确的是


| A.若X、Y、Z分别为Si、SiO2、H2SiO3,则可通过一步反应实现如图所示的转化关系 |
| B.若X、Y、Z分别为C、CO、CO2,则可通过一步反应实现如图所示的转化关系 |
| C.若X、Y、Z分别为Fe、FeCl2、FeCl3,则可通过一步反应实现如图所示的转化关系 |
| D.若X、Y、Z分别为AlCl3、Al(OH)3、NaAlO2,则可通过一步反应实现如图所示的转化关系 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关硅及其化合物的说法中不正确的是
A.在粗硅的提取中发生反应:2C+SiO2 2CO↑+Si,硅元素被还原 2CO↑+Si,硅元素被还原 |
| B.Si和SiO2均能与NaOH溶液反应生成硅酸钠 |
| C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 |
D.由Na2CO3+SiO2 CO2↑+Na2SiO3可知硅酸的酸性强于碳酸 CO2↑+Na2SiO3可知硅酸的酸性强于碳酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列分离、提纯的方法不能达到实验目的的是
| 选项 | 实验目的 | 分离、提纯的方法 |
| A | 海水淡化 | 蒸馏 |
| B | 分离固体碘和沙子 | 升华 |
| C | 除去铜粉中的铁粉 | 加入适量稀硫酸,过滤、洗涤、干燥 |
| D | 除去O2中的HCl气体 | 用饱和NaHCO3溶液洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.粗盐的提纯时,加入沉淀剂过滤的滤液在坩埚中蒸发结晶、出现晶膜停止加热 |
| B.用碱式滴定管可以准确量取20.00 mLKMnO4溶液 |
| C.在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42- |
| D.配制一定物质的量浓度的溶液时,容量瓶洗涤后未干燥,不影响所配溶液浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室通过对市售85%磷酸溶液进行减压蒸馏除水、结晶除杂得到纯磷酸晶体,实验装置如图。

已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成 (熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。
(熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。
下列实验装置和操作不能 达到实验目的的是

已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成
 (熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。
(熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。下列实验装置和操作
A.图甲中使用的 、浓硫酸、 、浓硫酸、 的目的均为干燥气体 的目的均为干燥气体 |
| B.向图乙得到的过饱和磷酸溶液中加入磷酸晶体,可以促进其结晶 |
| C.图丙中冷凝管的进水口是b,具支烧瓶中得到磷酸溶液 |
| D.磷酸中少量的水极难除去的原因是磷酸可与水分子间形成氢键 |
您最近一年使用:0次
【推荐1】某小组用硫铜矿煅烧废渣(主要含Fe2O3、CuO、FeO)为原料制取Cu2O,流程如图:
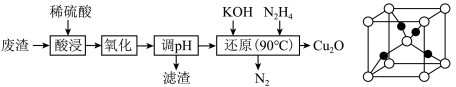
下列说法错误的是

下列说法错误的是
| A.“调节pH”时可以选择CuO或Cu(OH)2 |
| B.“还原”过程中消耗的CuSO4、N2H4的物质的量之比为4:1 |
| C.用N2H4还原制取Cu2O的优点是产生N2氛围,可防止产品被氧化 |
| D.Cu2O的晶胞结构如上图所示,1个Cu2O晶胞中含1个氧原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以含镍废料(主要成分为NiO,含少量FeO、Fe2O3、CoO、BaO和SiO2)为原料制备碳酸钴(CoCO3)和NixOy的工艺流程如图。下列说法正确的是


| A.“滤渣I”成分是SiO2 |
| B.“氧化”时为证明添加NaClO3已足量,可用KSCN溶液进行检验 |
C.“沉钴”反应的离子方程式为2 +Co2+=CoCO3↓+CO2↑+H2O +Co2+=CoCO3↓+CO2↑+H2O |
| D.NiSO4溶液通过蒸发结晶获得NiSO4·6H2O晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一种从含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如图:
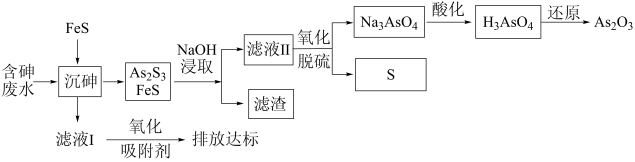
已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq) 2AsS
2AsS (aq)
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是

已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq)
(aq)III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是
| A.As2S3中砷元素的化合价为+3价 |
| B.“沉砷”过程中FeS可以用过量的Na2S代替 |
C.用氧气进行“氧化脱硫”涉及离子方程式AsS +2O2=AsO +2O2=AsO +3S↓ +3S↓ |
| D.能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸 |
您最近一年使用:0次



