全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称。空气吹出法工艺是目前“海水提溴”的最主要方法之一,其工艺流程如图:

(1)步骤①中获得 的离子方程式为
的离子方程式为_______ 。
(2)根据上述反应可判断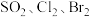 氧化性由强到弱的顺序
氧化性由强到弱的顺序_______ 。
(3)步骤③中完全吸收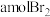 共有
共有_______ 个电子转移(用a和 的代数式表示)。
的代数式表示)。

(1)步骤①中获得
 的离子方程式为
的离子方程式为(2)根据上述反应可判断
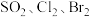 氧化性由强到弱的顺序
氧化性由强到弱的顺序(3)步骤③中完全吸收
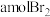 共有
共有 的代数式表示)。
的代数式表示)。
更新时间:2024-01-18 22:46:32
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某工厂酸性废水中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,研究学习小组取该工厂一定量的废水,浓缩后将所得澄清试液分成3份,进行如下实验:
中的几种,研究学习小组取该工厂一定量的废水,浓缩后将所得澄清试液分成3份,进行如下实验:
回答下列问题:
(1)根据实验结果判断该废水中一定存在的离子是_______ ,一定不存在的离子是_______ ,可能存在的离子是_______ 。
(2)写出第一份试液中发生反应的离子方程式_______ 。
(3)写出b〜c段有气体生成的离子反应方程式_______ 。
(4)设计实验方案检验该溶液中可能存在的阴离子是否存在_______ 。(写出实验操作、现象及结论)。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,研究学习小组取该工厂一定量的废水,浓缩后将所得澄清试液分成3份,进行如下实验:
中的几种,研究学习小组取该工厂一定量的废水,浓缩后将所得澄清试液分成3份,进行如下实验:| 试样 | 所加试剂 | 实验现象 |
| 第一份试液 | 加入少量Cu片 | Cu片逐渐溶解,溶液变为蓝色,有气泡冒出,试管内无色气体在试管口变为红棕色 |
| 第二份试液 | 滴加用盐酸酸化的 溶液 溶液 | 有白色沉淀产生 |
| 第三份试液 | 逐滴滴加NaOH溶液,加热,加入NaOH溶液的体积(V)与生成的沉淀、产生的气体 |  |
(1)根据实验结果判断该废水中一定存在的离子是
(2)写出第一份试液中发生反应的离子方程式
(3)写出b〜c段有气体生成的离子反应方程式
(4)设计实验方案检验该溶液中可能存在的阴离子是否存在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
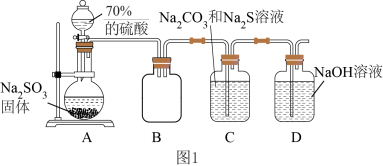
【推荐2】硫代硫酸钠( ),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少
),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少 。
。
已知: 在酸性溶液中发生反应:
在酸性溶液中发生反应: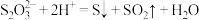
(1)实验室制备 气体也可以用浓硫酸与Cu反应,该反应的化学方程式是
气体也可以用浓硫酸与Cu反应,该反应的化学方程式是_______ 。图1装置B的作用是________ 。
(2)图1装置C中发生反应生成 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是_____ 。
(3)某同学用图2中装置验证装置C中生成了 。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是_______ 。
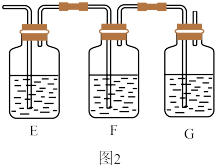
A.品红、 溶液、澄清石灰水
溶液、澄清石灰水
B.酸性 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水
C. 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水
(4)从装置C中所得溶液经过结晶等操作获得的 晶体中含有少量的
晶体中含有少量的 ,试检验其中含有
,试检验其中含有 的方法是:取少量固体,
的方法是:取少量固体,________ ,离心沉降,过滤,_______ ,若有白色沉淀生成,则原晶体中含有 。(实验中可选用的试剂:稀盐酸、稀硫酸、
。(实验中可选用的试剂:稀盐酸、稀硫酸、 溶液)
溶液)
 ),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少
),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少 。
。
已知:
 在酸性溶液中发生反应:
在酸性溶液中发生反应: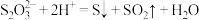
(1)实验室制备
 气体也可以用浓硫酸与Cu反应,该反应的化学方程式是
气体也可以用浓硫酸与Cu反应,该反应的化学方程式是(2)图1装置C中发生反应生成
 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是(3)某同学用图2中装置验证装置C中生成了
 。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
A.品红、
 溶液、澄清石灰水
溶液、澄清石灰水 B.酸性
 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水C.
 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水(4)从装置C中所得溶液经过结晶等操作获得的
 晶体中含有少量的
晶体中含有少量的 ,试检验其中含有
,试检验其中含有 的方法是:取少量固体,
的方法是:取少量固体, 。(实验中可选用的试剂:稀盐酸、稀硫酸、
。(实验中可选用的试剂:稀盐酸、稀硫酸、 溶液)
溶液)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在高温条件下用普通铁粉和水蒸气反应,可以得到粉末状的四氧化三铁,四氧化三铁又可以经过此反应的逆反应,在高温条件下生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”,可用于焊接铁轨。下面是某兴趣小组在实验室制备“引火铁”的过程。回答下列问题:
I.利用图1所示装置(加热装置省略)制取铁的氧化物。
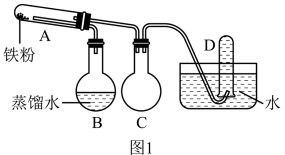
(1)试管A中发生反应的化学方程式是_______ ,若在D中收集到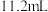 气体(已折算为标准状态下),则转移的电子数目为
气体(已折算为标准状态下),则转移的电子数目为_______ 。
(2)装置B的作用是_______ 。
(3)为检验产物中是否有四氧化三铁生成,甲同学进行了如下实验
①写出稀盐酸与四氧化三铁反应的离子反应方程式_______ 。
②甲同学根据上述现象,认为没有四氧化三铁生成;乙同学认为可能有四氧化三铁,原因是_______ (用离子反应方程式表示)。
Ⅱ.利用图2所示装置制取“引火铁”。

(4)仪器a的名称是_______ ,装置C的作用是_______ 。
(5)为了安全,装置D加热前,应该进行的操作是_______ 。
I.利用图1所示装置(加热装置省略)制取铁的氧化物。

(1)试管A中发生反应的化学方程式是
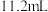 气体(已折算为标准状态下),则转移的电子数目为
气体(已折算为标准状态下),则转移的电子数目为(2)装置B的作用是
(3)为检验产物中是否有四氧化三铁生成,甲同学进行了如下实验
| 步骤 | 现象 |
| 取少量产品于试管中,加入稀盐酸 | 产品溶解,有气泡产生 |
在上述溶液中滴加 溶液 溶液 | 溶液未变红 |
②甲同学根据上述现象,认为没有四氧化三铁生成;乙同学认为可能有四氧化三铁,原因是
Ⅱ.利用图2所示装置制取“引火铁”。

(4)仪器a的名称是
(5)为了安全,装置D加热前,应该进行的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】一氯化碘(ICl)是一种卤素互化物。卤素互化物具有强氧化性稀溶液,可与金属直接反应,也可用作有机合成中的碘化剂,一般可由卤素单质直接化合制得。有关一氯化碘制备及性质验证,请回答下列问题:
Ⅰ.海藻提碘可得到 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:

(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和_______ 。
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______ 。

Ⅱ.某学习小组在实验室中拟用下图装置制取纯净、干燥的氯气,并利用氯气与碘反应制备一氯化碘。

查阅资料了解到以下内容:
①碘与氯气的反应为放热反应
②ICl是一种红棕色液体,沸点97.4℃,不溶于水
③ICl能与KI反应生成
请回答下列问题:
(3)各装置连接顺序为A→_______ ;
(4)B装置烧瓶需放在冷水中,其目的是:_______ ,B装置得到的液态产物进一步提纯可得到较纯净的ICl,采取的方法是_______ 。
(5)ICl与稀NaOH溶液可发生非氧化还原反应,请写出该反应的离子方程式_______ 。
(6)请设计简单的实验证明ICl的氧化性比 强:
强:_______ 。
Ⅰ.海藻提碘可得到
 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

Ⅱ.某学习小组在实验室中拟用下图装置制取纯净、干燥的氯气,并利用氯气与碘反应制备一氯化碘。

查阅资料了解到以下内容:
①碘与氯气的反应为放热反应
②ICl是一种红棕色液体,沸点97.4℃,不溶于水
③ICl能与KI反应生成

请回答下列问题:
(3)各装置连接顺序为A→
(4)B装置烧瓶需放在冷水中,其目的是:
(5)ICl与稀NaOH溶液可发生非氧化还原反应,请写出该反应的离子方程式
(6)请设计简单的实验证明ICl的氧化性比
 强:
强:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组想探究实验室用MnO2与盐酸反应制取氯气的反应条件,实验装置及药品如下。
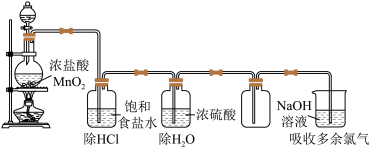
(1)写出实验室制氯气的离子方程式_______ 。
(2)结合平衡移动原理,解释饱和食盐水的作用是_______ 。
(3)已知:不同温度下MnO2与盐酸反应的平衡常数
MnO2与盐酸的反应是_______ 反应(填“放热”或“吸热”)。
(4)为探究条件对该反应的影响,小组同学设计并完成以下实验:
①根据上述实验可知MnO2与盐酸产生氯气的反应条件为_______ 。
②针对实验1和实验3的现象,小组同学从电极反应角度分析物质氧化性和还原性的变化规律。
写出实验中制氯气反应的电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:_______ 。
提出假设:
ⅰ.增大c(H+),可以_______ 。
ⅱ.增大c(Cl-),可以增大Cl-的还原性。
③补充实验,实验II、III分别证实了②中的分析。
(固液混合物A为一定浓度的盐酸和MnO2混合物;加热装置已略去)
较浓a溶液是_______ ,固体b是_______ 。

(1)写出实验室制氯气的离子方程式
(2)结合平衡移动原理,解释饱和食盐水的作用是
(3)已知:不同温度下MnO2与盐酸反应的平衡常数
| 温度t/℃ | 50 | 80 | 110 |
| 平衡常数K | 3.104×10-4 | 2.347×10-3 | 1.293×10-2 |
(4)为探究条件对该反应的影响,小组同学设计并完成以下实验:
| 序号 | 试剂 | 实验操作 | 现象 |
| 实验1 | 4 mol/L盐酸、MnO2 | 加热 | 无明显现象 |
| 实验2 | 7 mol/L浓盐酸、MnO2 | 不加热 | 无明显现象 |
| 实验3 | 7 mol/L浓盐酸、MnO2 | 加热 | 产生黄绿色气体 |
②针对实验1和实验3的现象,小组同学从电极反应角度分析物质氧化性和还原性的变化规律。
写出实验中制氯气反应的电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:
提出假设:
ⅰ.增大c(H+),可以
ⅱ.增大c(Cl-),可以增大Cl-的还原性。
③补充实验,实验II、III分别证实了②中的分析。
| 实验序号 | 实验操作 | 试剂 | 产物 |
| I |  | 没有添加新的试剂 | 无氯气生成 |
| II | 较浓a溶液 | 有氯气生成 | |
| III | 固体b | 有氯气生成 |
较浓a溶液是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题
(1)按如图所示操作,充分反应后:

①Ⅰ中铁丝上观察到的现象是_______ ;
②Ⅱ中发生反应的离子方程式为_______ ;
③结合Ⅰ、Ⅱ的实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_______ 。
(2)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为: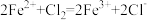 ,将足量Cl2通入FeBr2溶液中,反应的离子方程式为
,将足量Cl2通入FeBr2溶液中,反应的离子方程式为 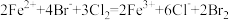 ;这个事实说明Cl-、Fe2+、Br-的还原性强弱顺序为
;这个事实说明Cl-、Fe2+、Br-的还原性强弱顺序为 _______ 。
(1)按如图所示操作,充分反应后:

①Ⅰ中铁丝上观察到的现象是
②Ⅱ中发生反应的离子方程式为
③结合Ⅰ、Ⅱ的实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(2)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为:
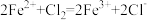 ,将足量Cl2通入FeBr2溶液中,反应的离子方程式为
,将足量Cl2通入FeBr2溶液中,反应的离子方程式为 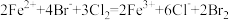 ;这个事实说明Cl-、Fe2+、Br-的还原性强弱顺序为
;这个事实说明Cl-、Fe2+、Br-的还原性强弱顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
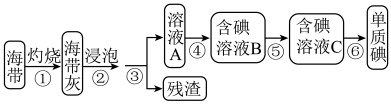
Ⅰ.从海带中提取碘单质,实验流程图如下:
回答下列问题:
(1)在进行步骤①之前,称取mg干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入_____ (填仪器名称)中灼烧至海带完全成灰烬。
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入氯水后颜色变蓝,此反应的离子方程式是_____ ;乙同学认为使用酸化的H2O2溶液能更有利于提取碘,写出离子方程式_____ 。
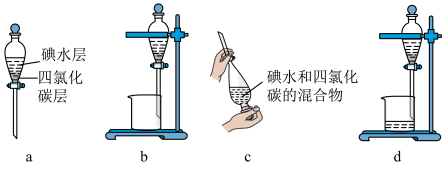
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是_____ (填字母)。_____ 。
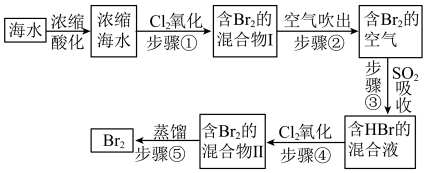
Ⅱ.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
(5)将海水浓缩的方法是_____ 。
(6)步骤②通入热空气吹出Br2,利用了Br2的_____ 性质。
(7)步骤③反应的离子方程式是_____ ,从理论上分析,下列能代替SO2吸收溴的是_____ (填字母)。
A.NaOH B.Na2SO3 C.H2O D.FeCl2
Ⅰ.从海带中提取碘单质,实验流程图如下:
回答下列问题:
(1)在进行步骤①之前,称取mg干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入氯水后颜色变蓝,此反应的离子方程式是
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是
Ⅱ.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
(5)将海水浓缩的方法是
(6)步骤②通入热空气吹出Br2,利用了Br2的
(7)步骤③反应的离子方程式是
A.NaOH B.Na2SO3 C.H2O D.FeCl2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如下:
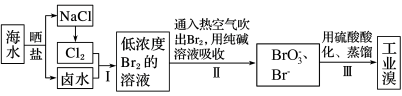
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是_______ 。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的__________ 。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面横线上填入适当的化学计量数:_____ Br2+_____ CO32-=_____ BrO3-+_____ Br-+_____ CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________ 。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是__________ 。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面横线上填入适当的化学计量数:
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】溴及其衍生物是制药业和制取阻燃剂、钻井液等的重要原料,需求量很大。工业上以提取镁后的浓缩海水为原料提取溴的部分流程图如下:
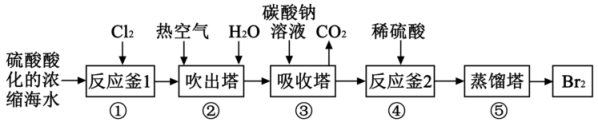
回答下列问题:
(1)海水需要浓缩的原因是_______ ;热空气和水(蒸气)的作用是_______ 。
(2)反应釜1中生成的溴位于混合体系的_______ 层;溴层中混有的杂质(单质)主要是_______ 。
(3)该流程操作应在_______ (选填“干燥”或“通风”或“无氧”)环境下进行,其原因是_______ 。
(4)已知在酸性条件下,氧化性: 。若步骤④中的稀硫酸用盐酸代替会导致生成的溴中混有少量氯气,发生反应的离子方程式是
。若步骤④中的稀硫酸用盐酸代替会导致生成的溴中混有少量氯气,发生反应的离子方程式是_______ 。

回答下列问题:
(1)海水需要浓缩的原因是
(2)反应釜1中生成的溴位于混合体系的
(3)该流程操作应在
(4)已知在酸性条件下,氧化性:
 。若步骤④中的稀硫酸用盐酸代替会导致生成的溴中混有少量氯气,发生反应的离子方程式是
。若步骤④中的稀硫酸用盐酸代替会导致生成的溴中混有少量氯气,发生反应的离子方程式是
您最近一年使用:0次



