按要求填写下列空格。
(1)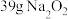 中阴离子的数目为
中阴离子的数目为________
(2) 个水分子的质量为
个水分子的质量为________
(3)现有标准状况下 和
和 混合气体6.72L,其质量为10g,则此混合气体中,
混合气体6.72L,其质量为10g,则此混合气体中, 和
和 的物质的量之比是
的物质的量之比是________
(4)9.2g氮的氧化物 中N原子的物质的量为
中N原子的物质的量为 ,则x的数值为
,则x的数值为________ 。
(5)某盐混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则 =
=________
(6)取 钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是
钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是________
(7)使用胆矾配制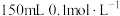 的
的 溶液,需要用托盘天平称取胆矾的质量为
溶液,需要用托盘天平称取胆矾的质量为________
(1)
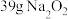 中阴离子的数目为
中阴离子的数目为(2)
 个水分子的质量为
个水分子的质量为(3)现有标准状况下
 和
和 混合气体6.72L,其质量为10g,则此混合气体中,
混合气体6.72L,其质量为10g,则此混合气体中, 和
和 的物质的量之比是
的物质的量之比是(4)9.2g氮的氧化物
 中N原子的物质的量为
中N原子的物质的量为 ,则x的数值为
,则x的数值为(5)某盐混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则 =
=(6)取
 钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是
钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是(7)使用胆矾配制
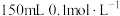 的
的 溶液,需要用托盘天平称取胆矾的质量为
溶液,需要用托盘天平称取胆矾的质量为
更新时间:2024-01-24 00:48:37
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】Ⅰ.氧化还原反应在生产生活中普遍存在。
(1)工业上制取 的原理为:
的原理为: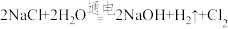 ↑ 。当收集到标准状况下224
↑ 。当收集到标准状况下224
 时,生成的
时,生成的 为
为_______ g。
(2)激光雷达的核心部件需要一种氮化铝( )导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50
)导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50 2.0
2.0 的
的 溶液恰好完全反应,求氮化铝样品中
溶液恰好完全反应,求氮化铝样品中 的质量分数
的质量分数_______ 已知: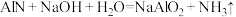 。
。
Ⅱ. 的减排已经引起国际社会的广泛关注,近日我国科学家实现了
的减排已经引起国际社会的广泛关注,近日我国科学家实现了 高选择性、高稳定性加氢合成甲醇(
高选择性、高稳定性加氢合成甲醇( )。回答下列问题:
)。回答下列问题:
(3) 的摩尔质量是
的摩尔质量是______  。
。
(4)2
 中所含原子的物质的量为
中所含原子的物质的量为_______  。
。
(5)_______ g的氢气中所含H原子的数目与1
 相同。
相同。
(6)含0.1 个O的
个O的 中有
中有_______ 个电子,标况下该 的体积为
的体积为_______ L。
(1)工业上制取
 的原理为:
的原理为: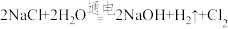 ↑ 。当收集到标准状况下224
↑ 。当收集到标准状况下224
 时,生成的
时,生成的 为
为(2)激光雷达的核心部件需要一种氮化铝(
 )导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50
)导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50 2.0
2.0 的
的 溶液恰好完全反应,求氮化铝样品中
溶液恰好完全反应,求氮化铝样品中 的质量分数
的质量分数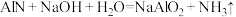 。
。Ⅱ.
 的减排已经引起国际社会的广泛关注,近日我国科学家实现了
的减排已经引起国际社会的广泛关注,近日我国科学家实现了 高选择性、高稳定性加氢合成甲醇(
高选择性、高稳定性加氢合成甲醇( )。回答下列问题:
)。回答下列问题:(3)
 的摩尔质量是
的摩尔质量是 。
。(4)2

 中所含原子的物质的量为
中所含原子的物质的量为 。
。(5)

 相同。
相同。(6)含0.1
 个O的
个O的 中有
中有 的体积为
的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】0.40L某浓度的NaOH溶液恰好与标准状况下5.8 L Cl2完全反应,计算:
(1)生成的NaClO的物质的量;
(2)该溶液中NaOH的物质的量浓度。
(1)生成的NaClO的物质的量;
(2)该溶液中NaOH的物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】在15℃下将氨气通入一盛水的玻璃球内,至氨气不再溶解为止。经称量得知玻璃球内的饱和溶液质量为3.400g,然后将玻璃球浸入体积为50.00mL浓度为0.5000mol/L的硫酸溶液中,将球击破。充分反应后溶液中剩余的酸还能与10.00mL 1.000mol/L的NaOH溶液恰好完全反应生成正盐。该氨水中的溶质全部以NH3计,则:
(1)饱和溶液中NH3的物质的量为____________________ 。
(2)饱和溶液中NH3的质量分数为__________ 。
(3)测得所得饱和氨水的密度为0.918g/cm3,则饱和溶液中NH3的物质的量浓度为__________ 。
(1)饱和溶液中NH3的物质的量为
(2)饱和溶液中NH3的质量分数为
(3)测得所得饱和氨水的密度为0.918g/cm3,则饱和溶液中NH3的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】硫酸和盐酸组成的混合液100.0 mL,向其中加入氢氧化钡粉末4.275g,充分反应后,经过滤、洗涤、干燥,得到沉淀2.330g,同时测得滤液中的OH-离子浓度为0.100 mol·L-1 。(设溶液总体积始终不变)请列式计算
(1)原溶液中硫酸的物质的量为___________ 。
(2)原混合液中盐酸的物质的量浓度___________ 。
(3)若将原硫酸和盐酸混合溶液100ml与足量金属锌反应,则在标况下产生的气体体积为___________ 。
(1)原溶液中硫酸的物质的量为
(2)原混合液中盐酸的物质的量浓度
(3)若将原硫酸和盐酸混合溶液100ml与足量金属锌反应,则在标况下产生的气体体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将32g铜与100mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L。
请回答:
(1)NO气体与NO2气体体积比为___ 。
(2)将产生的气体全部逸出后向溶液中加入VmLamol/LNaOH溶液,恰好使溶液中的铜离子全部转化为沉淀,则原硝酸溶液的浓度为__ mol/L(用V和a表示)。
请回答:
(1)NO气体与NO2气体体积比为
(2)将产生的气体全部逸出后向溶液中加入VmLamol/LNaOH溶液,恰好使溶液中的铜离子全部转化为沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】现有碳酸钠和氯化钠的混合物15g,将其放入烧杯中加入100g水,使其完全溶解。向所得溶液中加入溶质质量分数为9.8%的稀硫酸,烧杯中溶液的质量与加入稀硫酸的质量关系如图所示,请回答下列问题。

(1)B点时烧杯中溶液含有的阳离子是_______ (填离子符号)。
(2)恰好完全反应时加入稀硫酸的质量为_______ g。
(3)混合物中氯化钠的质量是_______ 克(写出具体计算过程)?

(1)B点时烧杯中溶液含有的阳离子是
(2)恰好完全反应时加入稀硫酸的质量为
(3)混合物中氯化钠的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】利用相关知识填空:
(1)等质量的SO2和SO3所含的氧原子个数之比是__________ 。
(2)4.8 g CH4中所含氢原子个数与______ g水所含氢原子数相等。
(3)标准状况下,测得1.32 g某气体的体积为0.672 L,则此气体的摩尔质量为___________ 。
(4)将4 g NaOH溶于水配成250 mL溶液,溶液中NaOH的物质的量浓度为_____________ 。
(5)100 mL 0.3 mol/L Na2SO4溶液和50 mL 0.2 mol/L Al2(SO4)3溶液混合后,溶液中 的物质的量浓度为
的物质的量浓度为___ 。
(1)等质量的SO2和SO3所含的氧原子个数之比是
(2)4.8 g CH4中所含氢原子个数与
(3)标准状况下,测得1.32 g某气体的体积为0.672 L,则此气体的摩尔质量为
(4)将4 g NaOH溶于水配成250 mL溶液,溶液中NaOH的物质的量浓度为
(5)100 mL 0.3 mol/L Na2SO4溶液和50 mL 0.2 mol/L Al2(SO4)3溶液混合后,溶液中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)12.4 gNa2R含Na+ 0.4mol,则R的摩尔质量为_____ 。
(2)在硫酸钠和硫酸铝的混合溶液中,Al3+的物质的量浓度为0.2mol/L, 为0.4mol/L,则Na+的物质的量浓度为
为0.4mol/L,则Na+的物质的量浓度为_____ 。
(3)在一定温度下体积为2L的密闭容器中4molSO2和3mol氧气反应,反应一段时间后,压强减小了20%,此时生成SO3的物质的量为_____ 。
(4)实验室里需用480mL 0.2mol·L-1的硫酸铜溶液,现使用容量瓶进行配制,托盘天平需称取胆矾的质量为____ 。
(2)在硫酸钠和硫酸铝的混合溶液中,Al3+的物质的量浓度为0.2mol/L,
 为0.4mol/L,则Na+的物质的量浓度为
为0.4mol/L,则Na+的物质的量浓度为(3)在一定温度下体积为2L的密闭容器中4molSO2和3mol氧气反应,反应一段时间后,压强减小了20%,此时生成SO3的物质的量为
(4)实验室里需用480mL 0.2mol·L-1的硫酸铜溶液,现使用容量瓶进行配制,托盘天平需称取胆矾的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某同学欲配制40%的NaOH溶液100克,实验室中现有10%的NaOH溶液和NaOH固体,问此同学应各取上述物质多少克?
您最近一年使用:0次



