将铜片放入 115mL 某浓度的浓硫酸中,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500mL,再加入足量锌粉,使之充分反应,收集到 2.24L(标准状况下)氢气。过滤残留固体,干燥后称量,质量减轻了 7.5g。求原硫酸的物质的量浓度________________ 。
更新时间:2020-06-02 09:13:48
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】按要求填写下列空格。
(1)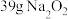 中阴离子的数目为
中阴离子的数目为________
(2) 个水分子的质量为
个水分子的质量为________
(3)现有标准状况下 和
和 混合气体6.72L,其质量为10g,则此混合气体中,
混合气体6.72L,其质量为10g,则此混合气体中, 和
和 的物质的量之比是
的物质的量之比是________
(4)9.2g氮的氧化物 中N原子的物质的量为
中N原子的物质的量为 ,则x的数值为
,则x的数值为________ 。
(5)某盐混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则 =
=________
(6)取 钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是
钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是________
(7)使用胆矾配制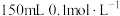 的
的 溶液,需要用托盘天平称取胆矾的质量为
溶液,需要用托盘天平称取胆矾的质量为________
(1)
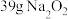 中阴离子的数目为
中阴离子的数目为(2)
 个水分子的质量为
个水分子的质量为(3)现有标准状况下
 和
和 混合气体6.72L,其质量为10g,则此混合气体中,
混合气体6.72L,其质量为10g,则此混合气体中, 和
和 的物质的量之比是
的物质的量之比是(4)9.2g氮的氧化物
 中N原子的物质的量为
中N原子的物质的量为 ,则x的数值为
,则x的数值为(5)某盐混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则 =
=(6)取
 钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是
钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是(7)使用胆矾配制
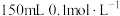 的
的 溶液,需要用托盘天平称取胆矾的质量为
溶液,需要用托盘天平称取胆矾的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】根据物质的量等相关物理量回答下列问题:
(1)_______ mol 所含氢原子数与
所含氢原子数与 所含氢原子数相等。
所含氢原子数相等。
(2)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为_______ 。
(3)20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为_______ 。
(4)NO和 可以发生反应
可以发生反应 ,若反应生成
,若反应生成 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为_______ mol。若有a molNO与b mol 充分反应,则反应后氮原子与氧原子的个数比为
充分反应,则反应后氮原子与氧原子的个数比为_______ (用含a、b的代数式表示)。
(5)36gCO与 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与 的混合气体的总物质的量为
的混合气体的总物质的量为_______ mol,其中的CO在标准状况下的体积为_______ L。
(1)
 所含氢原子数与
所含氢原子数与 所含氢原子数相等。
所含氢原子数相等。(2)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为(3)20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为
(4)NO和
 可以发生反应
可以发生反应 ,若反应生成
,若反应生成 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为 充分反应,则反应后氮原子与氧原子的个数比为
充分反应,则反应后氮原子与氧原子的个数比为(5)36gCO与
 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与 的混合气体的总物质的量为
的混合气体的总物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CO2的摩尔质量是______ g/mol。
(2)在标准状态下,5.6LCO2的物质的量是______ mol,质量是_______ g。
(3)22gCO2的体积是_______ L(标准状况)。
(4)相同质量的CO和CO2所含的氧原子个数比是_______ 。
(5)同温同压下,同体积的CO和CO2的物质的量之比为__________ 。
(1)CO2的摩尔质量是
(2)在标准状态下,5.6LCO2的物质的量是
(3)22gCO2的体积是
(4)相同质量的CO和CO2所含的氧原子个数比是
(5)同温同压下,同体积的CO和CO2的物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】天然碱的组成可以用aNa2CO3·bNaHCO3·cH2O(a、b、c为整数)表示。现有A、B两种不同的天然碱样品,分别进行如下实验以确定其化学式。
将质量为31.0g的天然碱A于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO22.24L(标准状况)和水5.4g。
(1)天然碱A的化学式中:a=___ ,b=___ ,c=___ 。
已知:Na2CO3与稀盐酸的反应分下列两步进行:Na2CO3+HCl NaCl+NaHCO3,NaHCO3+HCl
NaCl+NaHCO3,NaHCO3+HCl NaCl+CO2↑+H2O。
NaCl+CO2↑+H2O。
将质量为12.45g的天然碱B溶于水,逐滴滴加某浓度的稀盐酸,产生气体的体积与加入盐酸的体积(标准状况)的关系如下表所示:
(2)由表中数据可推测加入50mL盐酸时,产生气体的体积为___ mL(标准状况);
(3)盐酸的浓度为___ mol/L;天然碱B的化学式为:___ 。
(4)若取一定质量的天然碱B加入到30mL该浓度的盐酸中,请写出产生气体体积V(mL,标准状况)与天然碱B质量W(g)之间的关系式___ 。
将质量为31.0g的天然碱A于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO22.24L(标准状况)和水5.4g。
(1)天然碱A的化学式中:a=
已知:Na2CO3与稀盐酸的反应分下列两步进行:Na2CO3+HCl
 NaCl+NaHCO3,NaHCO3+HCl
NaCl+NaHCO3,NaHCO3+HCl NaCl+CO2↑+H2O。
NaCl+CO2↑+H2O。将质量为12.45g的天然碱B溶于水,逐滴滴加某浓度的稀盐酸,产生气体的体积与加入盐酸的体积(标准状况)的关系如下表所示:
| 盐酸体积(mL) | 20 | 40 | 60 | 80 |
| 产生气体体积(mL) | 0 | 560 | 1680 | 2520 |
(2)由表中数据可推测加入50mL盐酸时,产生气体的体积为
(3)盐酸的浓度为
(4)若取一定质量的天然碱B加入到30mL该浓度的盐酸中,请写出产生气体体积V(mL,标准状况)与天然碱B质量W(g)之间的关系式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)5.3g Na2CO3的物质的量为____________ ,将其配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为____________ 。取出该溶液10mL,在取出的溶液中通入HCl气体到不再产生气泡为止,共消耗____________ mL HCl气体(标准状况)。
(2)V mL Al2(SO4)3溶液中,含有Al 3+m g,则溶液中SO42-的物质的量浓度为_______ 。(用含有m、V的式子表示)
(2)V mL Al2(SO4)3溶液中,含有Al 3+m g,则溶液中SO42-的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】有下列物质的溶液:①CH3COOH ②HCl ③H2SO4 ④NaHSO4
(1)若四种溶液的物质的量浓度相同,其c(H+)的大小比较为____________ (用序号表示,下同)。
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为___________ ,经测定溶液中c(CH3COO-)为1.4×10-3 mol/L,此温度下醋酸的电离常数Ka=____________ ,温度升高,Ka将_____ (填“变大”“不变”或“变小”,下同),加入少量CH3COONa后c(H+)______ ,Ka______ 。
(1)若四种溶液的物质的量浓度相同,其c(H+)的大小比较为
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在标准状况下,5.6L NH3所含分子数约是__________ ,物质的量是_____________ ,它的质量是___________ ,溶于水配成250ml溶液时其物质的量浓度为___________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】已知锌跟浓硫酸反应生成SO2,跟稀硫酸反应生成H2,32.5克的锌与50 mL 18.4 mol/L浓硫酸充分反应,锌完全溶解,同时收集到标准状况下的气体VL。将反应后的溶液稀释到500mL,测得溶液中氢离子的浓度为0.08 mol/L。
(1)反应过程中消耗的H2SO4的物质的量是________ 。
(2)气体的成分是______ ,V为______ 。
(3)反应过程中转移的电子的物质的量是________ 。
(4)另取相同浓硫酸,向其中改加铁粉,若逐渐加入a克铁粉,同时加热,最终数据均同上,则a=_____ 。
(1)反应过程中消耗的H2SO4的物质的量是
(2)气体的成分是
(3)反应过程中转移的电子的物质的量是
(4)另取相同浓硫酸,向其中改加铁粉,若逐渐加入a克铁粉,同时加热,最终数据均同上,则a=
您最近一年使用:0次
【推荐2】锌与100mL18.5mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1。请计算:
(1)反应中共消耗H2SO4的物质的量为__ 。
(2)反应中共消耗Zn的质量为__ 。
(3)气体的成分及物质的量之比为__ 。
(1)反应中共消耗H2SO4的物质的量为
(2)反应中共消耗Zn的质量为
(3)气体的成分及物质的量之比为
您最近一年使用:0次
【推荐3】0.80g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
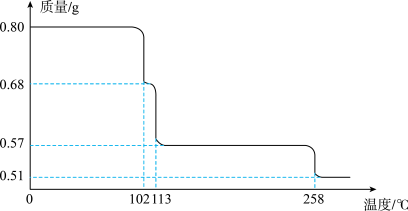
请回答下列问题:
(1)试确定200℃时固体物质的化学式_______ (要求写出推断过程);
(2)取270℃所得样品,于570℃灼烧得到的主要产物是_______ ,把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为_______ ,其存在的最高温度是_______ ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为_______ 。
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=_______ mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1mol·L-1 硫酸铜溶液中通入过量 H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_______ mol·L-1。

请回答下列问题:
(1)试确定200℃时固体物质的化学式
(2)取270℃所得样品,于570℃灼烧得到的主要产物是
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
您最近一年使用:0次



