某小组设计实验探究钠与水的反应,请完善下列实验方案并回答相关问题。
(1)[实验用品] 、水、石蕊试液、玻璃片、小刀、滤纸、
、水、石蕊试液、玻璃片、小刀、滤纸、___________ 、烧杯
(2)[实验设计与实施]
(3)[结论]可由现象___________ (填序号)证实猜想。写出钠与水反应的化学方程式并用双线桥表示电子转移:___________ 。
(1)[实验用品]
 、水、石蕊试液、玻璃片、小刀、滤纸、
、水、石蕊试液、玻璃片、小刀、滤纸、(2)[实验设计与实施]
| 猜想 | 钠可能具有强还原性,依据是 | |
| 实验 | 在烧杯中加入一些水,滴加几滴石蕊试液,取绿豆大小的一块钠,吸千表面煤油,放入水中 | |
| 实验现象 | 分析及结论 | |
| ①钠浮于水面上 | 钠的密度比水小; | |
| ②钠形状的变化: | ||
| ③溶液变为 | 有碱生成 | |
更新时间:2024-01-27 11:26:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为实验室用二氧化锰和浓盐酸为原料制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网。
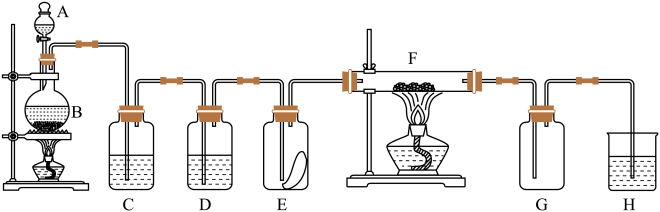
(1)仪器A的名称是___________ 。
(2)写出MnO2与浓盐酸反应的化学方程式___________ 。
(3)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(4)E中的红色布条是否褪色?___________ (填“是”或“否”),写出F中反应的化学方程式:____________________________ 。
(5)H中的试剂为___________ ,其作用是___________ ,写出H中发生反应的离子方程式________________________ 。
(6)氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥标出反应中电子转移的方向和数目:TiO2+2C+2Cl2 TiCl4+2CO
TiCl4+2CO___________ 。

(1)仪器A的名称是
(2)写出MnO2与浓盐酸反应的化学方程式
(3)装置C中盛装的溶液是
(4)E中的红色布条是否褪色?
(5)H中的试剂为
(6)氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥标出反应中电子转移的方向和数目:TiO2+2C+2Cl2
 TiCl4+2CO
TiCl4+2CO
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】下图为实验室抽取纯净而干燥的氯气(Cl2)的实验装置图

(1)“气体发生装置”中的反应原理如下,请用双线桥法表示出电子转移的方向和数目:
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O _______________________
(2)当反应消耗174g MnO2时,生成的Cl2数目为___ 。
(3)浓硫酸的作用是:_______________________ 。
(4)请指出上图中一处非常明显的错误(不考虑“尾气吸收装置”可能发生倒吸,及“尾气吸收装置”中水蒸气进入“气体收集装置”)_______________________ ;
(5)改正错误后,进行实验。请将如下实验步骤按正确操作顺序排序__________________ 。
①打开分液漏斗,向烧瓶中加入一定量的浓盐酸
②检验收集装置内已集满氯气
③连接实验装置
④结束实验
⑤装入药品
⑥点燃酒精灯
⑦检查装置气密性
(6)已知“尾气吸收装置”中反应的氧化产物是NaClO,请写出“尾气吸收装置”中反应的离子方程式:_______________________ 。

(1)“气体发生装置”中的反应原理如下,请用双线桥法表示出电子转移的方向和数目:
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O (2)当反应消耗174g MnO2时,生成的Cl2数目为
(3)浓硫酸的作用是:
(4)请指出上图中一处非常明显的错误(不考虑“尾气吸收装置”可能发生倒吸,及“尾气吸收装置”中水蒸气进入“气体收集装置”)
(5)改正错误后,进行实验。请将如下实验步骤按正确操作顺序排序
①打开分液漏斗,向烧瓶中加入一定量的浓盐酸
②检验收集装置内已集满氯气
③连接实验装置
④结束实验
⑤装入药品
⑥点燃酒精灯
⑦检查装置气密性
(6)已知“尾气吸收装置”中反应的氧化产物是NaClO,请写出“尾气吸收装置”中反应的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)用双线桥法表示出下列反应的电子转移方向和数目。
①3S+6KOH K2SO3+2K2S+3H2O
K2SO3+2K2S+3H2O__________________________
②2FeCl3+Cu=2FeCl2+CuCl2________________________________
(2)现用如图所示的装置制取饱和氯水,请回答有关问题:

①写出装置甲中发生反应的化学方程式:_________________________ 。
②装置乙的作用是:______________________ 。
③若丁装置中为NaOH与酚酞的混合溶液,将氯气通入丁装置中,溶液红色褪去,则推测可能的原因是:
a.________________________________________ ;
b.________________________________________ 。
①3S+6KOH
 K2SO3+2K2S+3H2O
K2SO3+2K2S+3H2O②2FeCl3+Cu=2FeCl2+CuCl2
(2)现用如图所示的装置制取饱和氯水,请回答有关问题:

①写出装置甲中发生反应的化学方程式:
②装置乙的作用是:
③若丁装置中为NaOH与酚酞的混合溶液,将氯气通入丁装置中,溶液红色褪去,则推测可能的原因是:
a.
b.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E五种物质焰色反应均为黄色,它们按图所示关系相互转化.
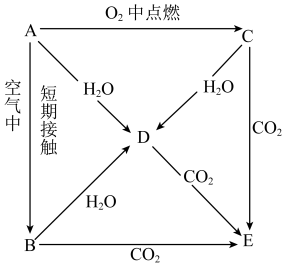
(1)这五种物质中,A:___________ 、 C: ___________ .
(2)将CO2通入E的饱和溶液中,该反应的离子方程式为______________________________ .
(3)写出A→D、C→D、C→E反应的化学方程式
A→D:___________________________ .
C→D:___________________________ .
C→E:___________________________ .

(1)这五种物质中,A:
(2)将CO2通入E的饱和溶液中,该反应的离子方程式为
(3)写出A→D、C→D、C→E反应的化学方程式
A→D:
C→D:
C→E:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组探究金属钠与水在不同实验装置中的反应情况。

(1)钠与水反应的化学方程式是_______ 。
(2)钠放入甲中水槽后的实验现象是_______ 。
(3)按图乙所示方法收集钠与水反应产生的气体并进行定量计算 。实验方法是:先在某金属箔纸上扎一些小孔,然后用此金属箔纸包住钠,将钠放入水中的同时用试管收集气体。为达到实验目的,金属箔纸应该是_______ (填“铜箔”或“铝箔”)。
(4)向丙中试管放入一小块钠,开始钠沉入煤油和水的交界处与水反应,而后又浮到煤油层,在煤油和水层界面之间上下跳动,持续进行直至钠消耗完全,解释产生上述现象的原因_______ 。

(1)钠与水反应的化学方程式是
(2)钠放入甲中水槽后的实验现象是
(3)按图乙所示方法
(4)向丙中试管放入一小块钠,开始钠沉入煤油和水的交界处与水反应,而后又浮到煤油层,在煤油和水层界面之间上下跳动,持续进行直至钠消耗完全,解释产生上述现象的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】立足教材实验是掌握高中化学实验的基础,是理解化学科学的实验原理、实验方法和实验思路,提高学生实验能力的基本途径:
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是_________ ;
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——______________ ;
(3)实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是_________
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比铝的熔点高 D.用砂纸打磨不能除去表面的氧化膜
(4)实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验生成的气体,向反应后的溶液中加入酚酞试液,溶液中可以看到__________________________________________
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是__________ ,该反应每消耗1mol铁,转移电子的物质的量为_________ 。
(6)实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜色变化的原因是(用化学方程式表示):________________________________ 。
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——
(3)实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比铝的熔点高 D.用砂纸打磨不能除去表面的氧化膜
(4)实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验生成的气体,向反应后的溶液中加入酚酞试液,溶液中可以看到
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是
(6)实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜色变化的原因是(用化学方程式表示):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去),X中一定含有碳元素。
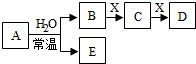
(1)若A为金属单质,B的焰色反应为黄色,请写出A与水反应的离子方程式_____ ,B与D反应的离子方程式_______________________________ 。
(2)若A为非金属单质,A与水反应时,H2O既不是氧化剂也不是还原剂,则E的结构式为__________ ,写出B与D反应的离子方程式_________________________ 。
(3)若A为化合物,E为离子化合物,请写出E的电子式__________________ ,写出B与D反应的化学方程式______________________________________ 。

(1)若A为金属单质,B的焰色反应为黄色,请写出A与水反应的离子方程式
(2)若A为非金属单质,A与水反应时,H2O既不是氧化剂也不是还原剂,则E的结构式为
(3)若A为化合物,E为离子化合物,请写出E的电子式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】喷泉实验是一种常见的现象,其产生原因是存在压强差。试根据图,回答下列问题:

(1)甲装置为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中盛有液体。下列组合不可能产生喷泉的是___________(填标号,下同)。
(2)在乙装置的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是___________。
(3)丙装置,引发喷泉的操作是___________ 。若在乙装置的锥形瓶中装入水,圆底烧瓶中充满NH3,引发喷泉的操作是___________ 。
(4)实验室中有时可以用Mg3N2同水作用制备氨气,同时生成Mg(OH)2,该反应的化学方程式为___________ 。
(5)液氨可以溶解碱金属单质,反应后溶液呈蓝色。该反应和碱金属单质与水的反应相似,请写出液氨与金属钠反应的化学方程式___________ ;在液氨中,氨分子间存在一种比化学键弱,但比范德华力强的作用,叫做___________ 。

(1)甲装置为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中盛有液体。下列组合不可能产生喷泉的是___________(填标号,下同)。
| A.CO2和饱和NaHCO3溶液 | B.NH3和H2O |
| C.HCl和NaOH溶液 | D.NH3和稀盐酸 |
| A.MnO2与双氧水 | B.Na2SO4与稀硝酸 |
| C.Cu与浓硫酸 | D.Na2SO3与稀硝酸 |
(4)实验室中有时可以用Mg3N2同水作用制备氨气,同时生成Mg(OH)2,该反应的化学方程式为
(5)液氨可以溶解碱金属单质,反应后溶液呈蓝色。该反应和碱金属单质与水的反应相似,请写出液氨与金属钠反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为探究苯与溴的取代反应,甲同学用装置I进行如下实验:
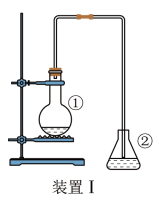
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3-5分钟后发现滴有AgNO3溶液的锥形瓶中有浅黄色沉淀生成,即证明苯与溴发生了取代反应。
(1)装置I中①的化学方程式为__________________________________________________ 。
(2)①中长导管的作用是______________________________________________ 。
(3)要得到纯净的产物,可用稀NaOH溶液、蒸馏水洗涤。洗涤分离粗产品后,要进一步提纯,下列操作中必须的是________ (填入正确选项前的字母);
A 重结晶 B 过滤 C 蒸馏 D 萃取
(4)乙同学设计如图所示装置II,并用下列某些试剂完成该实验。可选用的试剂是:苯、液溴、浓硫酸、氢氧化钠溶液、硝酸银溶液、四氯化碳。

① 能证明苯和液溴发生的是取代反应,而不是加成反应,则试管b中应加入___________ ,其作用是_________________________ ;试管c中应加入________________ 。
② 比较两套装置,装置II的主要优点是_____________________________________ 。(答出一点即可)

将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3-5分钟后发现滴有AgNO3溶液的锥形瓶中有浅黄色沉淀生成,即证明苯与溴发生了取代反应。
(1)装置I中①的化学方程式为
(2)①中长导管的作用是
(3)要得到纯净的产物,可用稀NaOH溶液、蒸馏水洗涤。洗涤分离粗产品后,要进一步提纯,下列操作中必须的是
A 重结晶 B 过滤 C 蒸馏 D 萃取
(4)乙同学设计如图所示装置II,并用下列某些试剂完成该实验。可选用的试剂是:苯、液溴、浓硫酸、氢氧化钠溶液、硝酸银溶液、四氯化碳。

① 能证明苯和液溴发生的是取代反应,而不是加成反应,则试管b中应加入
② 比较两套装置,装置II的主要优点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组利用装置Ⅰ制取 (加热装置未标注),并对
(加热装置未标注),并对 的性质进行实验探究。
的性质进行实验探究。
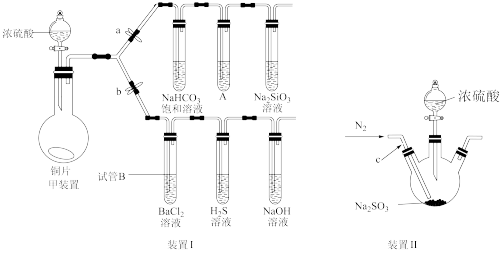
(1)组装好仪器后,首先进行的操作为_______ 。
(2)甲装置中反应的化学方程式是_______ 。
(3)该学习小组当中某同学提出将装置Ⅰ中的甲装置替换成装置Ⅱ会更好,则选择装置Ⅱ的优点在于:_______ 。
(4)按照该同学提议替换装置后,打开弹簧夹a、b,通入一段时间氮气,关闭弹簧夹c,停止通氮气。
①关闭弹簧夹a,打开弹簧夹b,向三颈烧瓶中滴加浓硫酸(体积分数70%)。实验过程中试管B中没有明显变化,盛装 溶液的试管中出现淡黄色浑浊,该实验证明二氧化硫具有
溶液的试管中出现淡黄色浑浊,该实验证明二氧化硫具有_______ 性。实验结束后取下试管B,从中取少量溶液于洁净的试管中。向试管中通入如下的气体,能使试管内的溶液产生白色沉淀的是_______ (填字母)
a. b.
b. c.
c. d.
d.
②若对碳、硅的非金属性相对强弱进行实验验证。试管A中盛装的试剂为_______ 。关闭弹簧夹b,打开弹簧夹a,向三颈烧瓶中滴加浓硫酸(体积分数70%),能够说明碳的非金属性比硅强的实验现象为_______ ,该实验同时也能说明酸性
_______  (填“>”或“<”)。
(填“>”或“<”)。
 (加热装置未标注),并对
(加热装置未标注),并对 的性质进行实验探究。
的性质进行实验探究。
(1)组装好仪器后,首先进行的操作为
(2)甲装置中反应的化学方程式是
(3)该学习小组当中某同学提出将装置Ⅰ中的甲装置替换成装置Ⅱ会更好,则选择装置Ⅱ的优点在于:
(4)按照该同学提议替换装置后,打开弹簧夹a、b,通入一段时间氮气,关闭弹簧夹c,停止通氮气。
①关闭弹簧夹a,打开弹簧夹b,向三颈烧瓶中滴加浓硫酸(体积分数70%)。实验过程中试管B中没有明显变化,盛装
 溶液的试管中出现淡黄色浑浊,该实验证明二氧化硫具有
溶液的试管中出现淡黄色浑浊,该实验证明二氧化硫具有a.
 b.
b. c.
c. d.
d.
②若对碳、硅的非金属性相对强弱进行实验验证。试管A中盛装的试剂为

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是________ 。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙、丁四名同学进行Fe(OH)3胶体的制备
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热。请评价该操作是否正确______________ 。
②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确____________ 。
(3)写出制备Fe(OH)3胶体的化学方程式:_________________ 。
(4)怎样检验制备的物质是否为胶体?___________________ 。
(5)取少量制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是___________ ,这种现象称为胶体的____________ 。
(6)氢氧化铁胶体稳定存在的主要原因是__________ 。
A.胶粒直径小于1 nm B.胶粒带正电荷
C.胶粒作布朗运动 D.胶粒能透过滤纸
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙、丁四名同学进行Fe(OH)3胶体的制备
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热。请评价该操作是否正确
②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确
(3)写出制备Fe(OH)3胶体的化学方程式:
(4)怎样检验制备的物质是否为胶体?
(5)取少量制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是
(6)氢氧化铁胶体稳定存在的主要原因是
A.胶粒直径小于1 nm B.胶粒带正电荷
C.胶粒作布朗运动 D.胶粒能透过滤纸
您最近一年使用:0次



