立足教材实验是掌握高中化学实验的基础,是理解化学科学的实验原理、实验方法和实验思路,提高学生实验能力的基本途径:
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是_________ ;
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——______________ ;
(3)实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是_________
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比铝的熔点高 D.用砂纸打磨不能除去表面的氧化膜
(4)实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验生成的气体,向反应后的溶液中加入酚酞试液,溶液中可以看到__________________________________________
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是__________ ,该反应每消耗1mol铁,转移电子的物质的量为_________ 。
(6)实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜色变化的原因是(用化学方程式表示):________________________________ 。
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——
(3)实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比铝的熔点高 D.用砂纸打磨不能除去表面的氧化膜
(4)实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验生成的气体,向反应后的溶液中加入酚酞试液,溶液中可以看到
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是
(6)实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜色变化的原因是(用化学方程式表示):
更新时间:2017-12-08 23:09:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________ 。


(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________ 。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________ 。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________ 。将所得沉淀过滤、洗涤、灼烧,可得到___________ g固体。
(1)物质X的名称



(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,B为淡黄色粉末。请填写下列空白:

(1)写出下列物质的化学式:A___________ ,B___________ ,C___________ ,D___________ 。
(2)写出下列反应的离子方程式、化学方程式:

___________ ,
___________ 。

(1)写出下列物质的化学式:A
(2)写出下列反应的离子方程式、化学方程式:


您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知B为碱性氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药剂;物质的转化关系如下图所示,请回答下列问题:

(1)请写出下列物质的化学式:A_______ 、E_______ 。
(2)请写出下列反应的化学方程式:A→C:_______ ;D→E:_______ ;F→E:_______ 。
(3)将2.3gA投入47.8g水中,所得溶液质量分数为_______ (用百分数表示)。若把A投入盛有 的溶液中,溶液中出现
的溶液中,溶液中出现_______ (填沉淀颜色)沉淀。

(1)请写出下列物质的化学式:A
(2)请写出下列反应的化学方程式:A→C:
(3)将2.3gA投入47.8g水中,所得溶液质量分数为
 的溶液中,溶液中出现
的溶液中,溶液中出现
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物。B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。请回答下列问题:

(1)甲__________ ;D__________ ;G__________ 。
(2)画出C中阳离子的结构示意图:__________ 。
(3)在空气中将C溶液滴入F溶液中,观察到的现象是____________________ 。
(4)反应①-⑤中,既属于化合反应又属于氧化还原反应的是__________ (填序号)。
(5)A与B反应的离子方程式为____________ 。
(6)实验室中存放氯化亚铁溶液,经常在其中放入表面除锈的铁钉,目的是______________ 。
(7)在配制G时,由于实验员失误,可能导致溶液中含有少量的F,为帮助实验员进行检验少量F的存在,请从下列物质中选择合适的试剂__________ 。
A KSCN溶液 B 稀盐酸 C KMnO4溶液 D NaOH溶液

(1)甲
(2)画出C中阳离子的结构示意图:
(3)在空气中将C溶液滴入F溶液中,观察到的现象是
(4)反应①-⑤中,既属于化合反应又属于氧化还原反应的是
(5)A与B反应的离子方程式为
(6)实验室中存放氯化亚铁溶液,经常在其中放入表面除锈的铁钉,目的是
(7)在配制G时,由于实验员失误,可能导致溶液中含有少量的F,为帮助实验员进行检验少量F的存在,请从下列物质中选择合适的试剂
A KSCN溶液 B 稀盐酸 C KMnO4溶液 D NaOH溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】如图1是钠及其化合物与水反应关系图,两圆圈相交的部分表示圆圈内的物质相互发生的反应,请按要求填空。
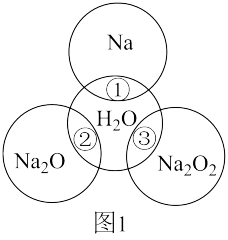
(1)反应①的化学方程式___________ 。
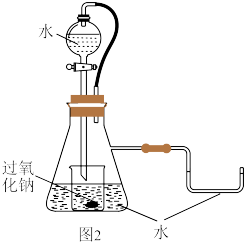
(2)研究性学习小组设计图2装置探究反应③是放热反应。
i、向烧杯内滴加水时,可观察到的现象是___________ 。
ⅱ、该反应的化学方程式为___________ 。
ⅲ、举例过氧化钠的用途___________ 。(写一种)
(3)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式___________ 。


(1)反应①的化学方程式
(2)研究性学习小组设计图2装置探究反应③是放热反应。
i、向烧杯内滴加水时,可观察到的现象是
ⅱ、该反应的化学方程式为
ⅲ、举例过氧化钠的用途
(3)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】1-18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质。
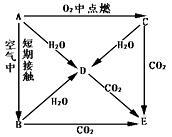
(1)写出A→E的化学式:A____________ 、
B_____________ 、C_____________ 、
D_____________ 、E_____________ 。
(2)写出A→D反应的离子方程式
A→D______________________________________ 。
(3)写出C→D、C→E反应的化学方程式,并标出电子转移的方向和数目。
C→D___________________________________________________ 。(双线桥)
C→E___________________________________________________ 。(双线桥)

(1)写出A→E的化学式:A
B
D
(2)写出A→D反应的离子方程式
A→D
(3)写出C→D、C→E反应的化学方程式,并标出电子转移的方向和数目。
C→D
C→E
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下图中的A~I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两种元素质量之比为3∶4;B元素在地壳中的含量位居第三;C由三种元素组成;G为紫红色。图中“——”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。

(1)写出G的化学式:
(2)反应①、②和③的基本反应类型相同,该基本反应类型
(3)写出B→A反应的化学方程式:
(4)写出H与D₁反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】人类的生产和生活都离不开金属。
(一)金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大致年代如图所示:
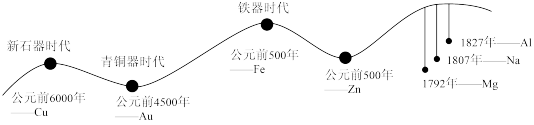
(1)由图可知人类最早使用的合金是___________ ;通过敲打可将金属材料打制成不同的形状,是利用了金属的___________ 性。
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾(硫酸铜晶体),熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是___________ (填序号)
A.“苦泉”的溶质之一——CuSO4
B.“挹其水之”——蒸发溶剂
C.“熬胆矾铁釜,久之亦化为铜”——发生置换反应
(3)铝的利用距今100多年,现在铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是________ (用化学方程式表示)
(二)实验室探究铜的冶炼
已知: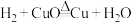 。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。
。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。
I、设计如图1实验装置,开展氢气还原氧化铜实验并检验固体产物。

(4)图1中制取氢气的化学反应方程式为____________________________________________ 。
(5)实验开始时,___________ (填序号)
A.先向长颈漏斗中加稀硫酸后点酒精灯 B.先点燃酒精灯加热后向长颈漏斗中加稀硫酸
(6)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到___________ ,证明固体产物有Cu2O。
II、探究反应生成Cu2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图2。
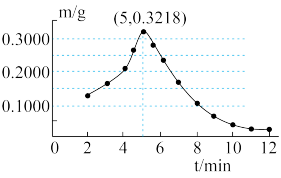
(7)由图2可知,在氢气还原氧化铜反应过程中,Cu2O质量的变化趋势是____________ 。
(8)为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是___________ 。
III、探究反应生成Cu2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1:经历 ,
, 两个反应,且在同一条件下两个反应同时进行。
两个反应,且在同一条件下两个反应同时进行。
假设2:依次经历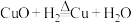 、
、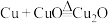 、
、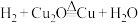 三个反应。
三个反应。
(9)结合探究II的结果,通过计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是___________________ 。(写出合理的推理过程)
(三)用废铜屑生产硫酸铜晶体(CuSO4∙5H2O)的流程如下:
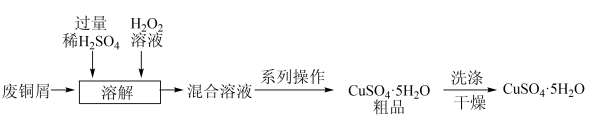
(10)“溶解”时发生的化学反应方程式为___________________ 。
(11)“洗涤、干燥”过程中常用95%的酒精做洗涤剂,优点是_________ 。
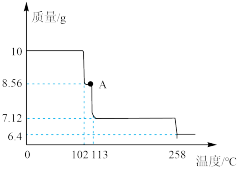
(12)取10g CuSO4∙5H2O,其受热脱水过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示。则晶体CuSO4∙3H2O存在的最高温度约为___________ 。
(一)金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大致年代如图所示:

(1)由图可知人类最早使用的合金是
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾(硫酸铜晶体),熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是
A.“苦泉”的溶质之一——CuSO4
B.“挹其水之”——蒸发溶剂
C.“熬胆矾铁釜,久之亦化为铜”——发生置换反应
(3)铝的利用距今100多年,现在铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是
(二)实验室探究铜的冶炼
已知:
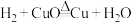 。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。
。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液,某兴趣小组对此开展如下探究。I、设计如图1实验装置,开展氢气还原氧化铜实验并检验固体产物。

(4)图1中制取氢气的化学反应方程式为
(5)实验开始时,
A.先向长颈漏斗中加稀硫酸后点酒精灯 B.先点燃酒精灯加热后向长颈漏斗中加稀硫酸
(6)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到
II、探究反应生成Cu2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图2。

(7)由图2可知,在氢气还原氧化铜反应过程中,Cu2O质量的变化趋势是
(8)为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是
III、探究反应生成Cu2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1:经历
 ,
, 两个反应,且在同一条件下两个反应同时进行。
两个反应,且在同一条件下两个反应同时进行。假设2:依次经历
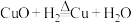 、
、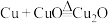 、
、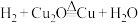 三个反应。
三个反应。(9)结合探究II的结果,通过计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是
(三)用废铜屑生产硫酸铜晶体(CuSO4∙5H2O)的流程如下:

(10)“溶解”时发生的化学反应方程式为
(11)“洗涤、干燥”过程中常用95%的酒精做洗涤剂,优点是
(12)取10g CuSO4∙5H2O,其受热脱水过程的热重曲线(剩余固体质量随温度变化的曲线)如图所示。则晶体CuSO4∙3H2O存在的最高温度约为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(1)预测Al能和CuSO4溶液反应,理由是_______ 。
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
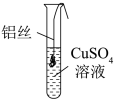
(2)铝丝表面未出现红色物质,原因是_______ (用化学方程式解释)。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(3)填写实验报告单:
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为_______ 。
(5)欲加快Al和CuSO4溶液的反应,可加入的物质是_______ (填一种即可)。
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是_______(填序号)。
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(1)预测Al能和CuSO4溶液反应,理由是
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。

(2)铝丝表面未出现红色物质,原因是
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(3)填写实验报告单:
| 序号 | 实验现象 | 结论与解释 |
| ① | 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与Al反应产生的气体是 |
| ② | 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 | 红色物质是 |
| ③ | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色:两层溶液界面清晰 | 反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度 |
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为
(5)欲加快Al和CuSO4溶液的反应,可加入的物质是
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是_______(填序号)。
| A.食醋 | B.食用油 | C.面粉 | D.咸菜 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。资料显示:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。如下两个装置可在不同温度下进行该反应并验证产物。

(1)甲装置中仪器a的名称为_____ 。
(2)装置甲验证气体产物的操作是____ 。装置C的作用是____ 。
(3)A同学取出少量乙装置中实验结束后的固体物质于另一试管中,加入少量盐酸,微热,观察到黑色粉末逐渐溶解,溶液呈浅绿色,有少量气泡产生。再向溶液中滴加几滴KSCN溶液,振荡,溶液没有出现红色,推断该条件下生成FeO,B同学却不同意该结论,他的理由是___ 。

(1)甲装置中仪器a的名称为
(2)装置甲验证气体产物的操作是
(3)A同学取出少量乙装置中实验结束后的固体物质于另一试管中,加入少量盐酸,微热,观察到黑色粉末逐渐溶解,溶液呈浅绿色,有少量气泡产生。再向溶液中滴加几滴KSCN溶液,振荡,溶液没有出现红色,推断该条件下生成FeO,B同学却不同意该结论,他的理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Fe与水蒸气反应,如图所示
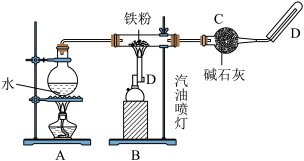
(1)在D处玻璃管口点燃生成的气体前,必须对该气体进行___________ 。
(2)B中反应的化学方程式:___________ 。
(3)当有16.8 g铁粉参加反应时,生成的气体在标准状况下的体积是___________ L。
(4)除去FeCl2中混有的FeCl3,可加入___________ ,反应的离子方程式为___________
(5)除去FeCl3中混有的FeCl2,可加入___________ ,反应的离子方程式为___________
(6)写出氢氧化钠溶液与铝反应的化学方程式___________

(1)在D处玻璃管口点燃生成的气体前,必须对该气体进行
(2)B中反应的化学方程式:
(3)当有16.8 g铁粉参加反应时,生成的气体在标准状况下的体积是
(4)除去FeCl2中混有的FeCl3,可加入
(5)除去FeCl3中混有的FeCl2,可加入
(6)写出氢氧化钠溶液与铝反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有四种元素,分别位于元素周期表的前四个不同周期,其原子序数总和为48。由它们可组成甲、乙、丙、丁四种单质和A、B、C、D四种化合物,其中甲、乙为非金属单质,丙、丁为金属单质;这些物质间的转化关系如下图所示(反应条件已省略)。
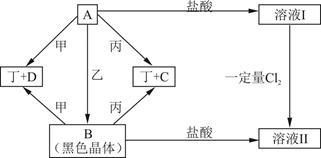
请回答下列问题:
(1)组成丁的元素在周期表中的位置________ ,B的俗名__________ ,C物质的用途之一___________ 。
(2)写出A+乙 B的化学方程式
B的化学方程式________________ 。
(3)在加热条件下,丁与气态D可发生反应,该反应的化学方程式为__________ 。
(4)若21.6g A与适量的乙反应生成B,A、B按上述图示转化为溶液I和溶液II(假设各步反应均恰好进行完全);向溶液I中通入________ mol Cl2,经充分反应可恰好使溶质的组成与溶液II完全相同。

请回答下列问题:
(1)组成丁的元素在周期表中的位置
(2)写出A+乙
 B的化学方程式
B的化学方程式(3)在加热条件下,丁与气态D可发生反应,该反应的化学方程式为
(4)若21.6g A与适量的乙反应生成B,A、B按上述图示转化为溶液I和溶液II(假设各步反应均恰好进行完全);向溶液I中通入
您最近一年使用:0次



