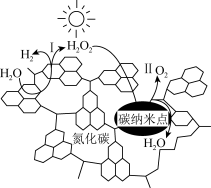
我国化学家研究的一种新型光催化剂(碳纳米点/氮化碳)可以利用太阳光高效实现分解水,其原理如图所示,下列说法不正确的是

| A.碳纳米纳米点和氮化碳均为新型无机非金属材料 |
| B.若反应Ⅱ是放热反应,则反应Ⅰ一定是吸热反应 |
| C.反应Ⅰ和反应Ⅱ均存在O-H键的断裂 |
D.总反应为H2O2  H2+O2 H2+O2 |
更新时间:2024-01-28 13:33:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.浓硫酸溶于水共价键断裂并放出大量的热,所以该过程是放热反应 |
| B.吸热反应一定要在加热或高温条件下才能进行 |
| C.物质发生化学反应都伴随着能量变化 |
| D.焰色反应有能量变化,所以焰色反应是化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应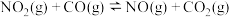 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
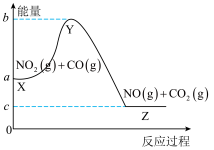
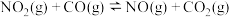 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
| A.图中X→Z为吸热过程 |
| B.理论上该反应不可以设计成原电池 |
| C.升高温度,正反应速率加快,逆反应速率减慢 |
| D.图中X→Y表示反应物断键时吸收能量的过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是( )
| A.测定HCl和NaOH中和反应的反应热时,单次实验均应测量3个温度,即盐酸起始温度、NaOH溶液起始温度和反应终止温度 |
| B.若2C(s)+O2(g)=2CO(g)△H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D.已知I:反应H2(g)+Cl2(g)=2HCl(g);△H=-a kJ/mol II:  且a、b、c均大于零,则断开1molH-Cl键所需的能量为2(a+b+c)kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
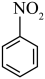
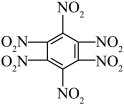
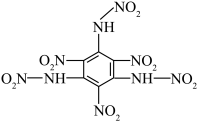
【推荐1】炸药广泛应用于爆破工程。我国科学家近日取得突破,合成了一种高能量且稳定性相对较好的炸药TNTNB.下表罗列了一类炸药的演变历史及相关性质,下列说法错误的是
| 硝基苯 | TNT(1863年) | HNB(1966年) | TNTNB(2023年) | |
| 结构式 |
|
|
|
|
 数量: 数量: | 1 | 3 | 6 | 6 |
| 相对能量Q: |  |  | 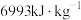 | 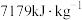 |
A.浓硝酸、浓硫酸、甲苯混合物在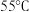 水浴加热可制取TNT 水浴加热可制取TNT |
| B.苯环数量相同的条件下,硝基数量越多,炸药能量越高 |
C.热化学方程式: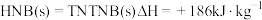 |
| D.TNTNB分子中有三种不同化学环境的N原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某些物质的燃烧热如下表:
乙烷与氢气反应生成甲烷的热化学方程式为
| 物质 | 氢气 | 甲烷 | 乙烷 |
燃烧热△H( ) ) | -285.8 | -891.0 | -1560.8 |
A.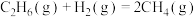  |
B.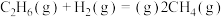 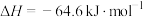 |
C.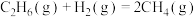 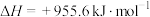 |
D.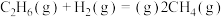 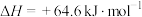 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220kJ·mol-1
②断裂1 mol H2(g)中的H—H键需要吸收436 kJ的能量,断裂1mol O2(g)中的共价键需要吸收496kJ的能量,生成H2O(g)中的1 mol H—O键能放出462 kJ的能量。则下列说法正确的是
2C(s)+O2(g)=2CO(g) ΔH2=-220kJ·mol-1
②断裂1 mol H2(g)中的H—H键需要吸收436 kJ的能量,断裂1mol O2(g)中的共价键需要吸收496kJ的能量,生成H2O(g)中的1 mol H—O键能放出462 kJ的能量。则下列说法正确的是
| A.断裂1 mol H2O(l)中化学键形成H、O原子的过程中需吸收的能量为924 kJ |
| B.a的值为-130 |
| C.2H2(g)+O2(g)=2H2O(g) ΔH =-(220+2a)kJ·mol-1 |
| D.加入某一催化剂能同等程度降低ΔH1、ΔH2的大小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】H2与ICl的反应分两步完成,其能量曲线如图所示。
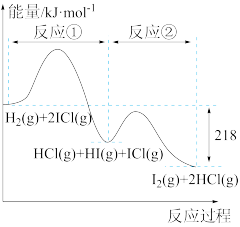
反应①:H2(g)+2ICl(g)=HCl(g)+HI(g)+ICl(g)
反应②:HCl(g)+HI(g)+ICl(g)=I2(g)+2HCl(g)
下列有关说法不正确的是

反应①:H2(g)+2ICl(g)=HCl(g)+HI(g)+ICl(g)
反应②:HCl(g)+HI(g)+ICl(g)=I2(g)+2HCl(g)
下列有关说法不正确的是
| A.反应①的能垒比反应②的大,所以总反应的反应速率取决于第②步反应 |
| B.反应①、②均是反应物总能量高于生成物总能量 |
| C.H2(g)+2ICl(g)=I2(g)+2HCl(g) △H=-218kJ•mol-1 |
| D.温度升高,活化分子百分数增大,反应碰撞概率增大,反应速率加快 |
您最近一年使用:0次
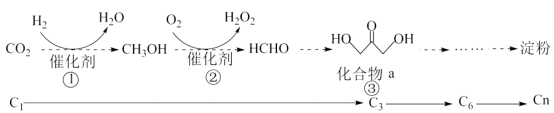
【推荐2】2021年我国科学家以 为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如下图所示。下列有关说法不正确的是
为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如下图所示。下列有关说法不正确的是
 为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如下图所示。下列有关说法不正确的是
为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如下图所示。下列有关说法不正确的是
| A.反应①实现了从无机物到有机物的转化 |
B.反应②为 ,有机反应类型属于氧化反应 ,有机反应类型属于氧化反应 |
C. 化合物a最多能与 化合物a最多能与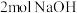 发生中和反应 发生中和反应 |
D. 水溶液能使蛋白质发生变性 水溶液能使蛋白质发生变性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对丙烷进行溴代反应,反应一段时间后得到如下结果:2CH3CH2CH3+Br2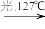 CH3CH2CH2Br(3%)+CH3CHBrCH3(97%)+2HBr
CH3CH2CH2Br(3%)+CH3CHBrCH3(97%)+2HBr
已知:正丙基结构简式CH3CH2CH2-、异丙基结构简式(CH3)2CH-,反应机理中链转移决速步为RH+Br·→R·+HBr,其反应势能变化如图所示。下列说法正确的是
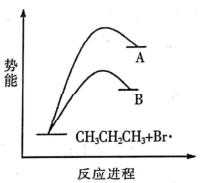
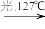 CH3CH2CH2Br(3%)+CH3CHBrCH3(97%)+2HBr
CH3CH2CH2Br(3%)+CH3CHBrCH3(97%)+2HBr已知:正丙基结构简式CH3CH2CH2-、异丙基结构简式(CH3)2CH-,反应机理中链转移决速步为RH+Br·→R·+HBr,其反应势能变化如图所示。下列说法正确的是

| A.物质组合A为异丙基+HBr |
| B.生成正丙基过程的活化能大于生成异丙基过程的活化能 |
| C.正丙基的稳定性强于异丙基 |
| D.溴原子取代的位置只取决于反应物与生成物的能量变化 |
您最近一年使用:0次