在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:
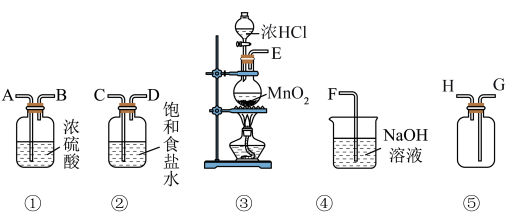
(1)连接上述仪器的正确顺序(填各接口处的字母):__________ E接____;____接____;____接____;____接F。
(2)装置中,饱和食盐水的作用是__________ 。
(3)化学实验中常用湿润的淀粉 试纸检验是否有
试纸检验是否有 产生。如果有
产生。如果有 产生,可观察到
产生,可观察到__________ ,反应方程式______________________________ 。
(4) 的氧化性比
的氧化性比 强得多,实验室也可以消
强得多,实验室也可以消 固体和浓盐酸反以制取氯气,反应方程式如下:
固体和浓盐酸反以制取氯气,反应方程式如下: 。该反应中被氧化和未被氧化的盐酸的物质的量之比是
。该反应中被氧化和未被氧化的盐酸的物质的量之比是__________ ,如果将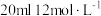 的浓盐酸与足量
的浓盐酸与足量 充分反应,实际能收集到的氯气在标准状况下的体积将
充分反应,实际能收集到的氯气在标准状况下的体积将__________ 。
A. B.
B. C.
C. D.
D.

(1)连接上述仪器的正确顺序(填各接口处的字母):
(2)装置中,饱和食盐水的作用是
(3)化学实验中常用湿润的淀粉
 试纸检验是否有
试纸检验是否有 产生。如果有
产生。如果有 产生,可观察到
产生,可观察到(4)
 的氧化性比
的氧化性比 强得多,实验室也可以消
强得多,实验室也可以消 固体和浓盐酸反以制取氯气,反应方程式如下:
固体和浓盐酸反以制取氯气,反应方程式如下: 。该反应中被氧化和未被氧化的盐酸的物质的量之比是
。该反应中被氧化和未被氧化的盐酸的物质的量之比是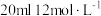 的浓盐酸与足量
的浓盐酸与足量 充分反应,实际能收集到的氯气在标准状况下的体积将
充分反应,实际能收集到的氯气在标准状况下的体积将A.
 B.
B. C.
C. D.
D.
更新时间:2024-01-29 10:29:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】草酸与高锰酸钾在酸性条件下能够发生反应: MnO +H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
通过下表实验探究外界因素对反应速率的影响。
(1)该反应中氧化剂和还原剂的物质的量之比为___________ 。
(2)其中T1=___________ ;V2=___________ 。
(3)若t1 <8,则由实验可得出的结论是___________ ;忽略溶液体积的变化,利用实验B中的数据计算,0~8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=___________ 。
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO 该反应有催化作用
该反应有催化作用
丙同学认为假设3不合理,其理由是___________ 。
②丁同学用如下实验证明假设2:除了酸性高锰酸钾和草酸外,还需要选择的试剂是___________ 。(填化学式)
 +H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)通过下表实验探究外界因素对反应速率的影响。
| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
| A | 293 | 4 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 4 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 4 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)其中T1=
(3)若t1 <8,则由实验可得出的结论是
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO
 该反应有催化作用
该反应有催化作用丙同学认为假设3不合理,其理由是
②丁同学用如下实验证明假设2:除了酸性高锰酸钾和草酸外,还需要选择的试剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业的汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为_________________________________________________________ ;
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式)_____________________ ;该反应是氧化还原反应,则其中的氧化剂是(填化学式)__________________________________________________ 。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为__________________________________
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式)
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】部分氯及铁的单质和化合物“价—类”图如下:

回答下列问题:
(1)d的电子式为___________ 。
(2)实验室采用固体和浓a溶液加热制备b,写出离子方程式:___________ ;在该反应中,氧化剂与还原剂的物质的量之比为___________ 。
(3)在酚酞溶液中滴加足量c的钠盐水溶液,观察到溶液先变红色后很快褪色,其原因是___________ (用离子方程式表示)。c的钠盐溶液中离子浓度大小排序为___________ 。
(4)f在空气中加热所得固体产物的化学式为___________ 。取少量i溶液于试管中,加入适量氢氧化钠溶液能观察到的现象是___________ ,将制得的g置于空气中生成h的化学方程式为___________ 。
(5)在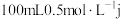 的氯化物水溶液中加入e,反应后的溶液中含浓度相等的2种金属离子(不考虑盐类水解),则溶解e的质量为
的氯化物水溶液中加入e,反应后的溶液中含浓度相等的2种金属离子(不考虑盐类水解),则溶解e的质量为___________ g。

回答下列问题:
(1)d的电子式为
(2)实验室采用固体和浓a溶液加热制备b,写出离子方程式:
(3)在酚酞溶液中滴加足量c的钠盐水溶液,观察到溶液先变红色后很快褪色,其原因是
(4)f在空气中加热所得固体产物的化学式为
(5)在
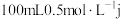 的氯化物水溶液中加入e,反应后的溶液中含浓度相等的2种金属离子(不考虑盐类水解),则溶解e的质量为
的氯化物水溶液中加入e,反应后的溶液中含浓度相等的2种金属离子(不考虑盐类水解),则溶解e的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】 是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用
是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用 与
与 反应制得
反应制得 和
和 。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的
。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的 的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
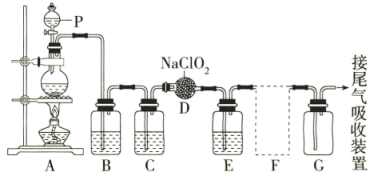
(1)仪器P的名称是________ 。
(2)请写出装置A中烧瓶内发生反应的化学方程式:__________ 。
(3)装置B、C中所盛试剂分别是________ 、__________ 。
(4)F为 收集装置,应选用下图的哪组装置来收集
收集装置,应选用下图的哪组装置来收集_______ (填序号),其中与装置E导管相连的导管口是______ (填接口字母)。
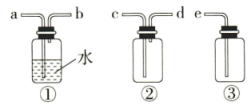
(5)装置D中发生反应的化学方程式为________ 。
(6) 与
与 反应可以得到以
反应可以得到以 为有效成分的漂白液,请用离子方程式表示该反应:
为有效成分的漂白液,请用离子方程式表示该反应:________ 。将 通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中
通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中 反应,
反应, 为
为_______ (填“酸性氧化物”或“碱性氧化物”)。
 是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用
是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用 与
与 反应制得
反应制得 和
和 。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的
。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的 的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
(1)仪器P的名称是
(2)请写出装置A中烧瓶内发生反应的化学方程式:
(3)装置B、C中所盛试剂分别是
(4)F为
 收集装置,应选用下图的哪组装置来收集
收集装置,应选用下图的哪组装置来收集
(5)装置D中发生反应的化学方程式为
(6)
 与
与 反应可以得到以
反应可以得到以 为有效成分的漂白液,请用离子方程式表示该反应:
为有效成分的漂白液,请用离子方程式表示该反应: 通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中
通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中 反应,
反应, 为
为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】无水氯化锌是白色固体,易吸水潮解,常用作有机合成的脱水剂、缩合剂和催化剂,还用作活性炭的活化剂。某校化学课题小组的同学设计如下实验方案制备无水 ,并进行纯度测定,涉及的实验装置如图所示:
,并进行纯度测定,涉及的实验装置如图所示:
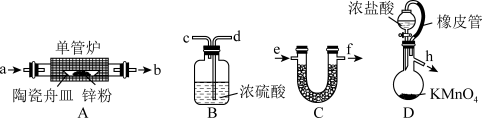
回答下列问题:
(1)按气流从左到右的方向,装置合理的连接顺序为h→_______ (填仪器接口小写字母,装置不可重复使用)。装置D中橡皮管的作用为_______ 。
(2)写出装置D中反应的离子方程式:_______ 。
(3)若省略装置B,经检验产物中含有氧化锌,利用所学知识解释原因:_______ 。
(4)装置C中的药品为_______ ,其作用为_______ 。
(5)氯化锌纯度的测定:取ag试样配成100mL溶液,取25.00mL,加入磷酸三钠消除干扰离子后,滴入两滴半二甲酚橙作指示剂,用bmol/LEDTA( )标准溶液滴定
)标准溶液滴定 ,反应的离子方程式为
,反应的离子方程式为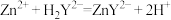 ,达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。
,达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。
①配制100mL 溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、
溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、_______ 。
②该氯化锌试样中氯化锌的质量分数为_______ (用含a、b的代数式表示)。
 ,并进行纯度测定,涉及的实验装置如图所示:
,并进行纯度测定,涉及的实验装置如图所示:
回答下列问题:
(1)按气流从左到右的方向,装置合理的连接顺序为h→
(2)写出装置D中反应的离子方程式:
(3)若省略装置B,经检验产物中含有氧化锌,利用所学知识解释原因:
(4)装置C中的药品为
(5)氯化锌纯度的测定:取ag试样配成100mL溶液,取25.00mL,加入磷酸三钠消除干扰离子后,滴入两滴半二甲酚橙作指示剂,用bmol/LEDTA(
 )标准溶液滴定
)标准溶液滴定 ,反应的离子方程式为
,反应的离子方程式为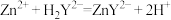 ,达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。
,达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。①配制100mL
 溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、
溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、②该氯化锌试样中氯化锌的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素X、Y、Z、W均为短周期元素,且原子序数依次增大。已知Y原子最外层电子数占核外电子总数的3/4,W-、Z+、X+的离子半径逐渐减小,化合物XW常温下为气体,Z是本周期中除稀有气体元素外,原子半径最大的元素。据此回答下列问题:
(1)W在元素周期表中的位置___________________ ,实验室制取W单质的离子方程式是____________________________________________________________ ;
(2)A、B均由上述四种元素中的三种组成的强电解质,A是一种强碱,B是某种家用消毒液的有效成分,则A、B的化学式分别为___________ 、____________ ;
(3)C是由Y和Z两种元素组成的一种化合物,其中Y和Z的原子个数比为1∶1,则C的电子式是____________ ;
(1)W在元素周期表中的位置
(2)A、B均由上述四种元素中的三种组成的强电解质,A是一种强碱,B是某种家用消毒液的有效成分,则A、B的化学式分别为
(3)C是由Y和Z两种元素组成的一种化合物,其中Y和Z的原子个数比为1∶1,则C的电子式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氧钒(IV)碱式碳酸铵晶体{(NH4)5[(VO)6(CO3)4(OH)9]· 10H2O}是制备多种含钒产品和催化剂的基础原料和前驱体。某兴趣小组用如图所示装置(夹持仪器略去)制备氧钒(IV)碱式碳酸铵晶体。
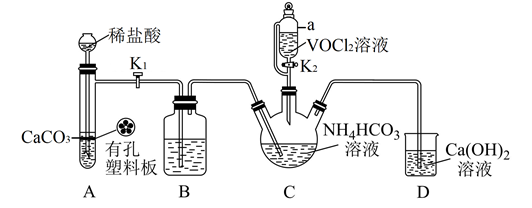
实验步骤如下:
I.向V2O5中加入足量盐酸酸化的N2H4·2HCl溶液,微沸数分钟,将反应液净化后转移到a中。
II.关闭K2,打开K1,待装置中空气排尽后,关闭K1.把制得的VOCl2溶液缓慢加入到足量NH4HCO3溶液中,有气泡产生并析出紫红色晶体。
III.反应结束后将混合液抽滤,产品用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,静置一段时间后得到产品。
已知:氧化性: KMnO4>O2>VO2+, >Fe2+, VO2+空气中易被氧化生成
>Fe2+, VO2+空气中易被氧化生成 ;
;
回答下列问题:
(1)仪器a的名称是_______ ,装置B的作用是_______ 。
(2)步骤II中,当_______ (填实验现象) 时, 关闭K1进行实验,装置C中生成氧钒(IV)碱式碳酸铵晶体的化学方程式_______ 。
(3)步骤III中用饱和NH4HCO3溶液洗涤的原因是_______ 。
(4)称量mg产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后加入KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,用尿素除去过量NaNO2用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点消耗标准溶液的体积为VmL。产品中钒的质量分数为_______ % (以VO2计。用含有m、c、V的式子表示)。
(5)设计实验证明装置C中VOCl2溶液是否变质_______ (供选试剂:KMnO4溶液、盐酸酸化的氯化亚铁溶液、盐酸酸化的氯化铁溶液、KSCN溶液)。

实验步骤如下:
I.向V2O5中加入足量盐酸酸化的N2H4·2HCl溶液,微沸数分钟,将反应液净化后转移到a中。
II.关闭K2,打开K1,待装置中空气排尽后,关闭K1.把制得的VOCl2溶液缓慢加入到足量NH4HCO3溶液中,有气泡产生并析出紫红色晶体。
III.反应结束后将混合液抽滤,产品用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,静置一段时间后得到产品。
已知:氧化性: KMnO4>O2>VO2+,
 >Fe2+, VO2+空气中易被氧化生成
>Fe2+, VO2+空气中易被氧化生成 ;
;回答下列问题:
(1)仪器a的名称是
(2)步骤II中,当
(3)步骤III中用饱和NH4HCO3溶液洗涤的原因是
(4)称量mg产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后加入KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,用尿素除去过量NaNO2用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点消耗标准溶液的体积为VmL。产品中钒的质量分数为
(5)设计实验证明装置C中VOCl2溶液是否变质
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某校化学活动小组做了如下探究实验:
实验一:测定相同体积的1mol/L的硫酸分别与足量锌粒和锌粉反应的速率,设计如图装置:

(1)写出此反应的离子方程式___________ 。
(2)按照图Ⅰ装置实验时,限定了两次实验时间均为10min,则还需要测定的另一个数据是_______ 。
(3)根据此实验探究,可以得出的结论是:其他条件不变时,___________ 。
实验二:利用H2C2O4溶液和酸性KMnO4溶液之间的反应,探究外界条件改变对化学反应速率的影响。实验如下表:
(4)V2 =___________ ;通过实验A、B可探究___________ 的改变对反应速率的影响。
(5)利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=_______ 。
(6)实验中发现:反应一段时间后该反应速率会加快,造成此种变化的原因是:反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是___________ 。
实验一:测定相同体积的1mol/L的硫酸分别与足量锌粒和锌粉反应的速率,设计如图装置:

(1)写出此反应的离子方程式
(2)按照图Ⅰ装置实验时,限定了两次实验时间均为10min,则还需要测定的另一个数据是
(3)根据此实验探究,可以得出的结论是:其他条件不变时,
实验二:利用H2C2O4溶液和酸性KMnO4溶液之间的反应,探究外界条件改变对化学反应速率的影响。实验如下表:
| 序号 | 温度/K | 0.02 mol∙L−1 KMnO4 | 0.1 mol∙L−1 H2C2O4 | H2O | 溶液颜色褪至无色时所需时间/s |
| V/mL | V/mL | V/mL | |||
| A | 293 | 2 | 5 | 3 | t1 |
| B | 293 | V1 | 3 | 5 | 8 |
| C | 313 | 2 | 3 | V2 | t2 |
(5)利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=
(6)实验中发现:反应一段时间后该反应速率会加快,造成此种变化的原因是:反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学小组用下列装置制备氨基甲酸铵(NH2COONH4),其反应原理为:2NH3(g) + CO2(g) = NH2COONH4(s) △H<0。已知:氨基甲酸铵难溶于四氯化碳;易水解生成碳酸氢铵,受热分解可生成尿素。

试回答下列问题:
(1)C装置中橡皮管的作用是___________ ;试剂x可以是___________ 。
(2)用上述装置制取氨基甲酸铵,以上所有装置的正确连接顺序是:___________→___________→E←___________←___________←___________。 (填大写字母)___________
(3)反应时,为了提高氨基甲酸铵的产量,三颈烧瓶应放置在___________ (填“热水浴’或“冷水浴”)中:装置E中浸有稀H2SO4的棉花作用是___________ 。
(4)反应在CCl4的液体中进行的原因是___________ 。
(5)实验制备过程中为了提高氨基甲酸铵纯度,请提出合理措施___________ 。

试回答下列问题:
(1)C装置中橡皮管的作用是
(2)用上述装置制取氨基甲酸铵,以上所有装置的正确连接顺序是:___________→___________→E←___________←___________←___________。 (填大写字母)
(3)反应时,为了提高氨基甲酸铵的产量,三颈烧瓶应放置在
(4)反应在CCl4的液体中进行的原因是
(5)实验制备过程中为了提高氨基甲酸铵纯度,请提出合理措施
您最近一年使用:0次



