A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期数与主族序数相等。请用回答下列问题:
(1)E元素的名称为___________ ;C元素在周期表中的位置为___________ 。
(2)D2C2电子式为___________ ;D2C2与BC2反应的化学方程式为___________ 。
(3)由A、C、D三种元素组成的化合物中含有的化学键有___________ 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是___________ L。
(1)E元素的名称为
(2)D2C2电子式为
(3)由A、C、D三种元素组成的化合物中含有的化学键有
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是
更新时间:2024-01-30 08:11:23
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】元素周期表前18位元素A、B、C、D核电荷数依次增大。A元素原子核内无中子,B元素原子M层电子数比最内层的电子数多1个,C元素的原子最外层电子数是K层电子数的3倍,D-离子电子层结构与氩原子的电子层结构相同。由此推断:
(1)A、B、C、D元素符号依次是_______ 、_______ 、_______ 、_______ 。
(2)①A原子的结构示意图为_______ ;
②C离子的结构示意图为_______ 。
(3)B离子的电子式为_______ ;
(4)D-的电子式为_______ 。
(5)B单质和C单质反应生成的化合物的化学式是_______ 。
(6)与B离子电子层结构相同的微粒有_______ 。(任意写出4种即可)
(1)A、B、C、D元素符号依次是
(2)①A原子的结构示意图为
②C离子的结构示意图为
(3)B离子的电子式为
(4)D-的电子式为
(5)B单质和C单质反应生成的化合物的化学式是
(6)与B离子电子层结构相同的微粒有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】元素周期表的形式多种多样,扇形元素周期表的一部分(1~36号元素)如图所示,对比中学常见的元素周期表,思考扇形元素周期表的填充规律。请用准确的化学符号和用语 回答下列问题:

(1)元素1在元素周期表中的位置_______ 。
(2)比较f、o、k简单离子的半径,由大到小的顺序是_______ (用离子符号表示)。
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式_______ 。
(4)i的最高价氧化物对应水化物的化学式_______ ,比较i、d最简单氢化物的稳定性_______ (用化学式表示)。
(5)比较m、f、g的金属性强弱,由强到弱的顺序是_______ (用元素符号表示)
(6)比较j和h的非金属性强弱,设计简单的实验方案_______ 。

(1)元素1在元素周期表中的位置
(2)比较f、o、k简单离子的半径,由大到小的顺序是
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式
(4)i的最高价氧化物对应水化物的化学式
(5)比较m、f、g的金属性强弱,由强到弱的顺序是
(6)比较j和h的非金属性强弱,设计简单的实验方案
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】有8种短周期元素,随着原子序数的递增(横坐标),其原子半径相对大小、最高正价或最低负价的变化情况如图所示。
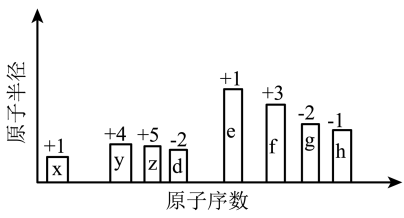
(1)元素h在周期表中的位置是____________ 。
(2)元素x和y形成的最简单化合物在家庭生活中的用途是____________ 。
(3)元素e、f最高价氧化物对应水化物的碱性强的是____________ 。(写化学式)
(4)元素z、x可形成原子个数比为1﹕3的化合物,其电子式为____________ 。

(1)元素h在周期表中的位置是
(2)元素x和y形成的最简单化合物在家庭生活中的用途是
(3)元素e、f最高价氧化物对应水化物的碱性强的是
(4)元素z、x可形成原子个数比为1﹕3的化合物,其电子式为
您最近一年使用:0次
【推荐1】工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3 。其过程如图所示。

请回答:(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有_______ 。
(2)将CaO投入含有大量的NH4C1的母液中,能生成可循环使用的NH3,该反应的化学方程式是_______ 。
(3)向饱和食盐水中首先通入的气体是_______ ,过程III中生成NaHCO3晶体的反应的化学方程式是_______ 。
(4)碳酸钠晶体失水的能量变化示意图如图:

Na2CO3·H2O(s)脱水反应的热化学方程式是_______ 。
(5)产品纯碱中常含有NaCl。取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体。则该产品中Na2CO3的质量分数是_______ 。
(6)熔融Na2CO3可作甲烷-空气燃料电池的电解质,该电池负极的反应式是_______ 。

请回答:(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有
(2)将CaO投入含有大量的NH4C1的母液中,能生成可循环使用的NH3,该反应的化学方程式是
(3)向饱和食盐水中首先通入的气体是
(4)碳酸钠晶体失水的能量变化示意图如图:

Na2CO3·H2O(s)脱水反应的热化学方程式是
(5)产品纯碱中常含有NaCl。取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体。则该产品中Na2CO3的质量分数是
(6)熔融Na2CO3可作甲烷-空气燃料电池的电解质,该电池负极的反应式是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】1273K时H2O(g)通过红热的铁生产H2,发生如下反应:Fe(s)+H2O(g)⇌FeO(s)+H2(g),反应的平衡常数Kp=1.49.(Kp是以各平衡混合气体分压表示的化学平衡常数。)
(1)计算每生产1.00mol氢气需通入水蒸气的物质的量为_____ 。
(2)1273K时,若反应体系中只有0.30mol的铁并通入1.00mol水蒸气与其反应,试计算反应后各组分的物质的量_______ 。反应后体系是否处于平衡状态,为什么_______ 。
(3)1273K,当1.0mnol水蒸气与0.80mol铁接触时,最后各组分的物质的量是________ 。
(1)计算每生产1.00mol氢气需通入水蒸气的物质的量为
(2)1273K时,若反应体系中只有0.30mol的铁并通入1.00mol水蒸气与其反应,试计算反应后各组分的物质的量
(3)1273K,当1.0mnol水蒸气与0.80mol铁接触时,最后各组分的物质的量是
您最近一年使用:0次
【推荐3】海水中含有大量的氯化镁,从海水中提取镁的生产流程如图所示:海水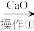 Mg(OH)2
Mg(OH)2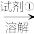 MgCl2
MgCl2 MgCl2·6H2O
MgCl2·6H2O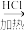 MgCl2
MgCl2 Mg。回答下列问题:
Mg。回答下列问题:
(1)操作①主要是指________ ,写出在海水中加入氧化钙生成氢氧化镁的化学方程式:_______
(2)试剂①可选用________ ,该反应的离子方程式为________ 。
(3)经操作③最终可得金属镁,当得到48g金属镁时,得到氯气的体积(标准状况下)为_____ L。
 Mg(OH)2
Mg(OH)2 MgCl2
MgCl2 MgCl2·6H2O
MgCl2·6H2O MgCl2
MgCl2 Mg。回答下列问题:
Mg。回答下列问题:(1)操作①主要是指
(2)试剂①可选用
(3)经操作③最终可得金属镁,当得到48g金属镁时,得到氯气的体积(标准状况下)为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】如图

A是单质,B为淡黄色固体
请填空:
(1)A是____ (填化学式)
(2)B是____ (填化学式)
(3)C是____ (填化学式)
(4)D是____ (填化学式)
(5)A→B:____ (填化学方程式)。

A是单质,B为淡黄色固体
请填空:
(1)A是
(2)B是
(3)C是
(4)D是
(5)A→B:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E为中学化学常见物质,其中均含同一种金属元素。A为单质,C可用作呼吸面具中的供氧剂,B、E的溶液 均大于7,五种物质之间的转化关系如图所示。请回答下列问题:
均大于7,五种物质之间的转化关系如图所示。请回答下列问题:
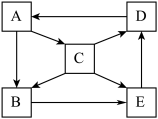
(1) 的化学方程式是
的化学方程式是_______ 。
(2)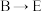 的离子方程式是
的离子方程式是_______ 。
(3) 的化学方程式是
的化学方程式是_______ 。
(4)D的化学式是_______ 。
 均大于7,五种物质之间的转化关系如图所示。请回答下列问题:
均大于7,五种物质之间的转化关系如图所示。请回答下列问题:
(1)
 的化学方程式是
的化学方程式是(2)
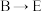 的离子方程式是
的离子方程式是(3)
 的化学方程式是
的化学方程式是(4)D的化学式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】有A、B、C、D四种元素,A元素是地壳中含量最多的金属元素;B元素的原子其M层电子数比L层少1个电子;C元素的原子得到2个电子,D元素的原子失去1个电子,所得到的微粒都具有与氖原子相同的电子层结构。回答下列问题:
(1)上述四种元素的名称分别是A_________ ;B_________ ;C_________ ;D_________ 。
(2)画出A离子、C原子的结构示意图:_________ ,_________ 。
(1)上述四种元素的名称分别是A
(2)画出A离子、C原子的结构示意图:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】 、
、 、
、 、
、 、
、 、
、 为短周期元素,且原子序数依次递增。
为短周期元素,且原子序数依次递增。 、
、 同主族,
同主族, 、
、 同主族。
同主族。 与其他非金属元素化合时易形成共价键,
与其他非金属元素化合时易形成共价键, 与其他非金属元素化合时易形成离子键,且离子
与其他非金属元素化合时易形成离子键,且离子 与
与 的核外电子排布相同。气态分子
的核外电子排布相同。气态分子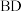 和
和 具有相同的电子数,
具有相同的电子数, 是空气中含量最高的物质。请回答下列问题:
是空气中含量最高的物质。请回答下列问题:
(1) 位于第
位于第______ 周期______ 族;
(2) 的简单离子结构示意图为
的简单离子结构示意图为______ ;
(3) 的电子式是
的电子式是______ ;
(4)由 、
、 、
、 三种元素形成的化合物的化学式为
三种元素形成的化合物的化学式为______ ,含有的化学键类型有______ ,属于______ (填“共价”或“离子”)化合物。
 、
、 、
、 、
、 、
、 、
、 为短周期元素,且原子序数依次递增。
为短周期元素,且原子序数依次递增。 、
、 同主族,
同主族, 、
、 同主族。
同主族。 与其他非金属元素化合时易形成共价键,
与其他非金属元素化合时易形成共价键, 与其他非金属元素化合时易形成离子键,且离子
与其他非金属元素化合时易形成离子键,且离子 与
与 的核外电子排布相同。气态分子
的核外电子排布相同。气态分子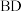 和
和 具有相同的电子数,
具有相同的电子数, 是空气中含量最高的物质。请回答下列问题:
是空气中含量最高的物质。请回答下列问题:(1)
 位于第
位于第(2)
 的简单离子结构示意图为
的简单离子结构示意图为(3)
 的电子式是
的电子式是(4)由
 、
、 、
、 三种元素形成的化合物的化学式为
三种元素形成的化合物的化学式为
您最近一年使用:0次




