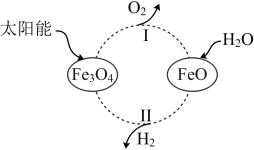
全球能源结构正在向多元、清洁、低碳转型。太阳能的利用是热门研究方向之一,例如,可以利用太阳能将水转化为 ,某种光分解水的过程如图所示,下列说法不正确的是
,某种光分解水的过程如图所示,下列说法不正确的是
 ,某种光分解水的过程如图所示,下列说法不正确的是
,某种光分解水的过程如图所示,下列说法不正确的是
A.该转化发生的总反应为 |
B.该转化过程中循环利用的物质有 |
C.过程Ⅰ中每产生 ,同时产生 ,同时产生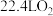 |
D.过程Ⅱ中生成 和 和 的物质的量之比为 的物质的量之比为 |
更新时间:2024-01-30 13:23:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】黄铁矿催化氧化的化学反应为 。设
。设 为阿伏加德罗常数的值,下列有关该反应的说法正确的是
为阿伏加德罗常数的值,下列有关该反应的说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列有关该反应的说法正确的是
为阿伏加德罗常数的值,下列有关该反应的说法正确的是A.36 gH2O中含有中子的数目为 |
B.每生成5.6 g  转移电子的数目为 转移电子的数目为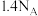 |
C.11.2 L H2中含有非极性键的数目为 |
D.500 mL 0.1 mol⋅L  溶液中含有 溶液中含有 数目为 数目为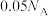 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是
①摩尔是国际单位制中七个基本物理量之一 ②1mol气体体积约为22.4L,则该气体不一定处于标准状况 ③在标准状况下,1mol任何气体体积约为22.4L ④氢离子的摩尔质量是1g/mol ⑤HCl的摩尔质量在数值上等于1molHCl分子的质量 ⑥1molCO2中含有1mol碳和2mol氧
①摩尔是国际单位制中七个基本物理量之一 ②1mol气体体积约为22.4L,则该气体不一定处于标准状况 ③在标准状况下,1mol任何气体体积约为22.4L ④氢离子的摩尔质量是1g/mol ⑤HCl的摩尔质量在数值上等于1molHCl分子的质量 ⑥1molCO2中含有1mol碳和2mol氧
| A.①②③ | B.①②③④ | C.②③④⑤ | D.②④⑤⑥ |
您最近一年使用:0次
【推荐1】汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75 mol,则下列判断不正确的是
| A.生成44.8 L N2 | B.有0.25 mol KNO3被还原 |
| C.转移电子的物质的量为1.25 mol | D.被氧化的N原子的物质的量为3.75 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应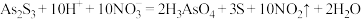 ,下列说法正确的是
,下列说法正确的是
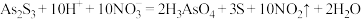 ,下列说法正确的是
,下列说法正确的是A. 为氧化剂,失去电子 为氧化剂,失去电子 |
B.每生成 ,同时生成 ,同时生成 |
C.还原产物与氧化产物的总物质的量之比为 |
D.每生成 ,该反应转移电子的物质的量为 ,该反应转移电子的物质的量为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】肼 常用作火箭燃料,燃烧
常用作火箭燃料,燃烧 肼生成液态水时放出
肼生成液态水时放出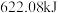 热量,可由
热量,可由 与
与 反应制备;下列变化的方程式表示正确的是
反应制备;下列变化的方程式表示正确的是
 常用作火箭燃料,燃烧
常用作火箭燃料,燃烧 肼生成液态水时放出
肼生成液态水时放出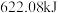 热量,可由
热量,可由 与
与 反应制备;下列变化的方程式表示正确的是
反应制备;下列变化的方程式表示正确的是A.次氯酸在水中的电离: |
B. 与 与 反应制备肼: 反应制备肼: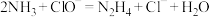 |
C.肼的燃烧: |
D. 与 与 的水溶液反应制备硒: 的水溶液反应制备硒: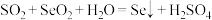 |
您最近一年使用:0次
【推荐2】已知二氧化硒是一种氧化剂,它可有Se+2H2SO4(浓)═2SO2↑+SeO2+2H2O制取,又知离子方程式aSeO2+bSO2+cH2O═aSe+bX+dY;则关于下列叙述正确的是( )
| A.a:b=1:1 |
| B.Y为OH- |
| C.氧化性为:SeO2>H2SO4(浓) |
| D.若每生成0.2 mol X,则该反应转移0.4NA个电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】能正确表示下列反应离子方程式的是
A.向FeSO4溶液中加入NH4HCO3溶液,得到FeCO3沉淀:Fe2++2HCO =FeCO3↓+CO2↑+H2O =FeCO3↓+CO2↑+H2O |
B.向NaHSO4溶液中加入过量Ba(OH)2溶液,得到白色沉淀:2H++SO +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
| C.将nmolCl2通入含有nmolFeBr2的溶液中:2Br-+Cl2=Br2+2Cl- |
D.在强碱溶液中次氯酸钠与氢氧化铁反应生成Na2FeO4:3ClO-+Fe(OH)3=FeO +3Cl-+H2O+H+ +3Cl-+H2O+H+ |
您最近一年使用:0次

 HCl+HClO说法正确的是
HCl+HClO说法正确的是

