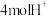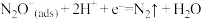室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将银和 溶液与铜和 溶液与铜和 溶液组成原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 溶液组成原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 | Cu的金属性比Ag强 |
| B | 向盛有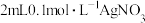 溶液的试管中滴加 溶液的试管中滴加 溶液,再向其中滴加4~5滴 溶液,再向其中滴加4~5滴 溶液。先有白色沉淀生成,后又产生黄色沉淀 溶液。先有白色沉淀生成,后又产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 用铂(Pt)电极电解等浓度的 和 和 的混合溶液,阴极有红色固体物质析出 的混合溶液,阴极有红色固体物质析出 | 氧化性:Cu2+>Fe3+ |
| D | 等体积、pH均为3的HA和HB两种酸,分别与足量的锌反应并收集气体,HA放出的氢气多且反应速率快 | HA酸性比HB强 |
| A.A | B.B | C.C | D.D |
更新时间:2024-01-28 14:04:31
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列四个图象的有关描述错误的是
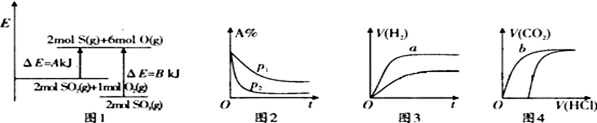
注:ΔE:表示能量,p表示压强;t表示时间,V表示体积,%表示体积百分含量。

注:ΔE:表示能量,p表示压强;t表示时间,V表示体积,%表示体积百分含量。
A.图1表示反应2SO2(g)+O2(g) 2SO3(g)的能量变化,该反应的ΔH=(A-B)kJ/mol 2SO3(g)的能量变化,该反应的ΔH=(A-B)kJ/mol |
B.图2表示其他条件不变时,反应2A(g)+B(g)  C(g)+D(g)在不同压强下随时间的变化 C(g)+D(g)在不同压强下随时间的变化 |
| C.图3表示体积和浓度均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
| D.图4表示100 mL 0.1mol· L-1 Na2CO3和NaHCO3两种溶液中,分别逐滴滴加0.1mol· L-1 HCl,产生CO2的体积随盐酸体积的变化,则b表示NaHCO3溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】pH=2的X、Y、Z三种酸的溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法中正确的是


| A.X是强酸,Y和Z是弱酸 |
| B.稀释前的浓度大小为c(Y)>c(Z)>c(X) |
| C.稀释前电离程度大小为X>Z>Y |
| D.pH=2时,X、Y、Z都是稀溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】利用下列装置进行实验,能达到实验目的的是
| 选项 | A | B |
| 目的 | 制备并收集氨气 | 实验室制备乙酸乙酯 |
| 实验装置 | 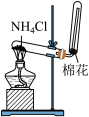 |  |
| 选项 | C | D |
| 目的 | 验证非金属性:S>C>Si | 证明在相同温度下Ksp: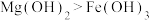 |
| 实验装置 | 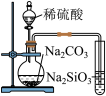 | 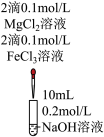 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知:常温下Ka1(H2SO3)=1.4×10-2,Ka2(H2SO3)=6.0×10-8,通过下列实验探究含硫化合物的性质。
实验1:测得0.1mol·L-1H2SO3溶液pH=2.1。
实验2:向10mL0.1mol·L-1NaHSO3溶液中逐滴加入5mL水,用pH计监测过程中pH变化。
实验3:用0.1mol·L-1NaOH溶液滴定10mL0.1mol·L-1H2SO3溶液。
实验4:向10mL0.1mol·L-1Na2S溶液中加入10mL0.1mol·L-1MnSO4溶液,充分混合,产生粉色沉淀,再加几滴0.1mol·L-1CuSO4溶液,产生黑色沉淀。
下列说法不正确的是
实验1:测得0.1mol·L-1H2SO3溶液pH=2.1。
实验2:向10mL0.1mol·L-1NaHSO3溶液中逐滴加入5mL水,用pH计监测过程中pH变化。
实验3:用0.1mol·L-1NaOH溶液滴定10mL0.1mol·L-1H2SO3溶液。
实验4:向10mL0.1mol·L-1Na2S溶液中加入10mL0.1mol·L-1MnSO4溶液,充分混合,产生粉色沉淀,再加几滴0.1mol·L-1CuSO4溶液,产生黑色沉淀。
下列说法不正确的是
A.由实验1可知:0.1mol·L-1H2SO3溶液中c( )<c(OH-) )<c(OH-) |
| B.实验2加水过程中,监测结果为溶液的pH不断增大 |
| C.因实验3可出现两次突跃,指示剂应选用甲基橙和酚酞 |
| D.由实验4可知:Ksp(MnS)>Ksp(CuS) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】下列说法不正确的是
| A.常温下,0.1 mol·L-1CH3COONa溶液的pH=8,则该溶液中 c(CH3COOH)=(10-6-10-8)mol·L—1 |
| B.对于相同浓度的弱酸HX和HY(前者的Ka较大)溶液,加水稀释相同倍数时,HY溶液的pH改变值大于HX溶液的pH改变值 |
C.硫酸钡固体在水中存在以下平衡BaSO4(s) Ba2+(aq)+SO42-(aq),当加入饱和碳酸钠溶液时可以生成BaCO3沉淀 Ba2+(aq)+SO42-(aq),当加入饱和碳酸钠溶液时可以生成BaCO3沉淀 |
D.常温下,a mol·L-1的CH3COOH溶液与0.01mol·L-1NaOH溶液等体积混合后溶液呈中性,此温度下醋酸的电离平衡常数Ka=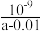 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】一种三室微生物燃料电池污水净化系统的原理如图所示,图中含酚废水中的有机物可用C6H5OH表示。下列说法不正确的是
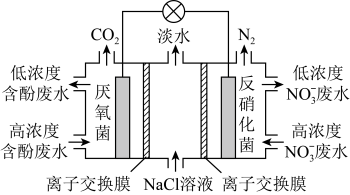

| A.左侧离子交换膜为阳离子交换膜 |
| B.左侧电极为负极,苯酚发生氧化反应 |
C.右侧电极的电极反应式:2 +10e-+6H2O=N2+12OH- +10e-+6H2O=N2+12OH- |
| D.左侧电极附近溶液的pH会逐渐减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】催化剂TAPP - Mn( II )的应用,使Li - CO2电池的研究取得了新的进展。Li-CO2 电池结构和该催化剂作用下正极反应可能的历程如图所示。下列说法错误的是
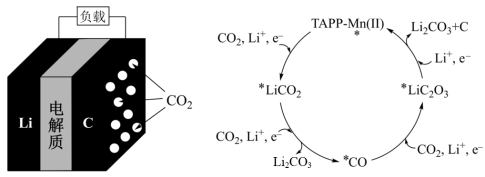

| A.Li- CO2电池可使用有机电解液 |
| B.充电时,Li+由正极向负极迁移 |
| C.放电时,电池总反应为3CO2 +4Li= 2Li2CO3 +C |
| D.该正极反应历程中有4种中间产物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】电化学装置能够实现化学能与电能的相互转化。利用下列装置(电极均为惰性电极),实现电解饱和食盐水,下列说法正确的是
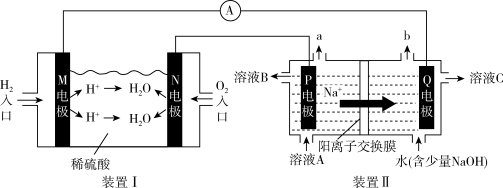

| A.导线中电子的流动方向:M→Q,N→P |
B.N电极的电极反应: |
| C.气体a能使湿润的淀粉碘化钾试纸变蓝 |
| D.溶液A为饱和食盐水,溶液C为稀食盐水 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】我国科学家开发了如图所示的电化学装置,实现了 的制备和废弃PET的回收利用。下列说法错误的是
的制备和废弃PET的回收利用。下列说法错误的是
 的制备和废弃PET的回收利用。下列说法错误的是
的制备和废弃PET的回收利用。下列说法错误的是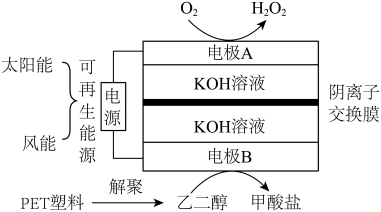
A.溶液中 移向电极B 移向电极B |
| B.电极B的电势高于电极A的电势 |
C.阳极区发生的反应为: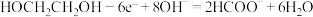 |
D.理论上每消耗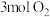 ,电极B消耗乙二醇 ,电极B消耗乙二醇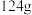 |
您最近一年使用:0次

 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是 ,可表示为
,可表示为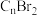 )为正极、盐一水“齐聚物”为电解质溶液的双离子电池如图所示。下列有关该电池的说法不正确的
)为正极、盐一水“齐聚物”为电解质溶液的双离子电池如图所示。下列有关该电池的说法不正确的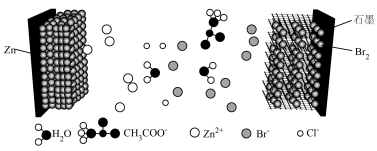

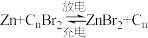
 被还原,
被还原, 在石墨烯纤维无纺布电极侧沉积,
在石墨烯纤维无纺布电极侧沉积, 被氧化后在阴极嵌入
被氧化后在阴极嵌入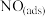 中间体还原为N2的一种反应历程如图(ads指吸附),下列说法错误的是
中间体还原为N2的一种反应历程如图(ads指吸附),下列说法错误的是