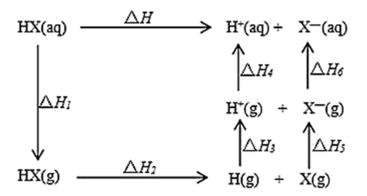
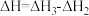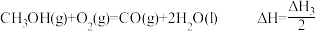已知热化学反应方程式:
①

②

下列说法正确的是
①


②


下列说法正确的是
A.反应①: | B.CO的燃烧热是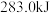 |
C.C生成 需要吸收热量 需要吸收热量 | D.盖斯定律可间接获得不方便测量的反应热 |
更新时间:2024-02-14 19:03:40
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知:① CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=a kJ·mol-1
② C(s)+O2(g)=CO2(g) ΔH2=b kJ·mol-1
③ 2H2O(l)=2H2(g)+O2(g) ΔH3=c kJ·mol-1
④ 2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH4=d kJ·mol-1 下列说法正确的是
② C(s)+O2(g)=CO2(g) ΔH2=b kJ·mol-1
③ 2H2O(l)=2H2(g)+O2(g) ΔH3=c kJ·mol-1
④ 2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH4=d kJ·mol-1 下列说法正确的是
| A.使用催化剂,ΔH1减小 | B.b>0 |
C.H2(g)+ O2(g)=H2O(l) ΔH= O2(g)=H2O(l) ΔH=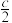 kJ·mol-1 kJ·mol-1 | D.d=2b-c-a |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+ O2(g)=SO2(g)+H2O(g) △H1
O2(g)=SO2(g)+H2O(g) △H1
②2H2S(g)+SO2(g)= S2(g)+2H2O(g) △H2
S2(g)+2H2O(g) △H2
③H2S(g)+ O2(g)=S(g)+H2O(g) △H3
O2(g)=S(g)+H2O(g) △H3
④2S(g) =S2(g) △H4
则△H4的正确表达式为( )
①H2S(g)+
 O2(g)=SO2(g)+H2O(g) △H1
O2(g)=SO2(g)+H2O(g) △H1②2H2S(g)+SO2(g)=
 S2(g)+2H2O(g) △H2
S2(g)+2H2O(g) △H2③H2S(g)+
 O2(g)=S(g)+H2O(g) △H3
O2(g)=S(g)+H2O(g) △H3④2S(g) =S2(g) △H4
则△H4的正确表达式为( )
| A.△H4=2/3(△H1+△H2-3△H3) |
| B.△H4=2/3(3△H3-△H1-△H2) |
| C.△H4=3/2(△H1+△H2-3△H3) |
| D.△H4=3/2(△H1-△H2-3△H3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列对热化学方程式的解读或书写正确的是
A.已知  ,则石墨比金刚石稳定 ,则石墨比金刚石稳定 |
B.已知①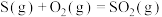  ;② ;②  ,则 ,则 |
C.已知甲烷燃烧热为 ,则甲烷燃烧的热化学方程式可以表示为 ,则甲烷燃烧的热化学方程式可以表示为 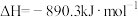 |
D.已知中和热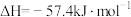 ,则1mol硫酸和足量稀NaOH溶液反应的反应热就是中和热 ,则1mol硫酸和足量稀NaOH溶液反应的反应热就是中和热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于热化学方程式的叙述正确的是( )
| A.2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ·mol-1,则H2的燃烧热为241.8kJ·mol-1 |
B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6kJ·mol-1 2NH3(g)△H=-38.6kJ·mol-1 |
| C.S(g)+O2(g)=SO2(g)△H1:S(s)+O2(g)=SO2(g)△H2,则△H1<△H2 |
| D.在稀溶液中:H+(aq)+OH-(ag)=H2O(l)△H=-57.3kJ·mol-1,若将0.5mol/L的稀H2SO4与1mol/L的NaOH的溶液等体积混合,放出的热量等于57.3kJ |
您最近一年使用:0次
【推荐1】氢气作为清洁高效、可持续“零碳”能源被广泛研究,水煤气变换反应(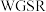 )的氧化还原机理和羧基机理如图所示。对
)的氧化还原机理和羧基机理如图所示。对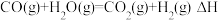 的热化学方程式的表述
的热化学方程式的表述不正确 的是
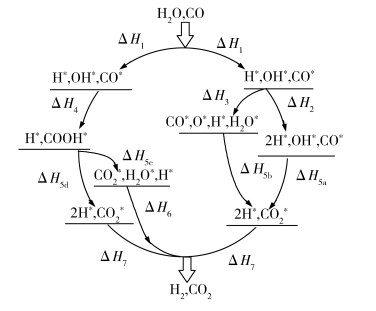
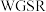 )的氧化还原机理和羧基机理如图所示。对
)的氧化还原机理和羧基机理如图所示。对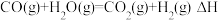 的热化学方程式的表述
的热化学方程式的表述
A.氧化还原机理途径: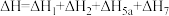 |
B.羧基机理途径: |
| C.两种机理途径都存在氢氧键断裂和氢氧键的形成 |
D.加入催化剂能改变机理途径,同时影响 的值 的值 |
您最近一年使用:0次
【推荐2】已知NaHCO3溶液与盐酸反应生成CO2吸热,Na2CO3溶液与盐酸反应生成CO2 放热。关于下列ΔH的判断正确的是
CO (aq)+H+(aq)
(aq)+H+(aq) HCO
HCO (aq) ΔH1
(aq) ΔH1
HCO (aq)+H+(aq)
(aq)+H+(aq)  H2CO3(aq) ΔH2
H2CO3(aq) ΔH2
H2CO3(aq) H2O(l)+CO2(g) ΔH3
H2O(l)+CO2(g) ΔH3
OH-(aq)+H+(aq) H2O(l) ΔH4
H2O(l) ΔH4
CO
 (aq)+H+(aq)
(aq)+H+(aq) HCO
HCO (aq) ΔH1
(aq) ΔH1HCO
 (aq)+H+(aq)
(aq)+H+(aq)  H2CO3(aq) ΔH2
H2CO3(aq) ΔH2H2CO3(aq)
 H2O(l)+CO2(g) ΔH3
H2O(l)+CO2(g) ΔH3OH-(aq)+H+(aq)
 H2O(l) ΔH4
H2O(l) ΔH4| A.ΔH1<0 ΔH2>0 | B.ΔH1+ΔH2>0 |
| C.ΔH1+ΔH2+ΔH3>0 | D.ΔH2<ΔH4 |
您最近一年使用:0次


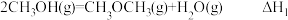
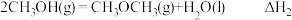
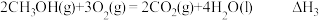
 的燃烧热为
的燃烧热为

 的燃烧热
的燃烧热