乙酰水杨酸(阿司匹林)是目前常用药物之一,实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
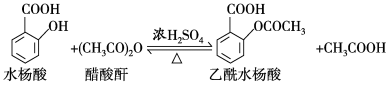
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作:
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
(2)①中需使用冷水,目的是___________ 。
(3)②中饱和碳酸氢钠的作用是___________ ,以便过滤除去难溶杂质。
(4)④采用的纯化方法为___________ 。
(5)本实验的产率是___________ %。

| 水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
| 熔点/℃ | 157~159 | -72~-74 | 135~138 |
| 相对密度/(g·cm-3) | 1.44 | 1.10 | 1.35 |
| 相对分子质量 | 138 | 102 | 180 |
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
| A.热水浴 | B.酒精灯 | C.煤气灯 | D.电炉 |
(3)②中饱和碳酸氢钠的作用是
(4)④采用的纯化方法为
(5)本实验的产率是
2024高三下·全国·专题练习 查看更多[1]
(已下线)题型三 以分离提纯为主的有机制备类实验-备战2024年高考化学答题技巧与模板构建
更新时间:2024-03-01 10:46:55
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学取刚降落在热电厂附近的雨水进行实验。
① 测得该雨水样品的pH为4.73;② 向雨水样品中滴加BaCl2溶液,有白色沉淀生成;③ 每隔1 h,通过pH计测定雨水样品的pH,测得的结果如下表:
根据以上信息,回答下列问题:
(1)正常雨水的pH为5.6,偏酸性,这是因为_________________________________ 。
(2)分析上述数据变化,你认为形成这一变化的原因是_____________________ 。
(3)兴趣小组同学取某一时段的这种雨水VL,加入0.5mol·L-1的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液。请计算(列出计算过程):
① 该V L雨水中溶解SO2的体积(标准状况)为______________ mL。
计算过程:
② 生成沉淀物的质量范围为________________________ 。
① 测得该雨水样品的pH为4.73;② 向雨水样品中滴加BaCl2溶液,有白色沉淀生成;③ 每隔1 h,通过pH计测定雨水样品的pH,测得的结果如下表:
测定时间/h | 0 | 1 | 2 | 3 | 4 |
雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
根据以上信息,回答下列问题:
(1)正常雨水的pH为5.6,偏酸性,这是因为
(2)分析上述数据变化,你认为形成这一变化的原因是
(3)兴趣小组同学取某一时段的这种雨水VL,加入0.5mol·L-1的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液。请计算(列出计算过程):
① 该V L雨水中溶解SO2的体积(标准状况)为
计算过程:
② 生成沉淀物的质量范围为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾[KAl(SO4)2•12H2O]相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:

根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.00g氨)需要取浓氨水(每升含有250g氨)__________ mL,用规格为_______ mL量筒量取。
(2)写出溶解步骤中反应得到的溶液的溶质为_______ (写化学式)
(3)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量______ 溶液,产生白色沉淀。
②_______ 、______ 、________ (填实验操作名称)。
③冷却、称重。
(4)若试样为m g,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:______ (用含有m、n的代数式表示)。

根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.00g氨)需要取浓氨水(每升含有250g氨)
(2)写出溶解步骤中反应得到的溶液的溶质为
(3)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量
②
③冷却、称重。
(4)若试样为m g,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】回答下列问题:
(1)20 g A物质和14 g B物质恰好完全反应,生成8.8 g C物质、3.6 g D物质和0.2 mol E物质,则E的摩尔质量为___ 。
(2)化合物A的分子组成可用NxHy表示,在一定条件下可发生分解反应,15 ml A气体完全分解生成5 mL N2和20 mLNH3(同温同压),则A的化学式为___ 。
(3)标准状况下,11.2 LCO和CO2混合气体的质量为20.4 g,求混合气体中CO和CO2的体积比、质量比分别为___ ;___ 。
(1)20 g A物质和14 g B物质恰好完全反应,生成8.8 g C物质、3.6 g D物质和0.2 mol E物质,则E的摩尔质量为
(2)化合物A的分子组成可用NxHy表示,在一定条件下可发生分解反应,15 ml A气体完全分解生成5 mL N2和20 mLNH3(同温同压),则A的化学式为
(3)标准状况下,11.2 LCO和CO2混合气体的质量为20.4 g,求混合气体中CO和CO2的体积比、质量比分别为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等功效。苹果酸是这种饮品的主要酸性物质。苹果酸是一种常见的有机酸,其结构简式为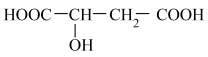 。
。
(1)苹果酸中含有的官能团的名称是___________ 、___________ 。
(2)苹果酸的分子式为___________ 。
(3)1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气___________ L。
(4)苹果酸可能发生的反应是___________ 。
A.与酚酞溶液作用显红色 B.与NaOH溶液反应
C.与乙酸在一定条件下酯化 D.与H2在一定条件下加成
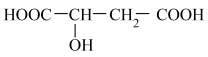 。
。(1)苹果酸中含有的官能团的名称是
(2)苹果酸的分子式为
(3)1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气
(4)苹果酸可能发生的反应是
A.与酚酞溶液作用显红色 B.与NaOH溶液反应
C.与乙酸在一定条件下酯化 D.与H2在一定条件下加成
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】扑热息痛F是一种解热镇痛类药物。由A制备F的一种合成路线如下:
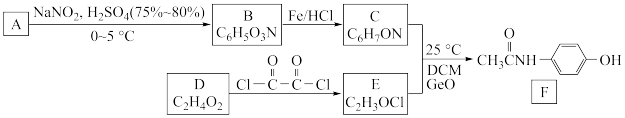
已知:①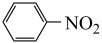

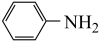
②苯环上原有的取代基对苯环上再导入取代基的位置有一定的影响。如-OH、-Cl等使新导入的取代基进入苯环的邻、对位;-NO2等使新导入的取代基进入苯环的间位。
(1)A的化学名称是__________ 。
(2)由D生成E的反应类型是__________ 。
(3)B的结构简式为____________ 。
(4)C与E反应生成F的化学方程式为___________ 。
(5)关于有毒物质 的下列说法正确的是
的下列说法正确的是___________ (填标号)。
a.遇水水解生成两种酸
b.该物质含有的官能团是氯原子和酯基
c.废弃的该物质常用焚烧法处理,焚烧后可直接排放
(6)芳香化合物X是F的同分异构体,既有酸性又有碱性,并能与碳酸氢钠溶液反应放出CO2,X共有____ 种(不考虑立体异构),其中属于天然蛋白质水解产物的结构简式____________ 。
(7)写出以苯为原料制备化合物B的合成路线________ (其他试剂任选)。
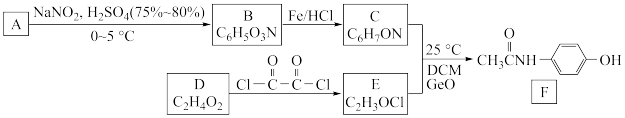
已知:①


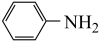
②苯环上原有的取代基对苯环上再导入取代基的位置有一定的影响。如-OH、-Cl等使新导入的取代基进入苯环的邻、对位;-NO2等使新导入的取代基进入苯环的间位。
(1)A的化学名称是
(2)由D生成E的反应类型是
(3)B的结构简式为
(4)C与E反应生成F的化学方程式为
(5)关于有毒物质
 的下列说法正确的是
的下列说法正确的是a.遇水水解生成两种酸
b.该物质含有的官能团是氯原子和酯基
c.废弃的该物质常用焚烧法处理,焚烧后可直接排放
(6)芳香化合物X是F的同分异构体,既有酸性又有碱性,并能与碳酸氢钠溶液反应放出CO2,X共有
(7)写出以苯为原料制备化合物B的合成路线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】苯甲醛在碱性条件下可发生反应: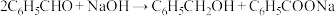 。相关物质的物理性质如下表:
。相关物质的物理性质如下表:
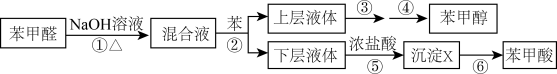
制备苯甲醇和苯甲酸的实验流程及主要实验装置(部分加热和固定装置已略)如下:______ 。仪器B的作用是______ 。
(2)第②步所用玻璃仪器有烧杯、______ 。
(3)第③步采用沸水浴加热蒸馏,收集到的馏分为______ ;再进行第④步,操作如图2所示。图2中有一处明显错误,正确的应改为______ 。
(4)第⑤步反应的离子方程式为______ ;冷水洗涤沉淀X的优点是______ ;检验沉淀X洗涤干净与否的操作:______ 。
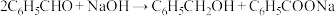 。相关物质的物理性质如下表:
。相关物质的物理性质如下表:苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |||
溶解性 | 水中 | 微溶 | 微溶 | 温度 | 溶解度 | 不溶 |
17℃ | 0.21g | |||||
25℃ | 0.34g | |||||
100℃ | 5.9g | |||||
有机溶剂中 | 易溶 | 易溶 | 易溶 | 易溶 | ||
密度(20℃)/ | 1.0 | 1.0 | 1.3 | 0.9 | ||
沸点/℃ | 178 | 205 | 249 | 80 | ||
熔点/℃ | 26 | ―15 | 122 | 5.4 | ||

(2)第②步所用玻璃仪器有烧杯、
(3)第③步采用沸水浴加热蒸馏,收集到的馏分为
(4)第⑤步反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸镁可用于印染、造纸、医药工业。利用某水泥厂的废料(含
 ,还有少量CaO、MnO2、
,还有少量CaO、MnO2、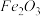 、FeO、
、FeO、 、
、 等杂质),制取
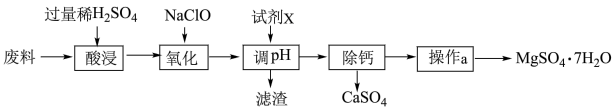
等杂质),制取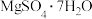 的流程如下:
的流程如下:
已知部分氢氧化物开始沉淀和完全沉淀时的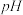 值如下表所示:
值如下表所示:
回答下列问题:
(1)氧化时,“酸浸”时,pH控制为1,若提高浸取速率,可采取的措施是_______ (任写一条)。
(2) 与
与 按物质的量1∶1反应生成MnO2,其离子方程式为
按物质的量1∶1反应生成MnO2,其离子方程式为_______ ;调节pH时可加入试剂X为_______ (任写一种),调节pH的范围为_______ 。
(3)滤渣除 、
、 外还有氧化物
外还有氧化物_______ 。
(4)在“除钙”前,需检验滤液中 是否被除尽,简述检验方法
是否被除尽,简述检验方法_______ 。(写出操作、现象和结论)
(5)操作a是将滤液_______ 、_______ 、过滤、洗涤、干燥便得到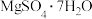 晶体。
晶体。
(6)处理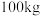 废料,最终得到
废料,最终得到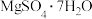 为
为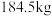 ,则
,则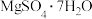 的产率为
的产率为_______ 。[产率 (实际产量
(实际产量 理论产量)
理论产量) ]
]

 ,还有少量CaO、MnO2、
,还有少量CaO、MnO2、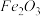 、FeO、
、FeO、 、
、 等杂质),制取
等杂质),制取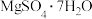 的流程如下:
的流程如下:
已知部分氢氧化物开始沉淀和完全沉淀时的
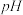 值如下表所示:
值如下表所示:| 沉淀物 | 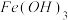 |  |  |  |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 | 8.4 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 | 10.8 |
(1)氧化时,“酸浸”时,pH控制为1,若提高浸取速率,可采取的措施是
(2)
 与
与 按物质的量1∶1反应生成MnO2,其离子方程式为
按物质的量1∶1反应生成MnO2,其离子方程式为(3)滤渣除
 、
、 外还有氧化物
外还有氧化物(4)在“除钙”前,需检验滤液中
 是否被除尽,简述检验方法
是否被除尽,简述检验方法(5)操作a是将滤液
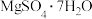 晶体。
晶体。(6)处理
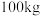 废料,最终得到
废料,最终得到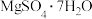 为
为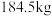 ,则
,则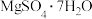 的产率为
的产率为 (实际产量
(实际产量 理论产量)
理论产量) ]
]
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
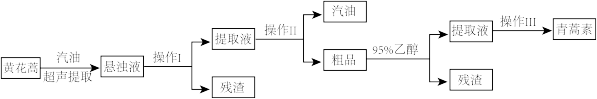
【推荐2】I.2016年美国Cell杂志发表了一项有关青蒿素具有降血糖活性的研究。从黄花蒿中提取青蒿素的方法以萃取原理为基础,采用汽油浸提法,具体操作如下:
已知:①青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水。
②青蒿素在95%乙醇中的溶解度随温度升高显著升高:乙醇的沸点为78℃。
③青蒿素热稳定性差,温度超过60℃,青蒿素的药效明显降低。
(1)超声提取是在强大的超声波作用下,使黄花蒿细胞乳化、击碎、扩散,采用超声提取的优点是_______ 。
(2)操作II中,温度计放置的位置是_______ 。
(3)操作II制备的粗品用95%乙醇溶解过滤的目的是_______ ;操作Ⅲ的具体步骤为:_______ 、_______ 、过滤、洗涤、干燥,在该操作过程中加热温度应不超过_______ ℃。
II.
(4)海带中富含碘元素,会加重合并甲状腺功能亢进的糖尿病患者的病情。小附同学在实验室中欲从碘水中提取碘,所需要的玻璃仪器有_______ ;若用 萃取,则振荡静置后的现象是
萃取,则振荡静置后的现象是_______ 。

已知:①青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水。
②青蒿素在95%乙醇中的溶解度随温度升高显著升高:乙醇的沸点为78℃。
③青蒿素热稳定性差,温度超过60℃,青蒿素的药效明显降低。
(1)超声提取是在强大的超声波作用下,使黄花蒿细胞乳化、击碎、扩散,采用超声提取的优点是
(2)操作II中,温度计放置的位置是
(3)操作II制备的粗品用95%乙醇溶解过滤的目的是
II.
(4)海带中富含碘元素,会加重合并甲状腺功能亢进的糖尿病患者的病情。小附同学在实验室中欲从碘水中提取碘,所需要的玻璃仪器有
 萃取,则振荡静置后的现象是
萃取,则振荡静置后的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】工业上以铬铁矿,主要成分为FeCr2O4,(含Al、Si氧化物等杂质)为主要原料制备红矾钠(Na2Cr2O7•2H2O)的工艺流程如图。(已知:FeCr2O4,中铬元素为+3价: 与
与 存在如下平衡:
存在如下平衡: 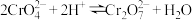 ),回答下列问题:
),回答下列问题:

(1)铬铁矿预先粉碎的目的是_____
(2)焙烧过程中,FeCr2O4转化为Na2CrO4,并产生红棕色固体物质和无色气体,写出该过程的化学方程式_____
(3)常温下,矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度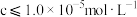 时,可认为基本已除尽。
时,可认为基本已除尽。
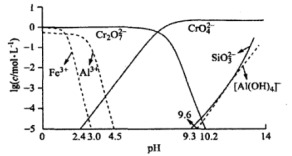
Fe元素在___________ (填操作单元的名称)过程中除去,中和时pH的理论范围为___________ 酸化的目的是_____ ;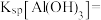
___________ 。
(4)利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2CrO7的总反应方程式为: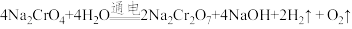 。则Na2CrO7在
。则Na2CrO7在___________ (填“阴”或“阳”)极室制得,电解时通过交换膜的离子主要为___________ 。

 与
与 存在如下平衡:
存在如下平衡: 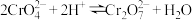 ),回答下列问题:
),回答下列问题:
(1)铬铁矿预先粉碎的目的是
(2)焙烧过程中,FeCr2O4转化为Na2CrO4,并产生红棕色固体物质和无色气体,写出该过程的化学方程式
(3)常温下,矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度
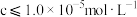 时,可认为基本已除尽。
时,可认为基本已除尽。
Fe元素在
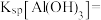
(4)利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2CrO7的总反应方程式为:
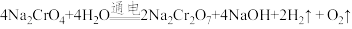 。则Na2CrO7在
。则Na2CrO7在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等。实验室合成苯甲酸的原理及有关数据及装置示意图如下:
反应过程: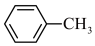
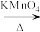


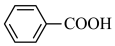
已知:(1)苯甲酸 100 ℃左右开始升华。
(2)反应试剂、产物的物理常数如下:
按下列合成步骤回答问题:
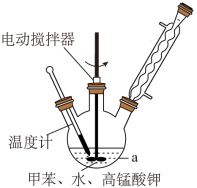
步骤Ⅰ:按图在 250 mL 仪器 a 中放入 2.7 mL 甲苯和 100 mL 水,控制温度为 100℃,搅拌溶液,在石棉网上加热至沸腾。从冷凝管上口分批加入 8.5 g 高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约 4~5h,反应完全后,停止加热。
步骤 Ⅱ:在反应结束后混合物中加入一定量亚硫酸氢钠溶液,产生黑色沉淀,趁热过滤、热水洗涤沉淀,合并滤液与洗涤液,再将其放在冰水浴中冷却,然后用浓盐酸酸化至苯甲酸全部析出;将析出的苯甲酸减压过滤,再用少量冷水洗涤苯甲酸固体,挤压除去水分,将制得的苯甲酸固体放在沸水浴上干燥,得到粗产品。
(1)仪器 a 的名称_______ 。
(2)步骤Ⅰ中反应完全的现象为_______ 。
(3)步骤 Ⅱ在反应混合物中加入一定量亚硫酸氢钠溶液,亚硫酸氢钠溶液的作用是_______ ;还可以用_______ (填选项)代替亚硫酸氢钠溶液。
A.H2O2 B.NaHCO3 C. Na2C2O4
(4)步骤 Ⅱ中干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______ 。
(5)若将苯甲酸粗产品进一步提纯,可用_______ 方法,最终得到2.0g产品,则苯甲酸产率为_______ 。
反应过程:

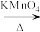


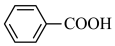
已知:(1)苯甲酸 100 ℃左右开始升华。
(2)反应试剂、产物的物理常数如下:
| 名称 | 性状 | 熔点 | 沸点/C | 密度/g·mL-1 | 溶解度/g(室温) | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体、易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 |

步骤Ⅰ:按图在 250 mL 仪器 a 中放入 2.7 mL 甲苯和 100 mL 水,控制温度为 100℃,搅拌溶液,在石棉网上加热至沸腾。从冷凝管上口分批加入 8.5 g 高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约 4~5h,反应完全后,停止加热。
步骤 Ⅱ:在反应结束后混合物中加入一定量亚硫酸氢钠溶液,产生黑色沉淀,趁热过滤、热水洗涤沉淀,合并滤液与洗涤液,再将其放在冰水浴中冷却,然后用浓盐酸酸化至苯甲酸全部析出;将析出的苯甲酸减压过滤,再用少量冷水洗涤苯甲酸固体,挤压除去水分,将制得的苯甲酸固体放在沸水浴上干燥,得到粗产品。
(1)仪器 a 的名称
(2)步骤Ⅰ中反应完全的现象为
(3)步骤 Ⅱ在反应混合物中加入一定量亚硫酸氢钠溶液,亚硫酸氢钠溶液的作用是
A.H2O2 B.NaHCO3 C. Na2C2O4
(4)步骤 Ⅱ中干燥苯甲酸晶体时,若温度过高,可能出现的结果是
(5)若将苯甲酸粗产品进一步提纯,可用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用乳酸与异戊醇反应制备乳酸异戊酯,有关数据和装置示意图如下:

实验步骤:
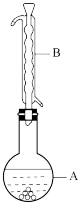
①如图连接好装置,在A中加入9g乳酸和17.6g异戊醇、数滴浓硫酸和2~3片碎瓷片开始缓慢加热A。
②回流1h,反应液冷却至室温后,倒入分液漏斗中,先水洗,再用饱和碳酸钠溶液洗涤至中性,最后用饱和食盐水和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻。
③过滤除去硫酸镁固体,进行蒸馏纯化,收集200~203℃馏分,得乳酸异戊酯13.6g。
回答下列问题:
(1)图中A仪器的名称是_______ ,B仪器的作用是_______ 。
(2)在该实验中,A的容积最适合的是_______ (填入正确选项前的字母)。
A.150mL B.100mL C.50mL
(3)分离提纯过程中加入无水硫酸镁的目的是_______ 。
(4)在蒸馏纯化过程中,下列说法错误的是_______ 。
A.温度计应该插入液面以下
B.加热一段时间后发现忘记加瓷片,应该冷却后补加
C.冷却水的方向是上进下出,保证冷却水快速流动
D.蒸馏时用到的主要玻璃仪器有:酒精灯、蒸馏烧瓶、冷凝管、温度计、牛角管、锥形瓶
(5)本实验中加入过量异戊醇的目的是_______ ,本实验的产率是_______ 。

| 相对分子质量 | 密度/(g∙cm-3) | 沸点/℃ | 水中溶解度 | |
| 乳酸 | 90 | 1.209 | 122 | 溶 |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乳酸异戊酯 | 160 | 0.96 | 202 | 不溶 |
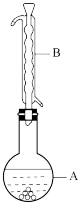
①如图连接好装置,在A中加入9g乳酸和17.6g异戊醇、数滴浓硫酸和2~3片碎瓷片开始缓慢加热A。
②回流1h,反应液冷却至室温后,倒入分液漏斗中,先水洗,再用饱和碳酸钠溶液洗涤至中性,最后用饱和食盐水和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻。
③过滤除去硫酸镁固体,进行蒸馏纯化,收集200~203℃馏分,得乳酸异戊酯13.6g。
回答下列问题:
(1)图中A仪器的名称是
(2)在该实验中,A的容积最适合的是
A.150mL B.100mL C.50mL
(3)分离提纯过程中加入无水硫酸镁的目的是
(4)在蒸馏纯化过程中,下列说法错误的是
A.温度计应该插入液面以下
B.加热一段时间后发现忘记加瓷片,应该冷却后补加
C.冷却水的方向是上进下出,保证冷却水快速流动
D.蒸馏时用到的主要玻璃仪器有:酒精灯、蒸馏烧瓶、冷凝管、温度计、牛角管、锥形瓶
(5)本实验中加入过量异戊醇的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:
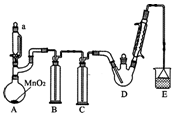
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
(1)仪器A中发生反应的化学方程式为____________ 。
(2)装置B中的试剂是____________ ,若撤去装置B,可能导致装置D中副产物____________ (填化学式)的量增加;装置D可采用____________ 加热的方法以控制反应温度在70℃左右。
(3)装置中球形冷凝管的作用为____________ ,写出E中所有可能发生的无机反应的离子方程式____________ 。
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行____________ 。
(5)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol•L-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O3溶液20.00mL。则产品的纯度为____________ (计算结果保留三位有效数字)。
滴定的反应原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)为证明三氯乙酸的酸性比乙酸强,某学习小组的同学设计了以下三种方案,你认为能够达到实验目的是____________
a.分别测定0.1mol•L-1两种酸溶液的pH,三氯乙酸的pH较小
b.用仪器测量浓度均为0.1mol•L-1的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
c.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)仪器A中发生反应的化学方程式为
(2)装置B中的试剂是
(3)装置中球形冷凝管的作用为
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行
(5)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol•L-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O3溶液20.00mL。则产品的纯度为
滴定的反应原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)为证明三氯乙酸的酸性比乙酸强,某学习小组的同学设计了以下三种方案,你认为能够达到实验目的是
a.分别测定0.1mol•L-1两种酸溶液的pH,三氯乙酸的pH较小
b.用仪器测量浓度均为0.1mol•L-1的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
c.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大
您最近一年使用:0次




