I.2016年美国Cell杂志发表了一项有关青蒿素具有降血糖活性的研究。从黄花蒿中提取青蒿素的方法以萃取原理为基础,采用汽油浸提法,具体操作如下:
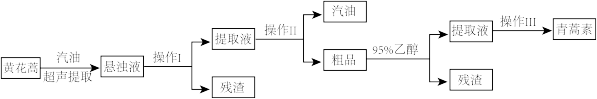
已知:①青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水。
②青蒿素在95%乙醇中的溶解度随温度升高显著升高:乙醇的沸点为78℃。
③青蒿素热稳定性差,温度超过60℃,青蒿素的药效明显降低。
(1)超声提取是在强大的超声波作用下,使黄花蒿细胞乳化、击碎、扩散,采用超声提取的优点是_______ 。
(2)操作II中,温度计放置的位置是_______ 。
(3)操作II制备的粗品用95%乙醇溶解过滤的目的是_______ ;操作Ⅲ的具体步骤为:_______ 、_______ 、过滤、洗涤、干燥,在该操作过程中加热温度应不超过_______ ℃。
II.
(4)海带中富含碘元素,会加重合并甲状腺功能亢进的糖尿病患者的病情。小附同学在实验室中欲从碘水中提取碘,所需要的玻璃仪器有_______ ;若用 萃取,则振荡静置后的现象是
萃取,则振荡静置后的现象是_______ 。

已知:①青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水。
②青蒿素在95%乙醇中的溶解度随温度升高显著升高:乙醇的沸点为78℃。
③青蒿素热稳定性差,温度超过60℃,青蒿素的药效明显降低。
(1)超声提取是在强大的超声波作用下,使黄花蒿细胞乳化、击碎、扩散,采用超声提取的优点是
(2)操作II中,温度计放置的位置是
(3)操作II制备的粗品用95%乙醇溶解过滤的目的是
II.
(4)海带中富含碘元素,会加重合并甲状腺功能亢进的糖尿病患者的病情。小附同学在实验室中欲从碘水中提取碘,所需要的玻璃仪器有
 萃取,则振荡静置后的现象是
萃取,则振荡静置后的现象是
更新时间:2022/11/12 14:00:56
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】CoCO3是一种制造锂电池电极的原料。以含钴废渣(主要成分CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算):
(1)“酸浸”时通入SO2发生反应的离子方程式是___________ 。
(2)“除铝”时调节溶液pH范围为___________ ,该过程中主要反应的离子方程式为___________ 。
(3)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是___________ 。
(4)“沉钴”时为使Co2+沉淀完全,Na2CO3溶液需稍过量且缓慢滴加,能说明Co2+已沉淀完全的实验操作是___________ 。
(5)CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为___________ 。
(6)某工业生产过程中得到溶液的溶质主要是ZnSO4和CuSO4。已知硫酸锌晶体的溶解度随温度变化如图,请设计从该混合液中获取ZnSO4晶体的实验方案:
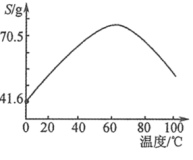
向溶液中加入稍过量的锌粉,充分反应后,___________ ,得到ZnSO4溶液,___________ ,得到ZnSO4晶体。(实验中须使用的试剂有:Zn粉、稀H2SO4、酒精)。

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算):
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Co2+ | 7.6 | 9.4 |
| Al3+ | 3.0 | 5.0 |
| Zn2+ | 5.4 | 8.0 |
(1)“酸浸”时通入SO2发生反应的离子方程式是
(2)“除铝”时调节溶液pH范围为
(3)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层)
 ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是(4)“沉钴”时为使Co2+沉淀完全,Na2CO3溶液需稍过量且缓慢滴加,能说明Co2+已沉淀完全的实验操作是
(5)CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为
(6)某工业生产过程中得到溶液的溶质主要是ZnSO4和CuSO4。已知硫酸锌晶体的溶解度随温度变化如图,请设计从该混合液中获取ZnSO4晶体的实验方案:

向溶液中加入稍过量的锌粉,充分反应后,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硅是最理想的太阳能电池材料,高性能晶硅电池是建立在高质量晶硅材料基础上的。工业上可以用如图所示的流程制取高纯硅。
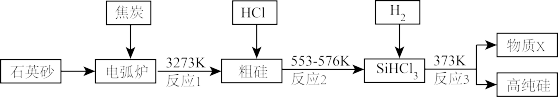
(1)硅在周期表中的位置是_______ ,反应1中氧化剂与还原剂的物质的量之比为:_______ 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3 (沸点31.8℃)中含有少量SiCl4 (沸点57.6℃)和SiH2Cl2 (沸点8.2℃)、SiH3Cl(沸点-30.4℃)提纯SiHCl3采用的方法为_______ ,整个过程中可以循环利用的物质X是:_______ (填化学式)
(3)提纯粗硅的过程中必须严格控制无水无氧,原因之一是硅的卤化物极易水解,写出SiCl4遇水剧烈反应的化学方程式_______
(4)硅在有HNO3存在的条件下,可以与HF生成H2SiF6,同时有不溶于水的气体生成,该气体遇空气变为红棕色,硅单质发生的化学方程式为_______
(5)某工厂用100吨纯度为75%的石英砂为原料经第一步反应制得的粗硅中含硅28吨,则该过程中硅的产率是:_______ (精确到小数点后两位)

(1)硅在周期表中的位置是
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3 (沸点31.8℃)中含有少量SiCl4 (沸点57.6℃)和SiH2Cl2 (沸点8.2℃)、SiH3Cl(沸点-30.4℃)提纯SiHCl3采用的方法为
(3)提纯粗硅的过程中必须严格控制无水无氧,原因之一是硅的卤化物极易水解,写出SiCl4遇水剧烈反应的化学方程式
(4)硅在有HNO3存在的条件下,可以与HF生成H2SiF6,同时有不溶于水的气体生成,该气体遇空气变为红棕色,硅单质发生的化学方程式为
(5)某工厂用100吨纯度为75%的石英砂为原料经第一步反应制得的粗硅中含硅28吨,则该过程中硅的产率是:
您最近一年使用:0次
【推荐3】NaCl溶液中混有 和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下,回答以下问题:
和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下,回答以下问题:

(1)写出上述实验过程中所用试剂(填化学式)和基本实验操作,试剂①_______ ;试剂②_______ ;操作③_______ ,操作④_______ 。
(2)适量试剂③的作用是_______ 。
(3)操作①是利用半透膜进行分离提纯。其原理为_______ 。
(4)简述胶体不同于溶液的最本质特征是_______ 。
(5)图为家用环保型消毒液发生器,玻璃管内是滴有酚酞的饱和食盐水。
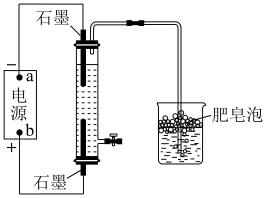
①书写电解饱和食盐水的化学方程式_______ ,肥皂泡中收集的气体主要是_______ 。
②电源a极相连的电极附近溶液的颜色变化为_______ 。
③反应中制得的消毒液含有NaClO成分,书写该装置中总反应的化学方程式:_______ 。
 和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下,回答以下问题:
和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下,回答以下问题:
(1)写出上述实验过程中所用试剂(填化学式)和基本实验操作,试剂①
(2)适量试剂③的作用是
(3)操作①是利用半透膜进行分离提纯。其原理为
(4)简述胶体不同于溶液的最本质特征是
(5)图为家用环保型消毒液发生器,玻璃管内是滴有酚酞的饱和食盐水。

①书写电解饱和食盐水的化学方程式
②电源a极相连的电极附近溶液的颜色变化为
③反应中制得的消毒液含有NaClO成分,书写该装置中总反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答有关问题:

(1)装置A中玻璃仪器①的名称是________ ,进水的方向是从____ 口(填字母)进水。
(2)利用装置B分液时为使液体顺利滴下,应进行的具体操作是_________________ 。
(3)从氯化钾溶液中得到氯化钾固体,应选择装置________ (填字母,下同);从碘水中分离出I2,应选择装置________ 。

(1)装置A中玻璃仪器①的名称是
(2)利用装置B分液时为使液体顺利滴下,应进行的具体操作是
(3)从氯化钾溶液中得到氯化钾固体,应选择装置
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】LFP是一种常见的锂离子电池正极材料,其中含有LiFePO4、炭黑、铝箔。利用废弃LFP正极材料回收金属、选择性提锂的工艺流程如下图所示。
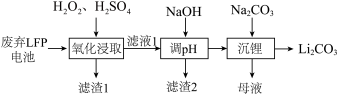
回答下列问题:
(1)Fe位于元素周期表的第___________ 周期___________ 族。
(2)若“滤渣1”中含有炭黑和FePO4,则“氧化浸取”中生成FePO4的离子方程式为___________ 。
(3)“滤渣2”的主要成分是___________ 。
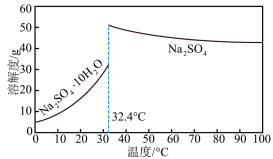
(4) 和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、___________ 、干燥。
(5)利用FePO4和Li2CO3与葡萄糖在氮气氛围中加热能制备LiFePO4和CO,则发生的化学方程式为___________ 。
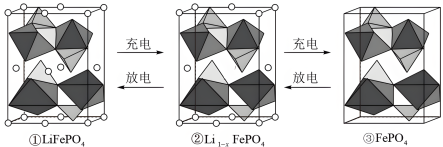
(6)LiFePO4的晶胞结构如图①所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。电池充电时,LiFeO4脱出部分 ,转化为
,转化为 (图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为
(图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为___________ g/cm3,LiFeO4转化 的电极反应式为
的电极反应式为___________ 。

回答下列问题:
(1)Fe位于元素周期表的第
(2)若“滤渣1”中含有炭黑和FePO4,则“氧化浸取”中生成FePO4的离子方程式为
(3)“滤渣2”的主要成分是
(4)
 和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
(5)利用FePO4和Li2CO3与葡萄糖在氮气氛围中加热能制备LiFePO4和CO,则发生的化学方程式为
(6)LiFePO4的晶胞结构如图①所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。电池充电时,LiFeO4脱出部分
 ,转化为
,转化为 (图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为
(图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为 的电极反应式为
的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钠水溶液中的歧化反应制得,反应的化学方程式为
2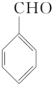 +NaOH
+NaOH
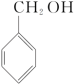 +
+
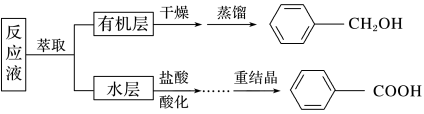
某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
重结晶过程:溶解 活性炭脱色
活性炭脱色 趁热过滤
趁热过滤 冷却结晶
冷却结晶 抽滤
抽滤 洗涤
洗涤 干燥。
干燥。
已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。苯甲酸微溶于水,乙醚难溶于水。
请根据以上信息,回答下列问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是___________ ,其理由是___________ 。萃取分液后,所得水层用盐酸酸化的目的是(请用化学方程式表示)___________ 。
(2)苯甲酸在A、B、C三种溶剂中的溶解度(S)随温度变化的曲线如图所示。重结晶时,合适的溶剂是___________ 。重结晶过程中,趁热过滤的作用是___________ 。洗涤时采用的合适洗涤剂是___________ (填字母)。

A.饱和食盐水 B.Na2CO3溶液
C.稀硫酸 D.蒸馏水
(3)相对分子质量的确定一般利用质谱法、蒸气密度法等。某有机物A的质谱图显示其相对分子质量最大是72。组成元素的测定常采用元素分析仪,也可采用燃烧法。称取3.6 g A,在足量氧气中充分燃烧,生成物通过浓硫酸后,浓硫酸的质量增加5.4 g,剩余气体通过碱石灰,碱石灰的质量增加11 g,则有机物A的分子式为___________ 。
(4)核磁共振谱常用氢谱或碳谱,它主要测定分子中具有不同特点的H或C的种类与比例。如对于有机物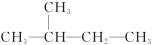 ,其碳谱有四组峰,峰面积之比为2∶1∶1∶1;氢谱有四组峰,峰面积之比为1∶2∶3∶6.有机物A的碳谱有两组峰,峰面积之比为4∶1,氢谱有一组峰。试写出有机物A的结构简式:
,其碳谱有四组峰,峰面积之比为2∶1∶1∶1;氢谱有四组峰,峰面积之比为1∶2∶3∶6.有机物A的碳谱有两组峰,峰面积之比为4∶1,氢谱有一组峰。试写出有机物A的结构简式:___________ 。
(5)有机物A的二氯代物有___________ 种。
2
 +NaOH
+NaOH
 +
+
某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:

重结晶过程:溶解
 活性炭脱色
活性炭脱色 趁热过滤
趁热过滤 冷却结晶
冷却结晶 抽滤
抽滤 洗涤
洗涤 干燥。
干燥。已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。苯甲酸微溶于水,乙醚难溶于水。
请根据以上信息,回答下列问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是
(2)苯甲酸在A、B、C三种溶剂中的溶解度(S)随温度变化的曲线如图所示。重结晶时,合适的溶剂是

A.饱和食盐水 B.Na2CO3溶液
C.稀硫酸 D.蒸馏水
(3)相对分子质量的确定一般利用质谱法、蒸气密度法等。某有机物A的质谱图显示其相对分子质量最大是72。组成元素的测定常采用元素分析仪,也可采用燃烧法。称取3.6 g A,在足量氧气中充分燃烧,生成物通过浓硫酸后,浓硫酸的质量增加5.4 g,剩余气体通过碱石灰,碱石灰的质量增加11 g,则有机物A的分子式为
(4)核磁共振谱常用氢谱或碳谱,它主要测定分子中具有不同特点的H或C的种类与比例。如对于有机物
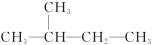 ,其碳谱有四组峰,峰面积之比为2∶1∶1∶1;氢谱有四组峰,峰面积之比为1∶2∶3∶6.有机物A的碳谱有两组峰,峰面积之比为4∶1,氢谱有一组峰。试写出有机物A的结构简式:
,其碳谱有四组峰,峰面积之比为2∶1∶1∶1;氢谱有四组峰,峰面积之比为1∶2∶3∶6.有机物A的碳谱有两组峰,峰面积之比为4∶1,氢谱有一组峰。试写出有机物A的结构简式:(5)有机物A的二氯代物有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】(1)青蒿素结构如图,有关叙述正确的是_____ (选填序号)。
c.易溶于水 d.含有过氧键,有较强氧化性
由青蒿酸为原料出发,经五步合成可得到青蒿素,其中第2步为还原反应:
某学习小组在实验室用双氢青蒿酸甲酯制取青蒿醇。
(2)反应中使用过量的氢化铝锂,理由是_____________________________________________ 。为使反应在溶液状态下进行,可用乙醚为溶剂,不用水的理由是____________________ 。
(3)请设计实验室制备装置(画出草图):____________
(4)该反应有机物的转化率约为96%,所得乙醚溶液中含有醇锂、醇铝、双氢青蒿酸甲酯、氢化铝锂。从反应混合物中提取青蒿醇的方法是:
①加_______ 后分液;
②从乙醚层提取青蒿醇。有多种方法,以下是二种方案:
方案一:蒸发结晶。 方案二:蒸馏析出晶体。
a.这2个方案在析出晶体后都应有残留液,原因是___________________________________ 。
b.请对这2个方案进行比较_______________________________________________________ 。

c.易溶于水 d.含有过氧键,有较强氧化性
由青蒿酸为原料出发,经五步合成可得到青蒿素,其中第2步为还原反应:

| 物质 | 性质 |
| 双氢青蒿酸甲酯(C16H28O2) | 固体,难溶于水,易溶于有机溶剂。 |
| 青蒿醇(C15H28O) | 固体,难溶于水,易溶于有机溶剂。 |
| 乙醚 | 无色液体,微溶于水;密度0.71g/cm3;沸点34.6℃。 |
| 氢化铝锂 | 固体,溶于乙醚。 与水反应:LiAlH4 + 4H2O →Al(OH)3↓+ LiOH +4H2↑ 可将一分子酯还原成二分子醇,自身生成醇铝、醇锂。 (醇铝、醇锂可与盐酸反应,生成铝盐、锂盐和相应的醇)。 |
某学习小组在实验室用双氢青蒿酸甲酯制取青蒿醇。
(2)反应中使用过量的氢化铝锂,理由是
(3)请设计实验室制备装置(画出草图):
(4)该反应有机物的转化率约为96%,所得乙醚溶液中含有醇锂、醇铝、双氢青蒿酸甲酯、氢化铝锂。从反应混合物中提取青蒿醇的方法是:
①加
②从乙醚层提取青蒿醇。有多种方法,以下是二种方案:
方案一:蒸发结晶。 方案二:蒸馏析出晶体。
a.这2个方案在析出晶体后都应有残留液,原因是
b.请对这2个方案进行比较
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下方法来制备无水FeCl2。有关物质的性质如下:
方法一:用H2还原无水FeCl3制取FeCl2。有关装置如下:____________ 。
(2)按气流由左到右的方向,上述仪器的连接顺序为____________。
(3)该制备装置的缺点为____________ 。
方法二:利用反应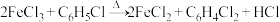 制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。
制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。_____________ 。
(5)仪器b中干燥剂可以选择_____________。
(6)反应结束后恢复至室温,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用最佳试剂是___________ 。
(7)回收滤液中C6H6Cl的操作方法是_____________。
(8)反应后将c中溶液稀释至250mL。量取25.00mL所配溶液,用0.400mol·L-1标准NaOH溶液滴定,终点时消耗标准液19.60mL。则氯化铁的转化率为___________ 。
(9)若反应后通入N2时间不足,则测得氯化铁的转化率______________ 。
A.偏低 B.偏高 C.不影响
(10)制备无水FeCl2需要用到无水FeCl3,某同学提出利用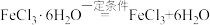 制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方_______________ 。
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯;易溶于乙醇,易吸水 | ||
| 熔点/℃ | -45 | 53 | 100℃时升华 | 672 |
| 沸点/℃ | 132 | 173 | >1000 | |
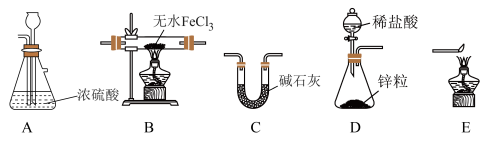
(2)按气流由左到右的方向,上述仪器的连接顺序为____________。
| A.D→C→B→A→E | B.D→A→B→C→E |
| C.D→B→A→C→E | D.D→C→A→B→E |
(3)该制备装置的缺点为
方法二:利用反应
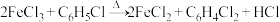 制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。
制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。
(5)仪器b中干燥剂可以选择_____________。
| A.碱石灰 | B.无水硫酸铜 | C.无水氯化钙 | D.浓硫酸 |
(6)反应结束后恢复至室温,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用最佳试剂是
(7)回收滤液中C6H6Cl的操作方法是_____________。
| A.萃取 | B.分液 | C.过滤 | D.蒸馏 |
(8)反应后将c中溶液稀释至250mL。量取25.00mL所配溶液,用0.400mol·L-1标准NaOH溶液滴定,终点时消耗标准液19.60mL。则氯化铁的转化率为
(9)若反应后通入N2时间不足,则测得氯化铁的转化率
A.偏低 B.偏高 C.不影响
(10)制备无水FeCl2需要用到无水FeCl3,某同学提出利用
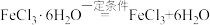 制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】TiCl4是制备钛及其化合物的重要中间体,某小组同学利用下列装置在实验室制备TiCl4,设计实验如下(夹持装置略去);

相关信息如下表所示:
请回答下列问题:
(1)按照气流由左到右的方向,上述装置合理的连接顺序为_____________ (填仪器接口字母)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;_____________
(按正确的顺序填入下列操作的字母)。
A.关闭分液漏斗活塞B.停止加热,充分冷却
C.打开分液漏斗活塞D.加热装置D中陶瓷管
实验时,当观察到______________ 时,开始进行步骤D。
(3)装置A中导管m的作用为_______________________ 。
(4)装置C的作用为___________________________________________ 。
(5)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为__________________________________ 。
(6)设计实验证明装置 F中收集到的液体中含有TiCl4:______________________________________________ 。
(7)制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为_________________ 。

相关信息如下表所示:
熔点/℃ | 沸点/℃ | 密度/(g • cm-3) | 水溶性 | |
TiCl4 | -25 | 136 | 1.5 | 易水解,能溶于有机溶剂 |
CC14 | -23 | 76.8 | 1.6 | 难溶于水 |
(1)按照气流由左到右的方向,上述装置合理的连接顺序为
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;
(按正确的顺序填入下列操作的字母)。
A.关闭分液漏斗活塞B.停止加热,充分冷却
C.打开分液漏斗活塞D.加热装置D中陶瓷管
实验时,当观察到
(3)装置A中导管m的作用为
(4)装置C的作用为
(5)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为
(6)设计实验证明装置 F中收集到的液体中含有TiCl4:
(7)制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
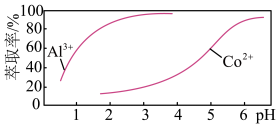
(1)“萃取分离”溶液中钴、锂的萃取率与平衡时溶液 的关系如图所示,
的关系如图所示, 一般选择5左右,理由是
一般选择5左右,理由是_______ 。

(2)萃取剂对 、
、 萃取率与
萃取率与 的关系如图所示。
的关系如图所示。
萃取分离钴、铝的实验操作:向萃取分液后的有机相中加稀硫酸调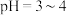 ,分液可得
,分液可得 溶液;
溶液;_______ ,可得 溶液。
溶液。
(3)已知萃取剂A、B中 对钴离子、锰离子萃取率的影响如图所示,为了除去
对钴离子、锰离子萃取率的影响如图所示,为了除去 ,应选择萃取剂
,应选择萃取剂_______ (填“A”或“B”)。

(1)“萃取分离”溶液中钴、锂的萃取率与平衡时溶液
 的关系如图所示,
的关系如图所示, 一般选择5左右,理由是
一般选择5左右,理由是
(2)萃取剂对
 、
、 萃取率与
萃取率与 的关系如图所示。
的关系如图所示。
萃取分离钴、铝的实验操作:向萃取分液后的有机相中加稀硫酸调
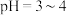 ,分液可得
,分液可得 溶液;
溶液; 溶液。
溶液。(3)已知萃取剂A、B中
 对钴离子、锰离子萃取率的影响如图所示,为了除去
对钴离子、锰离子萃取率的影响如图所示,为了除去 ,应选择萃取剂
,应选择萃取剂
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】选择下列实验方法分离物质,将分离方法的括号填在横线上。
A.萃取分液 B.过滤 C.结晶 D.分液 E.蒸馏
(1)分离饱和食盐水与沙子的混合物。______
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾。______
(3)分离水和汽油的混合物。______
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。______
A.萃取分液 B.过滤 C.结晶 D.分液 E.蒸馏
(1)分离饱和食盐水与沙子的混合物。
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)分离水和汽油的混合物。
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】从海藻中提取碘的流程图如下:
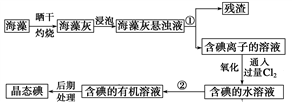
(1)制取碘的过程中操作②的名称:____________ , 在该操作中用到的玻璃仪器有______________ ,操作过程中观察到有机层液体为______ 色。
(2)提取碘的过程中,可供选择的有机溶剂是________ (填字母序号)。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
理由是______________________________________ 。(乙酸、甘油均可溶于水)
(3)含碘的有机物溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察下列实验装置,指出其错误之处,并指出正确操作。
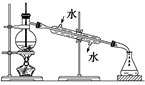
_______________________________________

(1)制取碘的过程中操作②的名称:
(2)提取碘的过程中,可供选择的有机溶剂是
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
理由是
(3)含碘的有机物溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察下列实验装置,指出其错误之处,并指出正确操作。

您最近一年使用:0次



