 是周期表中
是周期表中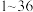 号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.(1)
 的电子式为
的电子式为 中含有的化学键类型为
中含有的化学键类型为(2)B、C两种元素的第三电离能由大到小的顺序为
(3)E在元素周期表中位置为
(4)比较:①键角大小:

 ;②在水中的溶解性大小
;②在水中的溶解性大小
 ;
;
更新时间:2024-03-01 07:08:50
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】W、X、Y、Z是短周期元素,其部分性质如表:
(1)X的简单氢化物的结构式_____ ,Y和W形成的化合物YW2的电子式_____ 。
(2)元素Z在周期表中的位置_____ 。
(3)比较X、Y最高价氧化物对应的水化物的酸性:_____ >_____ (填化学式)。
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的 |
| Z | 第三周期简单离子半径最小 |
(2)元素Z在周期表中的位置
(3)比较X、Y最高价氧化物对应的水化物的酸性:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图___ ,E元素在周期表中的位置是___ 。
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为___ 。(选序号)
a.离子键 b.极性共价键 c.非极性共价键
(3)D与C按原子个数比为1:1形成化合物的电子式是___ 。
(4)B、C所形成简单氢化物的稳定性由强到弱的顺序是___ (填化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和化合物甲反应的离子方程式___ 。
(1)画出D的原子结构示意图
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为
a.离子键 b.极性共价键 c.非极性共价键
(3)D与C按原子个数比为1:1形成化合物的电子式是
(4)B、C所形成简单氢化物的稳定性由强到弱的顺序是
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和化合物甲反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
I.乳酸(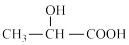 )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。
(1)在生活中,常选择上述物质中_______________ (填结构简式)清洗水壶里的水垢。
(2)生活中常选择_______________ 酒精 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水” 皮肤消毒。
皮肤消毒。
(3)上述物质中,属于天然高分子化合物的是_________________  填名称
填名称 。
。
(4)乳酸中发生如下变化: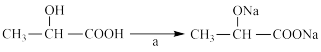 ,则所用的试剂a为
,则所用的试剂a为________ (写化学式)。
II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
(5)X在元素周期表中的位置为___________ ;Y元素的名称为________________ 。
(6)元素W的离子结构示意图是_______________ ;Z、Y形成的化合物为____________ (用化学式表示)。
I.乳酸(
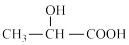 )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。(1)在生活中,常选择上述物质中
(2)生活中常选择
 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水” 皮肤消毒。
皮肤消毒。(3)上述物质中,属于天然高分子化合物的是
 填名称
填名称 。
。(4)乳酸中发生如下变化:
 ,则所用的试剂a为
,则所用的试剂a为II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最外层电子数是次外层的2倍 |
| Y | M层上的电子数是K层的3倍 |
| Z | Z的一种核素的质量数为53,中子数为34 |
| W | W2+与氖原子具有相同核外电子排布 |
(5)X在元素周期表中的位置为
(6)元素W的离子结构示意图是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】下表为长式周期表的一部分,其中的编号代表对应的元素。
(1)写出上表中元素⑾原子的外围电子排布式___________ 。元素⑿正三价离子的核外电子排布式_________________ 元素⑥负一价离子的结构示意图__________ 。
(2)元素⑦与⑥形成的化合物的电子式为:___________ ,其形成的化合物的晶体类型是:____________
(3)元素④、⑤的第一电离能较大的是:___________ (用元素符号表示)。元素⑤、⑥电负性较大的是:______________ (用元素符号表示)。
(4)④、⑤、⑥三种元素形成的离子,离子半径最大的是:___________ 。(用离子符号表示)
(5)⑦、⑧与水反应最剧烈的物质是___________ 。(填化学式)
(6)元素(11)在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:___________ 。

| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ⑨ | ⑩ | ||||||||||||||
| ⑾ | ⑿ | ⒀ |
(2)元素⑦与⑥形成的化合物的电子式为:
(3)元素④、⑤的第一电离能较大的是:
(4)④、⑤、⑥三种元素形成的离子,离子半径最大的是:
(5)⑦、⑧与水反应最剧烈的物质是
(6)元素(11)在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
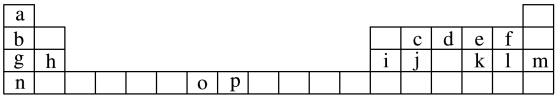
(1)c、d、e、f四种元素的第一电离能由小到大的顺序为_______ (填元素符号),l和n的离子半径较大的是_______ (填离子符号)。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光子的形式释放能量,以下现象与该原理一样的是_______ 。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据列于下表:比较两元素的 、
、 可知,气态
可知,气态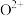 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)第三周期8种元素中电负性最大的是_______ (填元素符号)。
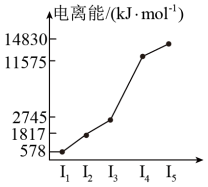
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式_______ 。

(1)c、d、e、f四种元素的第一电离能由小到大的顺序为
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光子的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据列于下表:比较两元素的
 、
、 可知,气态
可知,气态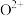 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是| 元素 | 0 | P | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
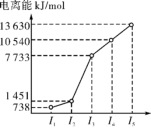
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有__________ 种不同空间运动状态的电子。
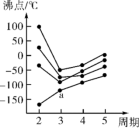
(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是___________ 。判断依据是_____________________ 。
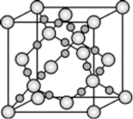
(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于___________ 晶体。
(4)第一电离能介于 Al、P 之间的第三周期元素有___________ 种。 GaCl3 中中心原子的杂化方式为___________ ,写出与 GaCl3 结构相同的一种离子___________ 。
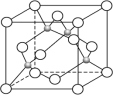
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为___________ g/cm3.(列出计算式即可)
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有

(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是

(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于

(4)第一电离能介于 Al、P 之间的第三周期元素有
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】三氟化氮( )是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有
)是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有 、
、 和
和 ,请根据要求回答下列问题:
,请根据要求回答下列问题:
(1) 键的键能为
键的键能为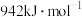 ,
, 单键的键能为
单键的键能为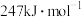 ,说明
,说明 中的
中的_____ (填“ ”或“
”或“ ”)键更稳定。
”)键更稳定。
(2) 的沸点(
的沸点( )比
)比 (
( )低的原因是
)低的原因是_____ 。
(3) 是一种无色、无臭的气体,但
是一种无色、无臭的气体,但 一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是
一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是_____ 。
(4) 的电离方程式为
的电离方程式为 ,
, 溶于水后形成
溶于水后形成 的结构是
的结构是_____ 。
(5)斯图杰尔和阿佩里曼成功地在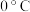 以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是
以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是_____ 。次氟酸分子中共价键的键角_____ (填“<”或“=”) 。
。
 )是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有
)是一种新型电子材料的原料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有 、
、 和
和 ,请根据要求回答下列问题:
,请根据要求回答下列问题:(1)
 键的键能为
键的键能为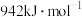 ,
, 单键的键能为
单键的键能为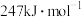 ,说明
,说明 中的
中的 ”或“
”或“ ”)键更稳定。
”)键更稳定。(2)
 的沸点(
的沸点( )比
)比 (
( )低的原因是
)低的原因是(3)
 是一种无色、无臭的气体,但
是一种无色、无臭的气体,但 一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是
一旦在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是(4)
 的电离方程式为
的电离方程式为 ,
, 溶于水后形成
溶于水后形成 的结构是
的结构是(5)斯图杰尔和阿佩里曼成功地在
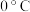 以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是
以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。次氟酸的结构是 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,回答下列问题:
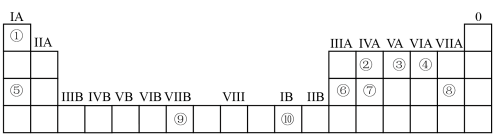
(1)①、②、③、④的电负性由大到小的顺序是__________________ (用元素符号表示).
(2)量子力学把电子在原子核外的一个空间运动状态 称为一个原子轨道,基态③原子的电子有______ 种空间运动状态 .
(3)④、⑤、⑥的原子半径由大到小的顺序为__________________ (用元素符号表示).
(4)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是__________________ (用化学式表示).
(5)①、④、⑤、⑧中的某些 元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________________________ .
(6)第一电离能( ):
):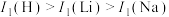 ,原因是
,原因是________________________ .
(7)铁元素在元素周期表中的位置________________________ ,基态 的价层电子排布式为
的价层电子排布式为________________________ .
(8)基态⑧原子占据的最高能级的电子云轮廓图的形状是______ 形;基态⑨原子的价层电子排布的轨道表示式为________________________ ;元素⑩属于______ 区(填“s”、“d”、“ds”或“p”).
(9)由④元素形成的常见物质有很多,例如: 、
、 、
、 等.基态④原子的核外电子排布式是
等.基态④原子的核外电子排布式是______ ,对 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测:
根据测定 分子中
分子中______ (填字母序号),确定其结构一定不是甲.
a.H—O键长 b.O—O键能 c.H—O—O键角

(1)①、②、③、④的电负性由大到小的顺序是
(2)量子力学把电子在原子核外的一个
(3)④、⑤、⑥的原子半径由大到小的顺序为
(4)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(5)①、④、⑤、⑧中的
(6)第一电离能(
 ):
):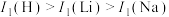 ,原因是
,原因是(7)铁元素在元素周期表中的位置
 的价层电子排布式为
的价层电子排布式为(8)基态⑧原子占据的最高能级的电子云轮廓图的形状是
(9)由④元素形成的常见物质有很多,例如:
 、
、 、
、 等.基态④原子的核外电子排布式是
等.基态④原子的核外电子排布式是 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测:
根据测定
 分子中
分子中a.H—O键长 b.O—O键能 c.H—O—O键角
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题。
(1)有下列粒子:①CH4 ②CH2O ③HCN ④NH3 ⑤ ⑥BF3 ⑦H2O。
⑥BF3 ⑦H2O。
①含有极性键的非极性分子的是______ (填编号,下同)。
②所有原子共平面的是_______ ,共线的是_______ 。
(2)过氧乙酸(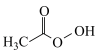 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有______ ,分子中σ键和π键的个数比为_______ 。
(3) GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为_____ ,每个 原子周围最近的
原子周围最近的 原子数目为
原子数目为______ 。已知GaAs的密度为d g/cm3,摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则晶胞的棱长为_____ nm(列式表示)。_____ (填字母)。
A.CO2 B.SiF4 C.SCl2 D. E.H3O+
E.H3O+
请分析键角大小比较的一般方法_____ 。
(1)有下列粒子:①CH4 ②CH2O ③HCN ④NH3 ⑤
 ⑥BF3 ⑦H2O。
⑥BF3 ⑦H2O。①含有极性键的非极性分子的是
②所有原子共平面的是
(2)过氧乙酸(
 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有(3)
 GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为 原子周围最近的
原子周围最近的 原子数目为
原子数目为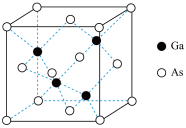
A.CO2 B.SiF4 C.SCl2 D.
 E.H3O+
E.H3O+请分析键角大小比较的一般方法
您最近一年使用:0次



