下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,回答下列问题:
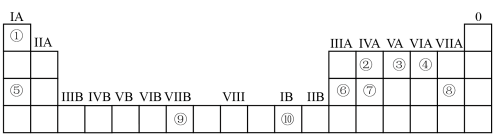
(1)①、②、③、④的电负性由大到小的顺序是__________________ (用元素符号表示).
(2)量子力学把电子在原子核外的一个空间运动状态 称为一个原子轨道,基态③原子的电子有______ 种空间运动状态 .
(3)④、⑤、⑥的原子半径由大到小的顺序为__________________ (用元素符号表示).
(4)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是__________________ (用化学式表示).
(5)①、④、⑤、⑧中的某些 元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________________________ .
(6)第一电离能( ):
):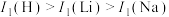 ,原因是
,原因是________________________ .
(7)铁元素在元素周期表中的位置________________________ ,基态 的价层电子排布式为
的价层电子排布式为________________________ .
(8)基态⑧原子占据的最高能级的电子云轮廓图的形状是______ 形;基态⑨原子的价层电子排布的轨道表示式为________________________ ;元素⑩属于______ 区(填“s”、“d”、“ds”或“p”).
(9)由④元素形成的常见物质有很多,例如: 、
、 、
、 等.基态④原子的核外电子排布式是
等.基态④原子的核外电子排布式是______ ,对 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测:
根据测定 分子中
分子中______ (填字母序号),确定其结构一定不是甲.
a.H—O键长 b.O—O键能 c.H—O—O键角

(1)①、②、③、④的电负性由大到小的顺序是
(2)量子力学把电子在原子核外的一个
(3)④、⑤、⑥的原子半径由大到小的顺序为
(4)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(5)①、④、⑤、⑧中的
(6)第一电离能(
 ):
):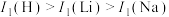 ,原因是
,原因是(7)铁元素在元素周期表中的位置
 的价层电子排布式为
的价层电子排布式为(8)基态⑧原子占据的最高能级的电子云轮廓图的形状是
(9)由④元素形成的常见物质有很多,例如:
 、
、 、
、 等.基态④原子的核外电子排布式是
等.基态④原子的核外电子排布式是 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测:
根据测定
 分子中
分子中a.H—O键长 b.O—O键能 c.H—O—O键角
更新时间:2024-03-01 20:55:30
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】我国科学家构建了新型催化剂“纳米片”(Co—N—C),该“纳米片“可用于氧化SO 和吸附Hg2+。回答下列问题:
和吸附Hg2+。回答下列问题:
(1)基态Co原子的价层电子排布式为___________ ,N、C、Co中第一电离能最大的是___________ (填元素符号)。
(2)在空气中SO 会被氧化成
会被氧化成 。
。 的空间构型是
的空间构型是___________ , 中S原子采用
中S原子采用___________ 杂化。
(3)氰气[(CN)2]称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则(CN)2分子中σ键、π键个数之比为___________ 。
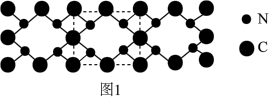
(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如图1所示。它的化学式为___________ ,它的硬度超过金刚石的主要原因是___________ 。
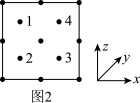
(5)氮化镓是新型半导体材料,其晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。图2为沿y轴投影的氮化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为( ,
, ,
,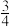 ),则原子3的原子分数坐标为
),则原子3的原子分数坐标为___________ 。
 和吸附Hg2+。回答下列问题:
和吸附Hg2+。回答下列问题:(1)基态Co原子的价层电子排布式为
(2)在空气中SO
 会被氧化成
会被氧化成 。
。 的空间构型是
的空间构型是 中S原子采用
中S原子采用(3)氰气[(CN)2]称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则(CN)2分子中σ键、π键个数之比为
(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如图1所示。它的化学式为

(5)氮化镓是新型半导体材料,其晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。图2为沿y轴投影的氮化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(
 ,
, ,
,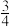 ),则原子3的原子分数坐标为
),则原子3的原子分数坐标为
您最近一年使用:0次
【推荐2】N,P,As等元素的化合物在生产和研究中有许多重要用途。请回答下列问题:
(1)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为_______ ,N—N键的键角为____ 。
(2)基态砷原子的价电子排布图为_______ ,砷与同周期相邻元素的第一电离能由大到小的顺序为______ 。
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是__________  填PH4”或“
填PH4”或“ ”
” 。
。
(4)SCl3+和 是等电子体,
是等电子体,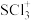 的空间构型是
的空间构型是_________ 。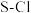 键键长
键键长____ 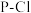 键键长
键键长 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,原因是
,原因是____________ 。
(1)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为
(2)基态砷原子的价电子排布图为
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。
 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是 填PH4”或“
填PH4”或“ ”
” 。
。(4)SCl3+和
 是等电子体,
是等电子体,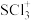 的空间构型是
的空间构型是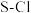 键键长
键键长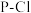 键键长
键键长 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,原因是
,原因是
您最近一年使用:0次
【推荐3】某电镀铜厂有两种废水,分别含有CN-和Cr2O72-等有毒离子,拟用NaClO和Na2S2O3按照下列流程进行处理。

请完成下列填空:
(1)HCN有剧毒,电子式是__ ,其分子属于__ (填“极性”、“非极性”)分子。
(2)表示原子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式。从中选择最详尽描述核外电子运动状态的方式,来表示氧原子的最外层电子的运动状态:__ ,其中最外层有__ 种不同能量的电子。
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是___ 。
a.相同条件下水溶液的pH:NaClO>Na2S2O3
b.还原性:H2S>HCl
c.相同条件下水溶液的酸性:HClO3>H2SO3
d.稳定性:HCl>H2S
(4)写出流程③的离子方程式为:___ 。
(5)反应③中,每消耗0.5molCr2O72-转移的电子数为___ ;
(6)取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,解释产生该现象的原因___ 。

请完成下列填空:
(1)HCN有剧毒,电子式是
(2)表示原子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式。从中选择最详尽描述核外电子运动状态的方式,来表示氧原子的最外层电子的运动状态:
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是
a.相同条件下水溶液的pH:NaClO>Na2S2O3
b.还原性:H2S>HCl
c.相同条件下水溶液的酸性:HClO3>H2SO3
d.稳定性:HCl>H2S
(4)写出流程③的离子方程式为:
(5)反应③中,每消耗0.5molCr2O72-转移的电子数为
(6)取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,解释产生该现象的原因
您最近一年使用:0次
【推荐1】有A、B、C、D四种元素其原子序数依次增大,且质子数均小于18,A元素原子的最外层只有1个电子,该元素形成的简单阳离子与 的核外电子排布相同;C元素原子的价电子排布式为
的核外电子排布相同;C元素原子的价电子排布式为 ;
; 的核外电子排布与
的核外电子排布与 的相同。回答下列问题:
的相同。回答下列问题:
(1)写出A、C、D的元素符号:A_______ 、C_______ 、D_______ 。
(2)B元素原子的电子排布式为_______ ;D元素原子的轨道表示式为_______ 。
(3)A、B、C、D的第一电离能由小到大的顺序为_______ (用元素符号表示,下同);电负性由小到大的顺序为_______ 。
 的核外电子排布相同;C元素原子的价电子排布式为
的核外电子排布相同;C元素原子的价电子排布式为 ;
; 的核外电子排布与
的核外电子排布与 的相同。回答下列问题:
的相同。回答下列问题:(1)写出A、C、D的元素符号:A
(2)B元素原子的电子排布式为
(3)A、B、C、D的第一电离能由小到大的顺序为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
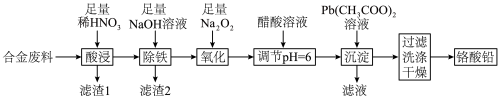
【推荐2】铬酸铅(PbCrO4)是黄色涂料“铬黄”的主要成分,实验室由某合金废料(主要成分为Fe、C、Cr2O3)制备PbCrO4的流程如图:
回答下列问题:
(1)基态82Pb2+的价层电子排布图为_______ 。
(2)“酸浸”时,加热可以加快反应速率,但温度不宜过高的原因是_______ (用化学方程式解释)。
(3)“滤渣2”中电负性最大的元素是_______ (填元素符号)。
(4)“氧化”时发生反应的离子方程式为_______ 。
(5)“调节pH=6”的目的是_______ 。
(6)二卤化铅(PbX2)是一类重要的含铅化合物,其熔点如下表所示:
①结合PbX2的熔点变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性_______ (填“增强”“不变”或“减弱”,后同)、共价性_______ 。
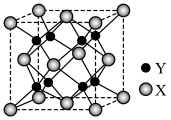
②PbF2的立方晶胞如图所示,其中X代表的离子是_______ (填离子符号);若该晶胞参数为anm,则正、负离子的最小核间距为_______ pm。
回答下列问题:
(1)基态82Pb2+的价层电子排布图为
(2)“酸浸”时,加热可以加快反应速率,但温度不宜过高的原因是
(3)“滤渣2”中电负性最大的元素是
(4)“氧化”时发生反应的离子方程式为
(5)“调节pH=6”的目的是
(6)二卤化铅(PbX2)是一类重要的含铅化合物,其熔点如下表所示:
| 二卤化铅 | PbF2 | PbCl2 | PbBr2 | PbI2 |
| 熔点/℃ | 824 | 501 | 373 | 402 |
②PbF2的立方晶胞如图所示,其中X代表的离子是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下图为元素周期表的一部分:

I.(1)元素③的基态原子轨道表示式为_________________ 。
(2)元素③④⑤的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)以下组合的原子间反应最容易形成离子键的是_____ (选填A、B、C、D,下同)。
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式_________________________________ 。
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。
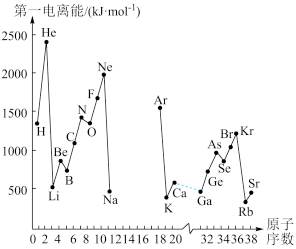
①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为___ < S <___ (填元素符号)
②图中第一电离能最小的元素在周期表中的位置____________________
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表( )
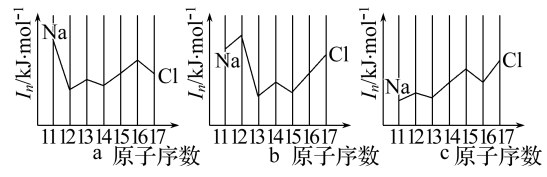
A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________________________________________

I.(1)元素③的基态原子轨道表示式为
(2)元素③④⑤的第一电离能由大到小的顺序为
(3)以下组合的原子间反应最容易形成离子键的是
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。

①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为
②图中第一电离能最小的元素在周期表中的位置
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表

A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
| 电离能/kJ/mol | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是
您最近一年使用:0次
【推荐1】硼酸( )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
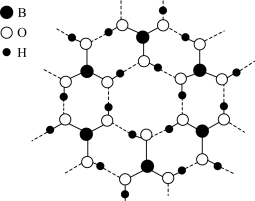
(1)关于 ,下列说法错误的是_______。
,下列说法错误的是_______。
(2)硼有两种天然同位素 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4) 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于_______ 元弱酸。B和 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:_______ 。
 )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
(1)关于
 ,下列说法错误的是_______。
,下列说法错误的是_______。A.分子中B原子采用 杂化 杂化 | B.硼酸晶体中层与层之间存在范德华力 |
C.1  晶体中含有6 晶体中含有6 氢键 氢键 | D. 水溶性较好 水溶性较好 |
(2)硼有两种天然同位素
 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。| A.80% | B.20% | C.略大于20% | D.略小于20% |
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为
(4)
 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】I.铁镁合金是一种性能优异的储氢材料。关于铁镁两种元素,请回答下列问题:
(1)同周期元素中,第一电离能小于镁的元素有_______ 种。
(2)基态Fe原子的简化电子排布式为_______ ,空间运动状态有_______ 种,Fe位于元周期表的_______ 区,基态原子的电子有_______ 种伸展方向。
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有_______ 种,下列状态的铁中,电离最外层一个电子所需能量最大的是_______ (填标号)。
a.[Ar] b.[Ar]
b.[Ar]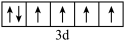
c.[Ar] d.[Ar]
d.[Ar]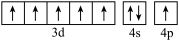
(4)试从结构角度解释 易被氧化为
易被氧化为
_______ 。
(5)对于呋喃: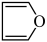 和吡咯:
和吡咯: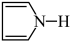 )所含的元素中,电负性最大的是
)所含的元素中,电负性最大的是_______ ,最小的是_______ ;第一电离能最大的是_______ 。
Ⅱ. 在食品、医药、电子工业中用途广泛。回答下列问题:
在食品、医药、电子工业中用途广泛。回答下列问题:
(6) 可做净水剂,其理由是
可做净水剂,其理由是_______ (用离子方程式表示)。
(7)下图是0.1mol/L电解质溶液的pH随温度变化的图像。其中符合0.1mol/L 溶液的是
溶液的是_______ (填罗马数字)。
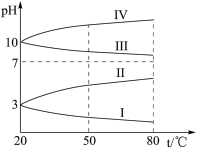
(8)20℃时,0.1mol/L 溶液中,
溶液中, =
=_______ mol/L(写出准确数值)。
Ⅲ、某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:请回答下列问题:
反应原理为: (Mn2+在溶液中为无色)
(Mn2+在溶液中为无色)
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点
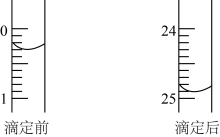
(9)若甲学生在实验过程中,记录滴定前后滴定管内液面读数如图所示,则此时消耗标准溶液的体积为_______ mL。
(10)此滴定实验达到终点的颜色变化为_______ 。
(11)重复滴定4次,每次消耗酸性KMnO4标准溶液的体积如表所示:
计算上述样品中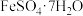 的质量分数为
的质量分数为_______ 。( ,小数点后保留一位)
,小数点后保留一位)
(12)若滴定前平视读数,滴定终点时仰视读数,则所测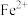 含量:
含量:_______ 。(填“无影响”、“偏高”或“偏低”)。
(1)同周期元素中,第一电离能小于镁的元素有
(2)基态Fe原子的简化电子排布式为
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有
a.[Ar]
 b.[Ar]
b.[Ar]
c.[Ar]
 d.[Ar]
d.[Ar]
(4)试从结构角度解释
 易被氧化为
易被氧化为
(5)对于呋喃:
 和吡咯:
和吡咯: )所含的元素中,电负性最大的是
)所含的元素中,电负性最大的是Ⅱ.
 在食品、医药、电子工业中用途广泛。回答下列问题:
在食品、医药、电子工业中用途广泛。回答下列问题:(6)
 可做净水剂,其理由是
可做净水剂,其理由是(7)下图是0.1mol/L电解质溶液的pH随温度变化的图像。其中符合0.1mol/L
 溶液的是
溶液的是

(8)20℃时,0.1mol/L
 溶液中,
溶液中, =
=Ⅲ、某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:请回答下列问题:
反应原理为:
 (Mn2+在溶液中为无色)
(Mn2+在溶液中为无色)a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点
(9)若甲学生在实验过程中,记录滴定前后滴定管内液面读数如图所示,则此时消耗标准溶液的体积为
(10)此滴定实验达到终点的颜色变化为
(11)重复滴定4次,每次消耗酸性KMnO4标准溶液的体积如表所示:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| V(KMnO4溶液)/mL | 17.10 | 19.98 | 20.00 | 20.02 |
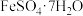 的质量分数为
的质量分数为 ,小数点后保留一位)
,小数点后保留一位)(12)若滴定前平视读数,滴定终点时仰视读数,则所测
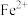 含量:
含量:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E是前四周期元素。A、B、C同周期,C、D同主族且原子半径C>D,A原子结构示意图为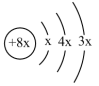 ,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:
(1)元素A、C、D的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(2)元素B、C、D中,其最高价氧化物对应水化物酸性最强的是_______ (填化学式,下同),简单离子半径最小的是_______ 。
(3)写出基态D原子的价电子轨道表示式_______ ,其电子占据最高能级的电子云轮廓图为_______ 形。
(4)E元素位于周期表中的_______ 区,其原子的价电子排布式为_______ 。
 ,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:(1)元素A、C、D的第一电离能由大到小的顺序是
(2)元素B、C、D中,其最高价氧化物对应水化物酸性最强的是
(3)写出基态D原子的价电子轨道表示式
(4)E元素位于周期表中的
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)键角:
______ 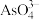 ,与
,与 互为等电子体的分子为
互为等电子体的分子为_______ (填化学式,任写一种即可)。
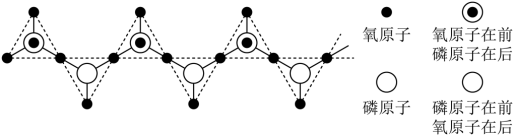
(2)浓磷酸在常温下呈粘稠状,原因_______ ,多聚磷酸由磷酸 加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为_______ 。
(3) 的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有_______ 个。
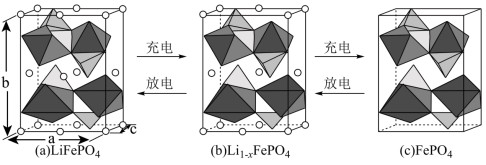
电池充电时, 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=_______ ,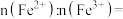
_______ 。
(1)键角:

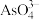 ,与
,与 互为等电子体的分子为
互为等电子体的分子为(2)浓磷酸在常温下呈粘稠状,原因
 加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
(3)
 的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有
电池充电时,
 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=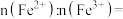
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】已知  和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题:
① 内的
内的 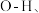 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为___________ ;
②用球棍模型表示的水分子结构是 ; 可与
可与  形成
形成 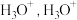 中的
中的 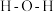 键角比
键角比  的键角
的键角___________ 。(填“大”或“小”)
(2)已知 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 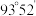 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 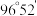 。
。
请回答下列问题:
① 子的电子式是
子的电子式是___________ ,结构式是___________ 。
② 分子是含有
分子是含有___________ 键和___________ 键的___________ (填“极性”或“非极性”)分子。
③ 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:___________ 。
 和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题: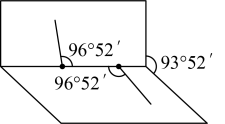
①
 内的
内的 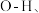 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为②用球棍模型表示的水分子结构是 ;
A. 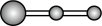 B.
B. 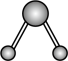 C.
C.  D.
D.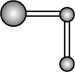
 可与
可与  形成
形成 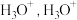 中的
中的 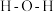 键角比
键角比  的键角
的键角(2)已知
 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 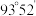 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 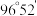 。
。请回答下列问题:
①
 子的电子式是
子的电子式是②
 分子是含有
分子是含有③
 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】硅烷广泛应用在现代高科技领域。制备硅烷的反应为:SiF4+NaAlH4=SiH4+NaAlF4.
(1)①基态硅原子的价层电子轨道表示式为_____ ,基态硅原子的电子有_____ 种空间运动状态。
②SiF4中,硅的化合价为+4价。硅显正化合价的原因是_____ 。
③下列说法正确的是_____ (填字母)。
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
④SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是_____ 。
⑤键角:SiF4_____ SiH4,原因_____ 。
(2)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-21cm3。
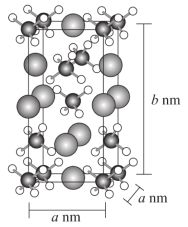
① 的VSEPR模型名称为
的VSEPR模型名称为_____ 。
②用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为_____ g•cm-3(用含a、b、NA的代数式表示)。
③NaAlH4是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:3NaAlH4═Na3AlH6+2Al+3H2↑。掺杂22Ti替换晶体中部分Al,更利于NaAlH4中H的解离,使体系更容易释放氢。从结构的角度推测其可能的原因:_____ 。
(1)①基态硅原子的价层电子轨道表示式为
②SiF4中,硅的化合价为+4价。硅显正化合价的原因是
③下列说法正确的是
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
④SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是
⑤键角:SiF4
(2)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-21cm3。

①
 的VSEPR模型名称为
的VSEPR模型名称为②用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为
③NaAlH4是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:3NaAlH4═Na3AlH6+2Al+3H2↑。掺杂22Ti替换晶体中部分Al,更利于NaAlH4中H的解离,使体系更容易释放氢。从结构的角度推测其可能的原因:
您最近一年使用:0次



