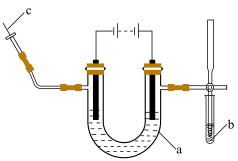
Ⅰ.海水中的氯化钠被提纯和精制后,可通过电解饱和食盐水制取氯气、氢气和氢氧化钠。实验室电解饱和食盐水所用装置如下图所示:___________ 。
A.试管 B.离心试管 C.U形管 D.Y形试管
②在a的两端滴加酚酞试液,通电后左边电极周围出现红色,写出该电极的电极反应式说明溶液变红的原因___________ 。
(2)通电后试管b中淀粉KI溶液由无色变为蓝色,结合离子方程式说明变化原因。___________ 。
(3)c处出来的气体可以点燃,其燃烧的现象是___________ 。
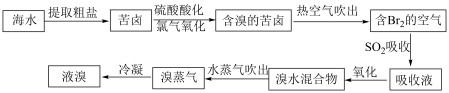
Ⅱ.地球上99%的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如下图所示:
(5)上述流程中热空气吹出已经得到了粗溴,为什么还要添加“SO2吸收、氧化、水蒸气吹出”三个步骤,其目的是___________ 。
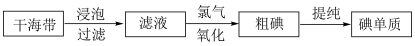
Ⅲ.海洋中的海带等海藻类植物具有富集碘的能力,工业上获取碘的主要流程如下图所示:
Ⅳ.硫元素和氮元素也存在于海洋中。
(7) 是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是
是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是___________ 。
(8)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环起始于氮的固定,过程可用下图表示。下列关于海洋氮循环的说法正确的是___________。
(9)N、O、S三种元素第一电离能由大到小的顺序为___________ 。
A.O > S > N B.S > N > O C.N > O > S D.O > N > S
A.试管 B.离心试管 C.U形管 D.Y形试管
②在a的两端滴加酚酞试液,通电后左边电极周围出现红色,写出该电极的电极反应式说明溶液变红的原因
(2)通电后试管b中淀粉KI溶液由无色变为蓝色,结合离子方程式说明变化原因。
(3)c处出来的气体可以点燃,其燃烧的现象是
Ⅱ.地球上99%的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如下图所示:
| A.溴离子的还原性 | B.溴单质的还原性 | C.溴的沸点高 | D.HBr极易溶于水 |
(5)上述流程中热空气吹出已经得到了粗溴,为什么还要添加“SO2吸收、氧化、水蒸气吹出”三个步骤,其目的是
Ⅲ.海洋中的海带等海藻类植物具有富集碘的能力,工业上获取碘的主要流程如下图所示:
| A.酒精 | B.裂化汽油 | C.四氯化碳 | D.乙酸 |
Ⅳ.硫元素和氮元素也存在于海洋中。
(7)
 是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是
是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是(8)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环起始于氮的固定,过程可用下图表示。下列关于海洋氮循环的说法正确的是___________。
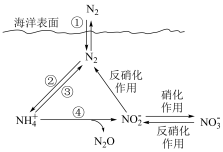
| A.海洋中的氮循环起始于氮的氧化 | B.海洋中的氮循环属于固氮作用的是③ |
| C.海洋中的硝化作用可能有氧气的参与 | D.NH4NO3中只含离子键 |
(9)N、O、S三种元素第一电离能由大到小的顺序为
A.O > S > N B.S > N > O C.N > O > S D.O > N > S
更新时间:2024-03-16 09:01:30
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池和液晶显示器制造中得到广泛应用。 是一种三角锥型分子,键角
是一种三角锥型分子,键角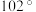 ,沸点
,沸点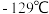 ;可在铜的催化作用下由
;可在铜的催化作用下由 和过量
和过量 反应得到:
反应得到: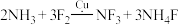
 上述化学方程式中的5种物质所含的化学键类型有
上述化学方程式中的5种物质所含的化学键类型有 ______  填序号
填序号 。
。
 离子键
离子键 共价键
共价键 配位键
配位键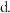 金属键
金属键
 与铜属于同一周期,且未成对价电子数最多的元素基态原子价电子排布式为
与铜属于同一周期,且未成对价电子数最多的元素基态原子价电子排布式为 ______ 。
 的沸点比
的沸点比 的沸点
的沸点 低得多的主要原因是
低得多的主要原因是 ______ 。
 理论上HF、
理论上HF、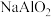 和NaCl按6:1:2的物质的量之比恰好反应生成HCl、
和NaCl按6:1:2的物质的量之比恰好反应生成HCl、 和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用.该物质为配合物,其中心离子是
和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用.该物质为配合物,其中心离子是 ______ ,配位数为 ______ 。
 根据下列五种元素的第一至第四电离能数据
根据下列五种元素的第一至第四电离能数据 单位:
单位:
 ,回答下面各题:
,回答下面各题:
①在周期表中,最可能处于同一族的是______ 和 ______ 。
②T元素最可能是______ (填“s”、“p”、“d”、“ds”等)区元素。若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物的空间构型为 ______ ,其中心原子的杂化轨道类型为 ______ 。
 是一种三角锥型分子,键角
是一种三角锥型分子,键角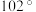 ,沸点
,沸点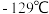 ;可在铜的催化作用下由
;可在铜的催化作用下由 和过量
和过量 反应得到:
反应得到: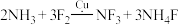
 上述化学方程式中的5种物质所含的化学键类型有
上述化学方程式中的5种物质所含的化学键类型有  填序号
填序号 。
。 离子键
离子键 共价键
共价键 配位键
配位键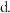 金属键
金属键  与铜属于同一周期,且未成对价电子数最多的元素基态原子价电子排布式为
与铜属于同一周期,且未成对价电子数最多的元素基态原子价电子排布式为  的沸点比
的沸点比 的沸点
的沸点 低得多的主要原因是
低得多的主要原因是  理论上HF、
理论上HF、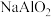 和NaCl按6:1:2的物质的量之比恰好反应生成HCl、
和NaCl按6:1:2的物质的量之比恰好反应生成HCl、 和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用.该物质为配合物,其中心离子是
和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用.该物质为配合物,其中心离子是  根据下列五种元素的第一至第四电离能数据
根据下列五种元素的第一至第四电离能数据 单位:
单位:
 ,回答下面各题:
,回答下面各题: | 元素代号 |  |  | 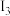 | 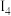 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是
②T元素最可能是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Fe2+、Fe3+与O22-、CN-、F-有机分子等形成的化合物具有广泛的应用。
(1)C、N、O原子的第一电离能由大到小的顺序是___________________________ 。
(2)Fe2+基态核外电子排布式为_____________________________ 。
(3)乙酰基二茂铁是常用汽油抗震剂,其结构如图1所示。

此物质中碳原子的杂化方式是______________________ 。
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为________ 。已知(CN)2是直线型分子,并具有对称性,则(CN)2中π键和σ键的个数比为_____________ 。
(5)F-不仅可与Fe3+形成[FeF6]3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,结构如图2所示。
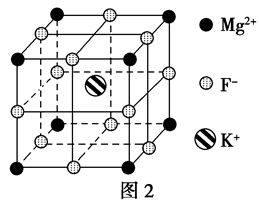
该晶体的化学式为___________________________________ 。
(1)C、N、O原子的第一电离能由大到小的顺序是
(2)Fe2+基态核外电子排布式为
(3)乙酰基二茂铁是常用汽油抗震剂,其结构如图1所示。

此物质中碳原子的杂化方式是
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为
(5)F-不仅可与Fe3+形成[FeF6]3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,结构如图2所示。

该晶体的化学式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】白钨矿(CaWO4)常伴生有方解石(CaCO3)、茧石(CaF2)和氟磷灰石[Ca10(PO4)6F2],具有良好的发光性,可用于生产苂光材料。
(1)已知元素W的原子序数为74,与元素Cr位于周期表的同一族,W在周期表中的位置为_____ 。
(2)元素C、O、F的第一电离能由小到大的顺序为______ ,从原子结构角度解释______ 。
(3)CO 与PO
与PO 的中心原子杂化方式分别为
的中心原子杂化方式分别为______ 。
(4)CaWO4的晶胞结构如图1所示,隐去氧离子后的晶胞前视图如图2所示。

(1)晶胞中氧原子的数目为_____ 。
(2)1号Ca2+的分数坐标为_____ 。
(1)已知元素W的原子序数为74,与元素Cr位于周期表的同一族,W在周期表中的位置为
(2)元素C、O、F的第一电离能由小到大的顺序为
(3)CO
 与PO
与PO 的中心原子杂化方式分别为
的中心原子杂化方式分别为(4)CaWO4的晶胞结构如图1所示,隐去氧离子后的晶胞前视图如图2所示。

(1)晶胞中氧原子的数目为
(2)1号Ca2+的分数坐标为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
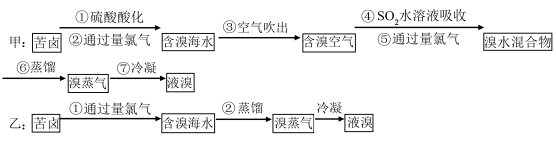
(1)甲、乙两同学在第一阶段得到含溴海水中,氯气的利用率较高的是________ (填“甲”或“乙”),原因是____________________________________ 。
(2)甲同学步骤④所发生反应的离子方程式为________________________ 。
(3)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是________ (填“甲”或“乙”),理由是__________________________________ 。
(4)某课外小组在实验室模拟工业上从浓缩海水中提取溴的工艺流程,设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。下列说法错误的是___________ 。

A.A装置中通入的a气体是Cl2
B.实验时应在A装置中通入a气体一段时间后,停止通入,改通入热空气
C.B装置中通入的b气体是SO2
D.C装置的作用只是吸收多余的SO2气体

(1)甲、乙两同学在第一阶段得到含溴海水中,氯气的利用率较高的是
(2)甲同学步骤④所发生反应的离子方程式为
(3)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是
(4)某课外小组在实验室模拟工业上从浓缩海水中提取溴的工艺流程,设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。下列说法错误的是

A.A装置中通入的a气体是Cl2
B.实验时应在A装置中通入a气体一段时间后,停止通入,改通入热空气
C.B装置中通入的b气体是SO2
D.C装置的作用只是吸收多余的SO2气体
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】南通有较长的海岸线, 海水资源的利用具有广阔的前景。工业上从海水中提取Br2与Mg 的流程如图:
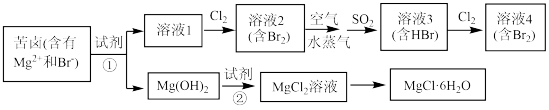
(1)写出一种海水淡化的方法:_______________ 。
(2)用电子式表示 MgCl2的形成过程:____________ 。
(3)工业上用MgCl2制取 Mg 一般常用的方法是________ 。
A.电解法 B.还原剂还原法 C.热分解法 D.铝热法
(4)提取溴的过程中,经过2次Br-⟶Br2转化的目的是___________ 。
(5)反应①,SO2被Br2氧化为 ,则该反应中消耗的n(SO2):n(Br2)=
,则该反应中消耗的n(SO2):n(Br2)= __ ;反应②的离子方程式为 __________ 。
(6)用下面提供的试剂,设计简单的实验证明Br 的非金属性比 I 强。(已知Br2和I2溶在水中浓度较稀时都呈黄色)。__________ 。(可选择的试剂:溴水、碘水、KI 溶液、四氯化碳、氯水、淀粉溶液。)

(1)写出一种海水淡化的方法:
(2)用电子式表示 MgCl2的形成过程:
(3)工业上用MgCl2制取 Mg 一般常用的方法是
A.电解法 B.还原剂还原法 C.热分解法 D.铝热法
(4)提取溴的过程中,经过2次Br-⟶Br2转化的目的是
(5)反应①,SO2被Br2氧化为
 ,则该反应中消耗的n(SO2):n(Br2)=
,则该反应中消耗的n(SO2):n(Br2)= (6)用下面提供的试剂,设计简单的实验证明Br 的非金属性比 I 强。(已知Br2和I2溶在水中浓度较稀时都呈黄色)。
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海水资源的利用具有广阔的前景。从海水中提取Br2与MgCl2•6H2O并准备金属镁部分流程如图:
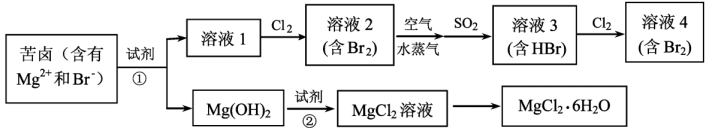
(1)为节约成本,试剂①最好选用____ 。
(2)提取溴过程中,从溶液l到溶液4,两次进行Br-→Br2的转化,目的是____ 。
(3)提取溴过程中,形成溶液3的化学方程式是____ 。
(4)用原子结构原理解释Cl2的氧化性强于Br2的原因____ 。
(5)工业制备金属镁的方程式为____ 。
(6)从MgCl2溶液获得MgCl2•6H2O晶体的主要操作为____ 。

(1)为节约成本,试剂①最好选用
(2)提取溴过程中,从溶液l到溶液4,两次进行Br-→Br2的转化,目的是
(3)提取溴过程中,形成溶液3的化学方程式是
(4)用原子结构原理解释Cl2的氧化性强于Br2的原因
(5)工业制备金属镁的方程式为
(6)从MgCl2溶液获得MgCl2•6H2O晶体的主要操作为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】海带中含有丰富的碘元素,某实验小组设计如图流程,从海带中提取碘。

(1)灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是___ (填字母);
A.烧杯 B.蒸发皿 C.坩埚 D.试管 E.酒精灯
(2)提取碘的过程中有关的实验操作名称:①___ ,③____ ;
(3)②对应的离子反应方程式为____ ;
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:__ ;
(5)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,装置如图。使用水浴的优点是___ ,最后晶态碘在____ 里聚集(填仪器名称)。
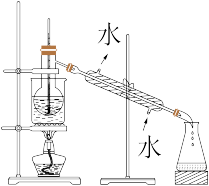

(1)灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是
A.烧杯 B.蒸发皿 C.坩埚 D.试管 E.酒精灯
(2)提取碘的过程中有关的实验操作名称:①
(3)②对应的离子反应方程式为
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
(5)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,装置如图。使用水浴的优点是

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验一 碘含量的测定

取0.0100 mol/L的 AgNO3标准溶液装入滴定管,取100.00 mL 海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中c(I-)的变化,部分数据如下表:
回答下列问题:
(1)实验中“灼烧”是在___________ (填仪器名称)中完成的。
(2)用文字具体描述“定容”过程:__________________________________
(3)根据表中数据判断滴定终点时用去AgNO3溶液的体积为___________ mL,计算得海带中碘的质量百分含量为_______________________ %。
实验二 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
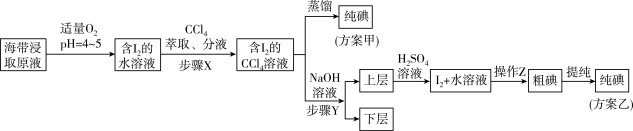
已知:3I2+6NaOH=5NaI+NaIO3+3H2O
(4)“适量O2”中能代替O2的最佳物质对应的电子式为_________________
(5)若要测定“I2+水溶液”中碘的含量,可以选择______________ 作指示剂,用 Na2S2O3溶液滴定,滴定终点的现象是____________________ 。
(6)若得到“I2+水溶液”时加入硫酸溶液过多,用Na2S2O3溶液滴定时会产生明显的误差,产生此误差的原因为_________________ (用离子方程式表示)。
实验一 碘含量的测定

取0.0100 mol/L的 AgNO3标准溶液装入滴定管,取100.00 mL 海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中c(I-)的变化,部分数据如下表:
V(AgNO )/mL )/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
(1)实验中“灼烧”是在
(2)用文字具体描述“定容”过程:
(3)根据表中数据判断滴定终点时用去AgNO3溶液的体积为
实验二 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O
(4)“适量O2”中能代替O2的最佳物质对应的电子式为
(5)若要测定“I2+水溶液”中碘的含量,可以选择
(6)若得到“I2+水溶液”时加入硫酸溶液过多,用Na2S2O3溶液滴定时会产生明显的误差,产生此误差的原因为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】海洋是巨大的资源宝库。
I.从海水中提取食盐和溴的过程如下:

(1)以上步骤I中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是_______ 。步骤Ⅱ.通入热空气或水蒸气吹出 ,利用了溴的
,利用了溴的_______ 性。
(2)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:_______ 。
Ⅱ.海藻中富含碘元素。某化学兴趣小组的同学在实验室里用灼烧海藻的灰分提取碘,流程如图:
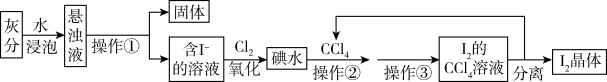
请回答下列问题:
(3)操作②选用 的理由是_______(填标号)。
的理由是_______(填标号)。
(4)用NaOH浓溶液反萃取后再加稀酸,可以分离 和
和 ,有关化学方程式为:
,有关化学方程式为:
碱性条件: 。
。
酸性条件: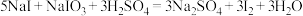 。
。
以下是反萃取过程的操作,请按要求填空:
①向装有 的
的 溶液的
溶液的_______ (填仪器名称)中加入少量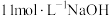 溶液;
溶液;
②振荡至溶液的紫红色消失,静置、分层,分液操作时,将含碘元素的碱溶液从仪器的_______ (填“上”、“下”)口倒入烧杯中;
③边搅拌边加入几滴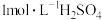 溶液,溶液立即转为棕黄色,并析出碘晶体。
溶液,溶液立即转为棕黄色,并析出碘晶体。
(5)本实验中可以循环利用的物质是_______ (填化学式)。
I.从海水中提取食盐和溴的过程如下:

(1)以上步骤I中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
 ,利用了溴的
,利用了溴的(2)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:
Ⅱ.海藻中富含碘元素。某化学兴趣小组的同学在实验室里用灼烧海藻的灰分提取碘,流程如图:

请回答下列问题:
(3)操作②选用
 的理由是_______(填标号)。
的理由是_______(填标号)。A. 不溶于水 不溶于水 | B. 的密度比水大 的密度比水大 |
C.碘在 中比在水中溶解度更大 中比在水中溶解度更大 | D. 与碘水不反应 与碘水不反应 |
 和
和 ,有关化学方程式为:
,有关化学方程式为:碱性条件:
 。
。酸性条件:
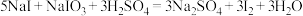 。
。以下是反萃取过程的操作,请按要求填空:
①向装有
 的
的 溶液的
溶液的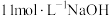 溶液;
溶液;②振荡至溶液的紫红色消失,静置、分层,分液操作时,将含碘元素的碱溶液从仪器的
③边搅拌边加入几滴
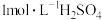 溶液,溶液立即转为棕黄色,并析出碘晶体。
溶液,溶液立即转为棕黄色,并析出碘晶体。(5)本实验中可以循环利用的物质是
您最近半年使用:0次



