Mg在CO2中燃烧的反应可用于火星电站发电、人员取暖等,反应的化学方程式为2Mg+CO2 2MgO+C。
2MgO+C。
(1)做氧化剂的物质是___________ ,Mg被___________ (填“氧化”或“还原”),碳元素的化合价___________ (填“升高”或“降低”)。
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是___________ mol,转移电子的物质的量是___________ mol。
 2MgO+C。
2MgO+C。(1)做氧化剂的物质是
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是
更新时间:2024-03-17 23:01:46
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】实验和理论是学习化学的两种重要途径,按要求回答下列问题:
Ⅰ.硫酸型酸雨的形成有如下可能的反应途径:
途径①:SO2+H2O=H2SO3,O2+2H2SO3 2H2SO4;
2H2SO4;
途径②:2SO2+O2 2SO3,SO3+H2O=H2SO4。
2SO3,SO3+H2O=H2SO4。
(1)上述反应中作氧化剂的是___________ (填化学式)。
(2)已知二氧化硫可与硫化氢气体反应,反应的化学方程式为SO2+2H2S=3S↓+2H2O。请用单线桥法标出电子转移的方向和数目:___________ 。被氧化与被还原的元素的质量之比为___________ 。
(3)SO2与CO2性质相似,均可与澄清石灰水反应,产生白色沉淀,将少量的SO2气体通入澄清石灰水中,写出该反应的离子方程式:___________ 。
Ⅱ.某地有瓶溶液只含C1-、 、
、 ,Ag+、Na+、Cu2+六种离子中的某几种,为确定离子种类做了如下实验:
,Ag+、Na+、Cu2+六种离子中的某几种,为确定离子种类做了如下实验:
①取少量原溶液于试管A中,观察,溶液呈无色。
②试管A中加入足量BaCl2溶液,有白色沉淀生成,再加稀硝酸,沉淀完全溶解。
③取②反应后的澄清溶液于试管B中,加入AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
(4)试分析原溶液中一定含有的离子是___________ ,一定不含有的离子是___________ ,可能含有的离子是___________ 。
Ⅰ.硫酸型酸雨的形成有如下可能的反应途径:
途径①:SO2+H2O=H2SO3,O2+2H2SO3
 2H2SO4;
2H2SO4;途径②:2SO2+O2
 2SO3,SO3+H2O=H2SO4。
2SO3,SO3+H2O=H2SO4。(1)上述反应中作氧化剂的是
(2)已知二氧化硫可与硫化氢气体反应,反应的化学方程式为SO2+2H2S=3S↓+2H2O。请用单线桥法标出电子转移的方向和数目:
(3)SO2与CO2性质相似,均可与澄清石灰水反应,产生白色沉淀,将少量的SO2气体通入澄清石灰水中,写出该反应的离子方程式:
Ⅱ.某地有瓶溶液只含C1-、
 、
、 ,Ag+、Na+、Cu2+六种离子中的某几种,为确定离子种类做了如下实验:
,Ag+、Na+、Cu2+六种离子中的某几种,为确定离子种类做了如下实验:①取少量原溶液于试管A中,观察,溶液呈无色。
②试管A中加入足量BaCl2溶液,有白色沉淀生成,再加稀硝酸,沉淀完全溶解。
③取②反应后的澄清溶液于试管B中,加入AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
(4)试分析原溶液中一定含有的离子是
您最近一年使用:0次
【推荐2】氧化还原反应是重要的化学反应类型,在生活、生产、科研领域都有广泛得应用,请回答以下问题。
(1)人体正常的血红蛋白含有 ,若误食亚硝酸盐会导致血红蛋白中的
,若误食亚硝酸盐会导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:
而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:___________ 、___________ (填“氧化性”或“还原性”)。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体 。
。
①将方程式补充完整:___________
___________NaClO+___________HCl(浓)=___________NaCl+___________ ↑+___________
↑+___________
②该反应中氧化剂是___________ (填化学式),氧化产物与还原产物个数比为___________ 。
(3)砒霜( )可与
)可与 反应:
反应: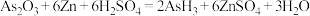 。
。
每生成1个 分子转移
分子转移___________ 个电子。
(4)金属钛具有熔点高、硬度大,常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。在工业上常采用金属钠还原熔融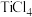 的方法制取:
的方法制取:  ,用单线桥法表示该反应电子转移的方向和数目
,用单线桥法表示该反应电子转移的方向和数目___________ 。
(1)人体正常的血红蛋白含有
 ,若误食亚硝酸盐会导致血红蛋白中的
,若误食亚硝酸盐会导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:
而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体
 。
。①将方程式补充完整:
___________NaClO+___________HCl(浓)=___________NaCl+___________
 ↑+___________
↑+___________
②该反应中氧化剂是
(3)砒霜(
 )可与
)可与 反应:
反应: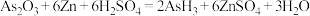 。
。每生成1个
 分子转移
分子转移(4)金属钛具有熔点高、硬度大,常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。在工业上常采用金属钠还原熔融
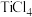 的方法制取:
的方法制取:  ,用单线桥法表示该反应电子转移的方向和数目
,用单线桥法表示该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。反应化学方程式为:3C+2K2Cr2O7 +8H2SO4 = 3CO2↑+2K2SO4+2Cr2(SO4)3 +8H2O
(1)上述反应中氧化剂是______ (填化学式),被氧化的元素是_____ (填元素符号)。
(2)H2SO4在上述反应中表现出来的性质是________ (填选项编号)
A.氧化性 B.氧化性和酸性 C.还原性和酸性 D.酸性
(3)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为_______ L。
(4)请用双线桥法 标出电子转移的方向和数目_____________ 。
(1)上述反应中氧化剂是
(2)H2SO4在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.还原性和酸性 D.酸性
(3)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为
(4)请用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为
 ;请回答下列问题(不考虑氢、氧的氧化还原):
;请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时,正极的电极反应式是_______ ;当外电路通过1mol电子时,理论上负极板的质量增加_______ g。
(2)在完全放电耗尽 和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
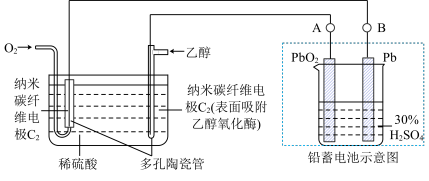
①生物燃料电池(BFC)中 极的电极反应式为:
极的电极反应式为:_______ 。
②在A电极上生成_______ 。
(3) 不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出
不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出 ,并用纯碱吸收。
,并用纯碱吸收。
① 与氢溴酸反应的离子方程式为
与氢溴酸反应的离子方程式为_______ 。
②碱吸收溴的主要反应是 ,吸收1mol
,吸收1mol  时,转移的电子数为
时,转移的电子数为_______ mol。
③请写出 溶液与足量的澄清石灰水反应的离子方程式
溶液与足量的澄清石灰水反应的离子方程式_______ 。

 ;请回答下列问题(不考虑氢、氧的氧化还原):
;请回答下列问题(不考虑氢、氧的氧化还原):(1)放电时,正极的电极反应式是
(2)在完全放电耗尽
 和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
①生物燃料电池(BFC)中
 极的电极反应式为:
极的电极反应式为:②在A电极上生成
(3)
 不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出
不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出 ,并用纯碱吸收。
,并用纯碱吸收。①
 与氢溴酸反应的离子方程式为
与氢溴酸反应的离子方程式为②碱吸收溴的主要反应是
 ,吸收1mol
,吸收1mol  时,转移的电子数为
时,转移的电子数为③请写出
 溶液与足量的澄清石灰水反应的离子方程式
溶液与足量的澄清石灰水反应的离子方程式
您最近一年使用:0次
【推荐2】有以下反应方程式:
A.CuO+H2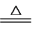 Cu+H2O
Cu+H2O
B.2KClO3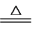 2KCl+3O2↑
2KCl+3O2↑
C.Cl2+2NaOH==NaCl+NaClO+H2O
D.2FeBr2+3Cl2=2FeCl3+2Br2
E.MnO2+4HCl(浓)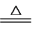 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
F.KClO3+6HCl(浓)=KC1+3H2O+3Cl2↑
G.HgS+O2=Hg+SO2
I.按要求将上述化学方程式序号填入相应空格内:
(1)一种单质使一种化合物中的一种元素被还原____________________ ;
(2)同一种物质中,同种元素间发生氧化还原反应________________ ;
(3)所有元素均参加氧化还原反应的是____________________________ 。
II.已知方程式F:KClO3+6HCI(浓)=KCl+3H2O+3Cl2↑。
(1)请用双线桥法标出电子转移的方向和数目_______________________ ;
(2)标准状况下当有33.6L的氯气放出时,转移电子的数目是_________________________ ;
(3)上述反应中氧化产物和还原产物的质量比为____________________________ 。
A.CuO+H2
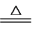 Cu+H2O
Cu+H2OB.2KClO3
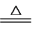 2KCl+3O2↑
2KCl+3O2↑C.Cl2+2NaOH==NaCl+NaClO+H2O
D.2FeBr2+3Cl2=2FeCl3+2Br2
E.MnO2+4HCl(浓)
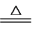 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2OF.KClO3+6HCl(浓)=KC1+3H2O+3Cl2↑
G.HgS+O2=Hg+SO2
I.按要求将上述化学方程式序号填入相应空格内:
(1)一种单质使一种化合物中的一种元素被还原
(2)同一种物质中,同种元素间发生氧化还原反应
(3)所有元素均参加氧化还原反应的是
II.已知方程式F:KClO3+6HCI(浓)=KCl+3H2O+3Cl2↑。
(1)请用双线桥法标出电子转移的方向和数目
(2)标准状况下当有33.6L的氯气放出时,转移电子的数目是
(3)上述反应中氧化产物和还原产物的质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空。
(1)钠元素在自然界都以化合物的形式存在。过氧化钠中氧元素的化合价为___________ 价,焰色试验为___________ 色(填颜色)。过氧化钠用于呼吸面具的反应方程式为①___________ ,②___________ 。上述任一个反应中,若有1molO2生成,转移的电子数目为___________ 个。(用含NA的表达式作答)
(2)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ 。

(3)已知NH3和Cl2在常温下可以快速发生反应:8NH3+3Cl2=N2+6NH4Cl;化工厂利用该原理,可用浓氨水来检验输送氯气的管道是否漏气,请按要求回答下列问题:
①9.03×1023个NH3分子其物质的量为___________ mol,含有___________ mol电子。
②用“双线桥”标出该反应8NH3+3Cl2═N2+6NH4Cl电子转移的方向和数目___________ ,当反应有14gN2生成时,参加反应的NH3物质的量为___________ mol。
(1)钠元素在自然界都以化合物的形式存在。过氧化钠中氧元素的化合价为
(2)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

(3)已知NH3和Cl2在常温下可以快速发生反应:8NH3+3Cl2=N2+6NH4Cl;化工厂利用该原理,可用浓氨水来检验输送氯气的管道是否漏气,请按要求回答下列问题:
①9.03×1023个NH3分子其物质的量为
②用“双线桥”标出该反应8NH3+3Cl2═N2+6NH4Cl电子转移的方向和数目
您最近一年使用:0次



