钠的化合物是化工生产与科学研究的重要组成部分。
(1)将Na、 、
、 、NaOH长时间露置在空气中,最终都会变为
、NaOH长时间露置在空气中,最终都会变为______ (填化学式)。
(2)探究某 样品是否已经变质:取少量
样品是否已经变质:取少量 样品,将其溶于水,加入
样品,将其溶于水,加入 溶液,充分振荡后,观察到
溶液,充分振荡后,观察到_______ (填实验现象),则说明 样品已经与空气中的
样品已经与空气中的 发生反应变质。
发生反应变质。
(3)“神舟号”载人航天器的返回舱内,为防止 浓度过大引起宇航员困乏,可用
浓度过大引起宇航员困乏,可用 降低
降低 的浓度,有关反应的化学方程式为
的浓度,有关反应的化学方程式为_______ ;用 (超氧化钾)代替
(超氧化钾)代替 也能达到同样的目的,反应产物也很相似,试计算用
也能达到同样的目的,反应产物也很相似,试计算用 和
和 分别与
分别与 反应,产生等质量的
反应,产生等质量的 ,所需
,所需 和
和 的质量比为
的质量比为_____ (填最简整数比)。
(4)食品工业经常把 和
和 用作膨松剂,室温下向含某膨松剂试样(
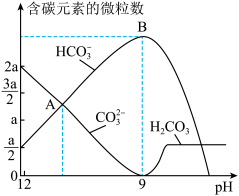
用作膨松剂,室温下向含某膨松剂试样(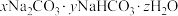 )的溶液中逐滴加入稀盐酸,反应过程中含碳元素的微粒数随pH变化的图像如图所示。(已知:
)的溶液中逐滴加入稀盐酸,反应过程中含碳元素的微粒数随pH变化的图像如图所示。(已知: 因有逸出未画出;
因有逸出未画出; 与少量盐酸发生下列反应:
与少量盐酸发生下列反应: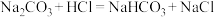 )。
)。
①x:y=____ 。
②图中B点溶液溶质的主要成分为_______ (填化学式),B点后发生反应的离子方程式为______ 。
(1)将Na、
 、
、 、NaOH长时间露置在空气中,最终都会变为
、NaOH长时间露置在空气中,最终都会变为(2)探究某
 样品是否已经变质:取少量
样品是否已经变质:取少量 样品,将其溶于水,加入
样品,将其溶于水,加入 溶液,充分振荡后,观察到
溶液,充分振荡后,观察到 样品已经与空气中的
样品已经与空气中的 发生反应变质。
发生反应变质。(3)“神舟号”载人航天器的返回舱内,为防止
 浓度过大引起宇航员困乏,可用
浓度过大引起宇航员困乏,可用 降低
降低 的浓度,有关反应的化学方程式为
的浓度,有关反应的化学方程式为 (超氧化钾)代替
(超氧化钾)代替 也能达到同样的目的,反应产物也很相似,试计算用
也能达到同样的目的,反应产物也很相似,试计算用 和
和 分别与
分别与 反应,产生等质量的
反应,产生等质量的 ,所需
,所需 和
和 的质量比为
的质量比为(4)食品工业经常把
 和
和 用作膨松剂,室温下向含某膨松剂试样(
用作膨松剂,室温下向含某膨松剂试样(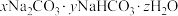 )的溶液中逐滴加入稀盐酸,反应过程中含碳元素的微粒数随pH变化的图像如图所示。(已知:
)的溶液中逐滴加入稀盐酸,反应过程中含碳元素的微粒数随pH变化的图像如图所示。(已知: 因有逸出未画出;
因有逸出未画出; 与少量盐酸发生下列反应:
与少量盐酸发生下列反应: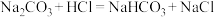 )。
)。①x:y=
②图中B点溶液溶质的主要成分为

更新时间:2024-03-18 12:20:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】.现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为______________________
(2)该气体所含原子总数为_____________________ 个。
利用“化学计量在实验中的应用”的相关知识进行填空
(3)含有6.02×1023个氧原子的H2SO4的物质的量是_______________
(4)与标准状况下VLCO2所含氧原子数目相同的水的质量是___________
(5)在一定的温度和压强下,1体积X2(g)跟3体积Y2(g)化合生成2体积化合物,则该化合物的化学式是____________________
(6)三种正盐的混合溶液中含有0.2 mol Na+、0.25 mol Mg2+、0.4 mol Cl-、SO42—,则n(SO42—)为__________________
(1)该气体的物质的量为
(2)该气体所含原子总数为
利用“化学计量在实验中的应用”的相关知识进行填空
(3)含有6.02×1023个氧原子的H2SO4的物质的量是
(4)与标准状况下VLCO2所含氧原子数目相同的水的质量是
(5)在一定的温度和压强下,1体积X2(g)跟3体积Y2(g)化合生成2体积化合物,则该化合物的化学式是
(6)三种正盐的混合溶液中含有0.2 mol Na+、0.25 mol Mg2+、0.4 mol Cl-、SO42—,则n(SO42—)为
您最近一年使用:0次
【推荐2】钠及其化合物在生产、生活中有着重要的应用。
(1)钠是一种银白色的金属,取2.3g钠块在干燥空气中放置一段时间后,其表面会失去金属光泽生成 ,此时固体质量为2.46g,则原钠块中已被氧化的钠为
,此时固体质量为2.46g,则原钠块中已被氧化的钠为_______ mol;再将该钠块在干燥空气中充分加热,会得到浅黄色的_______ (填化学式)粉末;经过上述两步实验后,最终得到的粉末的质量应为_______ g。
(2)某课外小组为了验证 和
和 的稳定性,设计如下图所示的实验装置
的稳定性,设计如下图所示的实验装置

①为使实验更具有说服力,你认为在试管A中最好放物质_______ (填化学式),在AB试管中能发生的反应的化学方程式为_______ 。
②实验时,C、D两个烧杯中的现象分别是_______ ,可以证明碳酸钠比碳酸氢钠稳定。
(1)钠是一种银白色的金属,取2.3g钠块在干燥空气中放置一段时间后,其表面会失去金属光泽生成
 ,此时固体质量为2.46g,则原钠块中已被氧化的钠为
,此时固体质量为2.46g,则原钠块中已被氧化的钠为(2)某课外小组为了验证
 和
和 的稳定性,设计如下图所示的实验装置
的稳定性,设计如下图所示的实验装置
①为使实验更具有说服力,你认为在试管A中最好放物质
②实验时,C、D两个烧杯中的现象分别是
您最近一年使用:0次
【推荐3】I、FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
(1)该反应中的还原剂是______________ 。
(2)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________ (填字母)。
A.亚硝酸盐被氧化 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
II、二氧化氯(ClO2)气体也是一种常用的自来水消毒剂。
(3)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原氯酸钠,可较安全地生成ClO2,反应的离子方程式为_____________ 。
(4)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法作如下检测(已知ClO2存在于pH为4~6的溶液中,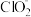 存在于中性溶液中):
存在于中性溶液中):
①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:_________ 。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL,该水样中ClO2的浓度是________ mg·L-1。
(1)该反应中的还原剂是
(2)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被氧化 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
II、二氧化氯(ClO2)气体也是一种常用的自来水消毒剂。
(3)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原氯酸钠,可较安全地生成ClO2,反应的离子方程式为
(4)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法作如下检测(已知ClO2存在于pH为4~6的溶液中,
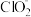 存在于中性溶液中):
存在于中性溶液中):①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL,该水样中ClO2的浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据题目信息,按要求完成下列填空:
(1)过氧化钠粉末与水反应的化学方程式:_____ 。
(2)实验室制取氨气(两种固体加热)的化学方程式:_____ 。
(3)二氧化硫通入溴水,可使溴水褪色,写出反应的化学方程式:_____ 。
(4)铜与浓硫酸加热条件下反应的化学方程式:_____ 。
(5)实验室制取氯气,多余的氯气可用氢氧化钠溶液吸收,写出反应的离子方程式:_____ 。
(6)三氟化氮(NF3)是一种无色无味的气体,27.0mLNF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:_____ 。
(1)过氧化钠粉末与水反应的化学方程式:
(2)实验室制取氨气(两种固体加热)的化学方程式:
(3)二氧化硫通入溴水,可使溴水褪色,写出反应的化学方程式:
(4)铜与浓硫酸加热条件下反应的化学方程式:
(5)实验室制取氯气,多余的氯气可用氢氧化钠溶液吸收,写出反应的离子方程式:
(6)三氟化氮(NF3)是一种无色无味的气体,27.0mLNF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知钠、氯及其化合物间有如下转化关系,请按要求填空。
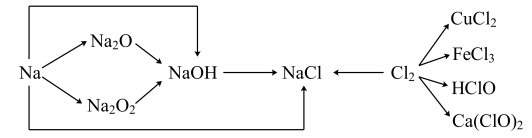
(1)一小块金属钠投入水中反应的化学方程式是___________ 。若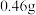 金属钠完全与水反应,可产生标准状况下H2的体积是
金属钠完全与水反应,可产生标准状况下H2的体积是___________ L,若反应后所得溶液为 ,则
,则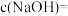
___________  。
。
(2) 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为___________ 、___________ 。
(3)新制的氯水中加入打磨过的镁条,观察到的现象是___________ ;请写出氯气与水反应的化学方程式:___________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为___________ 。

(1)一小块金属钠投入水中反应的化学方程式是
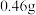 金属钠完全与水反应,可产生标准状况下H2的体积是
金属钠完全与水反应,可产生标准状况下H2的体积是 ,则
,则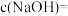
 。
。(2)
 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为(3)新制的氯水中加入打磨过的镁条,观察到的现象是
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)请选择物质,用序号填空:①新制氯水、②铁、③铜、④稀硫酸。将Fe2+转化为Fe3+,可选用的物质___ ;将Fe3+转化为Fe2+,可选用的物质___ 。
(2)在鲜活鱼的长途运输中,必须考虑以下几点:水中需要保持适量的O2;及时除去鱼排出的CO2;防止细菌的大量繁殖。现有两种在水中起供氧灭菌作用的物质,其性能如下:
过氧化钠(Na2O2):易溶于水,与水反应生成NaOH和O2。
过氧化钙(CaO2):微溶于水,与水反应生成Ca(OH)2(微溶)和O2。
根据以上介绍,你认为运输鲜活水产时应选择___ (填过氧化钠或过氧化钙)加入水中,原因是___ 。
(3)NaHCO3的俗名为___ ,Na2CO3和NaHCO3都属于___ 类(填酸、碱或盐),在生活中却被用作食用碱;往饱和的碳酸钠溶液中通入CO2,化学方程式为:___ 。
(2)在鲜活鱼的长途运输中,必须考虑以下几点:水中需要保持适量的O2;及时除去鱼排出的CO2;防止细菌的大量繁殖。现有两种在水中起供氧灭菌作用的物质,其性能如下:
过氧化钠(Na2O2):易溶于水,与水反应生成NaOH和O2。
过氧化钙(CaO2):微溶于水,与水反应生成Ca(OH)2(微溶)和O2。
根据以上介绍,你认为运输鲜活水产时应选择
(3)NaHCO3的俗名为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。
(1)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打溶液与氢氧化钠溶液反应的离子方程式:_________ 。
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:_________ 。
(3)有小组同学称取10 g所制备Na2O2的样品(设样品中杂质不参与下列反应),利用下列装置测定Na2O2样品的纯度(夹持仪器省略),已知Na2O2的摩尔质量为78 g/mol。

有同学提出该实验装置存在缺陷,应该在A、B装置之间增加一个盛有饱和 溶液的洗气瓶,该同学想法是否有必要?理由是
溶液的洗气瓶,该同学想法是否有必要?理由是_________ 。倒出量筒内水的体积后,折算成标准状况下O2的体积为1120 mL,计算样品中Na2O2的质量分数约为_________ 。
(4)向30 mL NaOH溶液中逐渐通入一定量的CO2,再向该溶液中逐滴加入2 mol/L盐酸,所加入盐酸的体积(单位为mL)与产生二氧化碳的体积(标准状况下)关系如图所示。
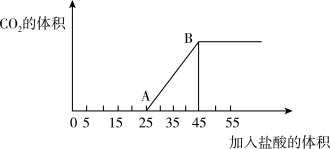
A点溶液中溶质为:_________ ,计算原NaOH溶液的物质的量浓度是_________ mol/L。
(1)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打溶液与氢氧化钠溶液反应的离子方程式:
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:
(3)有小组同学称取10 g所制备Na2O2的样品(设样品中杂质不参与下列反应),利用下列装置测定Na2O2样品的纯度(夹持仪器省略),已知Na2O2的摩尔质量为78 g/mol。

有同学提出该实验装置存在缺陷,应该在A、B装置之间增加一个盛有饱和
 溶液的洗气瓶,该同学想法是否有必要?理由是
溶液的洗气瓶,该同学想法是否有必要?理由是(4)向30 mL NaOH溶液中逐渐通入一定量的CO2,再向该溶液中逐滴加入2 mol/L盐酸,所加入盐酸的体积(单位为mL)与产生二氧化碳的体积(标准状况下)关系如图所示。

A点溶液中溶质为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】写出化学方程式,一步实现下列转变。
(1)Na→NaOH___________
(2)Al2O3→AlCl3___________
(3)Fe(OH)2→Fe(OH)3___________
(4)Na2O2→Na2CO3___________
(1)Na→NaOH
(2)Al2O3→AlCl3
(3)Fe(OH)2→Fe(OH)3
(4)Na2O2→Na2CO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了下图的实验装置。B中盛有饱和碳酸氢钠溶液,目的是除去二氧化碳中混有的氯化氢气体,E为收集氧气装置。
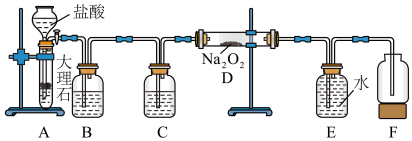
(1)写出装置A中发生反应的化学方程式_______________________________________________ 。
(2)C中盛有____________ ,目的是___________________________________________________ 。
(3)写出装置D中发生反应的化学方程式_______________________________________________ 。
(4)指出装置E的错误___________________________________ 。
(5)写出过氧化钠与水反应的离子反应方程式___________________________________________ 。

(1)写出装置A中发生反应的化学方程式
(2)C中盛有
(3)写出装置D中发生反应的化学方程式
(4)指出装置E的错误
(5)写出过氧化钠与水反应的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)已知NaCl的熔点为801℃,而 (可简写为
(可简写为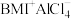 )的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么
)的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么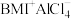 熔点远低于NaCl。
熔点远低于NaCl。_______ 。
(2)实验室中常用氨水吸收过量的 。现有一瓶500ml已经吸收
。现有一瓶500ml已经吸收 的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
a.向A中加入足量的NaOH溶液并加热,将生成的气体先通过碱石灰,再通入盛有过量无水 的装置C中,测量得反应前后装置C增重6.80g。
的装置C中,测量得反应前后装置C增重6.80g。
b.向B中加入足量稀硫酸并加热,将生成的气体先通过浓硫酸,再通入盛有过量碱石灰的装置D中,测量得反应前后装置D增重19.2g。
试回答以下问题:
①原溶液中亚硫酸铵与亚硫酸氢铵物质的量的之比是_______
②用来吸收 的氨水原物质的量浓度为
的氨水原物质的量浓度为_______
(1)已知NaCl的熔点为801℃,而
 (可简写为
(可简写为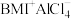 )的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么
)的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么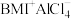 熔点远低于NaCl。
熔点远低于NaCl。(2)实验室中常用氨水吸收过量的
 。现有一瓶500ml已经吸收
。现有一瓶500ml已经吸收 的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);a.向A中加入足量的NaOH溶液并加热,将生成的气体先通过碱石灰,再通入盛有过量无水
 的装置C中,测量得反应前后装置C增重6.80g。
的装置C中,测量得反应前后装置C增重6.80g。b.向B中加入足量稀硫酸并加热,将生成的气体先通过浓硫酸,再通入盛有过量碱石灰的装置D中,测量得反应前后装置D增重19.2g。
试回答以下问题:
①原溶液中亚硫酸铵与亚硫酸氢铵物质的量的之比是
②用来吸收
 的氨水原物质的量浓度为
的氨水原物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】FeCl3是一种重要的化工产品:
(1)电子工业用FeCl3腐蚀铜的原理制造印刷电路板,写出FeCl3与Cu反应的离子方程式: 。
(2)某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ;在此基础上,又进行了定量组成的测定:
①取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g.溶液中c(Cl-)= mol/L。
②再取50.0 mL待测溶液,向其中加入过量稀硝酸,得到0.448 L(标准状况下)一种无色气体.写出反应的离子方程式: ,待测溶液中c(Cu2+)= mol/L。
(1)电子工业用FeCl3腐蚀铜的原理制造印刷电路板,写出FeCl3与Cu反应的离子方程式: 。
(2)某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ;在此基础上,又进行了定量组成的测定:
①取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g.溶液中c(Cl-)= mol/L。
②再取50.0 mL待测溶液,向其中加入过量稀硝酸,得到0.448 L(标准状况下)一种无色气体.写出反应的离子方程式: ,待测溶液中c(Cu2+)= mol/L。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O,相对分子质量392]晶体又称莫尔盐,易溶易电离但却比一般的亚铁盐稳定,因此广泛应用于制药、电镀以及定量分析。回答下列与之有关的问题:
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是______________ ;
②其中处于同主族的两种元素非金属性更强的是:_____________ 。
(2)为检验莫尔盐是否变质,可用的试剂为_______________ 。
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:
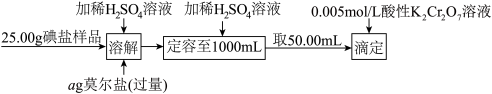
(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:______________________________ 。
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果_____________ (填“偏大”“偏小”或“无影响”)
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是
②其中处于同主族的两种元素非金属性更强的是:
(2)为检验莫尔盐是否变质,可用的试剂为
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:

(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果
您最近一年使用:0次



