X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,相关信息如下:
X最外层电子数是内层电子数的2倍,Y其单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强
(1)元素Y在元素周期表中的位置是_______ 。
(2)Z在氧气中完全燃烧所得产物的电子式为_______ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
已知: 是一种难溶于水的白色物质。
是一种难溶于水的白色物质。
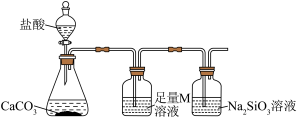
①盛放盐酸和碳酸钙的仪器名称分别是:_______ 、_______ ;M为_______ (填化学式),其作用是_______ 。
②能说明X元素的非金属性比硅元素强的实验现象是_______ 。
(5)元素Z与W相比,金属性较弱的是_______ (填元素名称),请写出能证明这一结论的实验事实_______ (列举一条)。
X最外层电子数是内层电子数的2倍,Y其单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强
(1)元素Y在元素周期表中的位置是
(2)Z在氧气中完全燃烧所得产物的电子式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
已知:
 是一种难溶于水的白色物质。
是一种难溶于水的白色物质。
①盛放盐酸和碳酸钙的仪器名称分别是:
②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
更新时间:2024-04-04 03:40:35
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】请同学们仔细阅读表中内容,并回答下列问题:
(1)写出①的元素符号:________ ;②的原子结构示意图:________ ;③的原子结构示意图:_________ ;④的周期:_______ ;⑤的族:________ 。
(2)甲元素最高价氧化物对应的水化物呈___________ 性(填“酸”或“碱”),乙元素最高价氧化物对应的水化物的化学式为___________ ,甲元素最高价氧化物对应的水化物与乙元素最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(3)甲与乙两元素的单质反应生成的化合物的电子式为___________ 。
(4)甲单质与丙的氢化物反应的化学方程式为______________ 。
元素 | 甲 | 乙 | 丙 |
元素符号 | ① | Cl | O |
原子结构示意图 |
| ② | ③ |
周期 | 三 | ④ | 二 |
族 | ⑤ | VIIA | VIA |
(2)甲元素最高价氧化物对应的水化物呈
(3)甲与乙两元素的单质反应生成的化合物的电子式为
(4)甲单质与丙的氢化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表列出了①~⑩号元素在元素周期表中的位置:
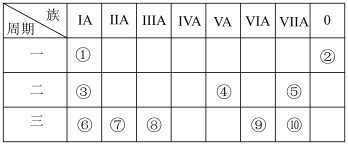
回答下列问题:
(1)①~⑩中,元素的化学性质最不活泼的是_____ (填元素符号,下同)。上述10种元素中,属于金属元素的有_______ 。
(2)写出①与④以原子个数比3:1形成的化合物的电子式:_________ 。
(3)元素④、⑤、⑩分别和①组成的简单化合物中,最稳定的是_______ (填化学式)。
(4)从元素原子得、失电子的角度看,⑤的单质具有_______ (填“氧化性”或“还原性”)。
(5)在盛有氢氧化钠溶液的小烧杯中通入元素⑩的单质,发生反应的离子方程式为_________ 。
(6)请从原子结构的角度解释元素⑥的金属性比元素③的金属性强的原因是________ 。

回答下列问题:
(1)①~⑩中,元素的化学性质最不活泼的是
(2)写出①与④以原子个数比3:1形成的化合物的电子式:
(3)元素④、⑤、⑩分别和①组成的简单化合物中,最稳定的是
(4)从元素原子得、失电子的角度看,⑤的单质具有
(5)在盛有氢氧化钠溶液的小烧杯中通入元素⑩的单质,发生反应的离子方程式为
(6)请从原子结构的角度解释元素⑥的金属性比元素③的金属性强的原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】下表列出了①~⑧所分别代表的八种元素在周期表中的位置,按要求填写下列问题:
(1)①~⑧八种元素中金属性最强的元素是_______ (填元素符号)。
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为_______ 。
(3)元素⑧的原子结构示意图为_______ 。
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为_______ 。
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式_______ 。
(6)第118号元素与⑥为同族元素,它位于元素周期表第_______ 周期。
周期 族 | IA | 0 | ||||||
1 | ① | lIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | |||||
4 | ⑦ | ⑧ |
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为
(3)元素⑧的原子结构示意图为
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式
(6)第118号元素与⑥为同族元素,它位于元素周期表第
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】钛(Ti)是一种性能非常优越的金属,被称为继铝、铁之后的第三金属。某化学兴趣小组设计如下实验探究Mg、Ti、Cu的金属活动性顺序:同温下,取大小相同的这三种金属薄片,分别投入等体积、等物质的量浓度的足量稀盐酸中,实验现象如下表所示。
回答下列问题:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是___________ (填序号)。
①除去氧化膜,利于直接反应
②使反应的金属温度相同
③使表面光亮,易观察现象
(2)写出镁与盐酸反应的离子方程式:___________ 。
(3)根据表中的实验现象可得出三种金属的活动性由强到弱的顺序为___________ ,判断的依据是___________ 。
(4)若将金属钛置于硫酸铜溶液中,可能的现象是___________ 。
| 金属 | Ti | Mg | Cu |
| 实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无明显现象 |
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是
①除去氧化膜,利于直接反应
②使反应的金属温度相同
③使表面光亮,易观察现象
(2)写出镁与盐酸反应的离子方程式:
(3)根据表中的实验现象可得出三种金属的活动性由强到弱的顺序为
(4)若将金属钛置于硫酸铜溶液中,可能的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】比较钠、镁、铝三种元素原子失电子能力的相对强弱
【实验探究1】钠、镁、铝与水的反应
向滴有酚酞的水中分别加入绿豆大小的钠,观察现象;加入用砂纸打磨后的镁条,观察现象,用酒精灯加热后,再观察实验现象;加入用砂纸打磨后的铝条,观察现象,用酒精灯加热后,再观察实验现象。
【实验探究2】镁、铝与酸的反应
向稀盐酸中分别加入加入经砂纸打磨后的镁条和铝条,观察现象和反应的剧烈程度。
【实验探究3】比较NaOH、Mg(OH)2、Al(OH)3三者的碱性强弱
氢氧化铝的化学性质-_______
①与强酸反应(例如,盐酸)
化学方程式:_______
离子方程式:_______
②与强碱反应(例如,氢氧化钠)
化学方程式:_______
离子方程式:_______
【实验探究1】钠、镁、铝与水的反应
向滴有酚酞的水中分别加入绿豆大小的钠,观察现象;加入用砂纸打磨后的镁条,观察现象,用酒精灯加热后,再观察实验现象;加入用砂纸打磨后的铝条,观察现象,用酒精灯加热后,再观察实验现象。
| 单质 | 钠 | 镁 | 铝 |
| 与水反应现象 | 与冷水剧烈反应,产生无色气体,溶液变红 | 与冷水无明显现象,加热后有气泡,溶液变粉红 | 与冷水不反应,加热后与水也极难发生反应 |
| 化学反应方程式 | 2Na+2H2O=2NaOH+H2↑ | Mg+2H2O Mg(OH)2+H2↑ Mg(OH)2+H2↑ | - |
| 结论 | 失电子能力(金属性):Na>Mg>Al | ||
向稀盐酸中分别加入加入经砂纸打磨后的镁条和铝条,观察现象和反应的剧烈程度。
| 单质 | 钠 | 镁 | 铝 |
| 与稀盐酸反应现象 | 与冷水剧烈反应,产生无色气体 | 反应较快,产生无色气体 | 反应较慢,产生无色气体 |
| 化学反应方程式 | 2Na+2HCl=2NaCl+H2↑ | Mg+2HCl=MgCl2+H2↑ | 2Al+6HCl=2AlCl3+3H2↑ |
| 结论 | 失电子能力(金属性):Na>Mg>Al | ||
| 氯化镁 | 氯化铝 | |
| 逐滴滴加氢氧化钠溶液至过量,现象 | 产生白色沉淀,沉淀不消失 | 产生白色沉淀,后白色沉淀溶解 |
| 化学反应方程式 | MgCl2+2NaOH=Mg(OH)2↓+2NaCl | AlCl3+3NaOH=Al(OH)3↓+3NaCl Al(OH)3+NaOH=Na[Al(OH)4] |
| 结论 | 碱性:NaOH>Mg(OH)2>Al(OH)3 | |
①与强酸反应(例如,盐酸)
化学方程式:
离子方程式:
②与强碱反应(例如,氢氧化钠)
化学方程式:
离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】根据表中的①~⑧种元素在周期表中的位置,回答下列问题。

(1)元素③、④形成的简单的离子,半径由大到小是___ (填离子符号)。
(2)用电子式表示元素⑥和⑧的化合物的形成过程:___ 。
(3)元素②的一种核素可以用来考古,请写该核素的中子数是__ ,该元素形成的一种化合物是形成温室效应的主要气体,请写出该化合物的结构式:___ 。
(4)元素⑧的简单气态氢化物是由___ (填“极性”或“非极性”)键形成的。

(1)元素③、④形成的简单的离子,半径由大到小是
(2)用电子式表示元素⑥和⑧的化合物的形成过程:
(3)元素②的一种核素可以用来考古,请写该核素的中子数是
(4)元素⑧的简单气态氢化物是由
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表为元素周期表的一部分,请参照给定元素的位置,回答下列问题:
(1)元素④、⑤、⑥的原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为_______ 。(用化学式表示)
(3)碱性强弱比较:元素⑤的氢氧化物_______ ⑥的氢氧化物(用<、=、>填空);两者相互反应的离子方程式为_______ 。
(4)由元素⑧形成的黄绿色气体单质能和溴化钠溶液发生化学反应,该反应的离子方程式为_______ ;该黄绿色气体单质也会使得湿润淀粉碘化钾试纸变蓝色,表明生成了碘单质(I2),由此推测元素⑧和碘元素形成的气态氢化物的稳定性强弱顺序为:_______ (用化学式表示)。
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为
(3)碱性强弱比较:元素⑤的氢氧化物
(4)由元素⑧形成的黄绿色气体单质能和溴化钠溶液发生化学反应,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】已知X、Y、Z、W、Q、P是短周期的主族元素。如图所示,横坐标表示原子半径相对大小,纵坐标表示化合价(最高正价或最低负价)。回答下列问题:

(1)Y在元素周期表中的位置_______ ;Y的单质化学性质稳定,原因是_______ 。
(2)Q的单质与P的最高价氧化物的水化物发生反应的离子方程式为_______ 。
(3)用电子式表示化合物PZ的形成过程_______ 。
(4)将PX投入水中,可得到X的单质,该反应的化学方程式为_______ 。
(5)Z与W相比较,非金属性较强的是_______ (填元素符号),设计实验证明_______ 。

(1)Y在元素周期表中的位置
(2)Q的单质与P的最高价氧化物的水化物发生反应的离子方程式为
(3)用电子式表示化合物PZ的形成过程
(4)将PX投入水中,可得到X的单质,该反应的化学方程式为
(5)Z与W相比较,非金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是___________________________ 。
(2)C2B的电子式是__________________ 。
(3)B、C、E的离子半径由大到小的顺序为__________________ (用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为_________________ 。
(4)B的气态氢化物与H2S相比沸点高的是_________ (用化学式回答);原因是___________ 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式:_____________ 。
(1)D在元素周期表中的位置是
(2)C2B的电子式是
(3)B、C、E的离子半径由大到小的顺序为
(4)B的气态氢化物与H2S相比沸点高的是
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式:
您最近一年使用:0次
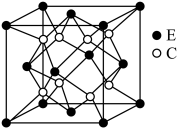
【推荐2】已知A、B、C、D、E和F都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子价电子排布式为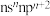 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
(1)元素F的符号是_____ ,基态F原子中有_____ 种能量不同的电子,其价电子轨道表示式为_____ 。
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是_____ 。
(3)从图中可以看出,C跟E形成的离子化合物的化学式为_____ ;E离子配位数为_____ 。
(4) 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为_____ , 是
是_____ (填“极性”或“非极性”)分子。
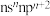 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
(1)元素F的符号是
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是
(3)从图中可以看出,C跟E形成的离子化合物的化学式为
(4)
 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为 是
是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】已知X、Y、Z、W、R五种元素中,X是宇宙中最丰富的元素,Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子最外层电子数比其次外层电子数多4个;W元素原子K层和M层电子总数等于其L层电子数;R元素原子最外层有1个电子,其阳离子与Z的阴离子电子核外电子总数相同。请完成下列问题。
(1)R元素的原子结构示意图为___________ ;由X、Z元素形成的10电子微粒的化学式可能是___________ (写两个)。
(2)含X、Y、Z、R四种元素的化合物属于___________ 。
a.酸 b.钠盐 c.酸式盐 d.碳酸盐 e.碱
(3)W的两种氧化物的分子式是___________ 、___________ 。
(4)13Y和14Y互称为___________ ,二者具有相同的___________ 。
A.质量数 B.中子数 C.化学性质 D.物理性质 E.核电荷数
(5)化合物RZX与Cl2反应的化学方程式为___________ 。
(1)R元素的原子结构示意图为
(2)含X、Y、Z、R四种元素的化合物属于
a.酸 b.钠盐 c.酸式盐 d.碳酸盐 e.碱
(3)W的两种氧化物的分子式是
(4)13Y和14Y互称为
A.质量数 B.中子数 C.化学性质 D.物理性质 E.核电荷数
(5)化合物RZX与Cl2反应的化学方程式为
您最近一年使用:0次