下列关于晶体的说法正确的个数是
①2p、3p、4p能级的轨道数依次增加
②金刚石、NaF、NaCl、H2S、H2O晶体的熔点依次降低
③形成氢键的三个原子不一定在同一条直线上
④晶体中分子间作用力越大,分子越稳定
⑤HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
⑥同周期,与Sc元素未成对电子数相等的元素有3种
⑦基态Cr3+的最高能层中成对电子与未成对电子的数目比为8:3
⑧元素Ge位于周期表第四周期ⅣA族,核外电子排布式为[Ar]4s24p2,属于P区
①2p、3p、4p能级的轨道数依次增加
②金刚石、NaF、NaCl、H2S、H2O晶体的熔点依次降低
③形成氢键的三个原子不一定在同一条直线上
④晶体中分子间作用力越大,分子越稳定
⑤HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
⑥同周期,与Sc元素未成对电子数相等的元素有3种
⑦基态Cr3+的最高能层中成对电子与未成对电子的数目比为8:3
⑧元素Ge位于周期表第四周期ⅣA族,核外电子排布式为[Ar]4s24p2,属于P区
| A.2 | B.3 | C.4 | D.5 |
更新时间:2024-04-01 21:12:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
| A.AB2为V形,则A一定为sp2杂化 |
B. 可与 可与 形成配离子 形成配离子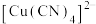 ,1mol该配离子中含有 ,1mol该配离子中含有 键的物质的量为8mol 键的物质的量为8mol |
C.正四面体形分子的键角一定是: |
D.Cr原子的激发态简化电子排布式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列电子排布式或轨道表示式书写正确的是
A.O原子的轨道表示式: |
B.Ca原子的电子排布式: |
C.Cr原子的电子排布式: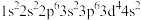 |
D. 的电子排布式: 的电子排布式: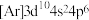 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确的是
①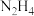 分子中既含极性键又含非极性键
分子中既含极性键又含非极性键
②只要有化学键断裂的过程就是化学变化
③干冰升华会破坏共价键
④水分子很稳定是由于水分子之间存在共价键
⑤ 、
、 、
、 、
、 分子中各原子最外层均达到8电子稳定结构
分子中各原子最外层均达到8电子稳定结构
⑥ 固体中的阴离子和阳离子个数比是1:2
固体中的阴离子和阳离子个数比是1:2
①
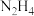 分子中既含极性键又含非极性键
分子中既含极性键又含非极性键②只要有化学键断裂的过程就是化学变化
③干冰升华会破坏共价键
④水分子很稳定是由于水分子之间存在共价键
⑤
 、
、 、
、 、
、 分子中各原子最外层均达到8电子稳定结构
分子中各原子最外层均达到8电子稳定结构⑥
 固体中的阴离子和阳离子个数比是1:2
固体中的阴离子和阳离子个数比是1:2| A.②④⑤ | B.①③④ | C.②③④ | D.③④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.Na2O2和NaOH所含化学键类型完全相同 |
| B.NH3比PH3稳定是因为NH3分子间存在氢键 |
| C.CO2溶于水和干冰升华都只有分子间作用力改变 |
| D.碱性氧化物一定是金属氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关微粒性质的排序中,正确的是
| A.键角:NH3>BF3 | B.熔点:SiO2>CO2 |
| C.酸性:HCOOH<CH3COOH | D.沸点:H2O>H2S>H2Se |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列现象与氢键有关的是( )
①冰的密度比液态水的密度小;②NH3的稳定性比第VA族其他元素的氢化物的高;③尿素的熔沸点比醋酸的高;④水分子在高温下也很稳定;⑤小分子的羧酸、醇可以和水以任意比例互溶;⑥邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低
①冰的密度比液态水的密度小;②NH3的稳定性比第VA族其他元素的氢化物的高;③尿素的熔沸点比醋酸的高;④水分子在高温下也很稳定;⑤小分子的羧酸、醇可以和水以任意比例互溶;⑥邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低
| A.①②③④ | B.①③④⑤ | C.①③⑤⑥ | D.②③⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】近期我国科研人员从连翘果实中分离出一种新的苯乙醇苷衍生物,其结构如图所示,它对肝细胞损伤表现出较强的抑制作用。下列有关该物质说法正确的是
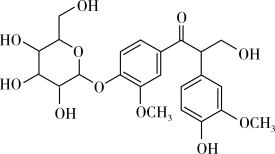

| A.分子中所有碳原子均在同一平面上 |
| B.可与乙醇分子间形成氢键,易溶于乙醇 |
| C.1 mol该物质可发生催化氧化得到5 mol醛基 |
| D.1 mol该物质最多能与6 mol H2发生加成反应 |
您最近一年使用:0次




 生成基态
生成基态 时电子填充的能级为4s
时电子填充的能级为4s

