几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是


A.NaCl中 的配位数大于干冰中CO2分子的配位数 的配位数大于干冰中CO2分子的配位数 |
| B.石墨晶体层内是共价键,层间是范德华力,所以石墨是一种混合型晶体 |
C.若金刚石的晶胞边长为acm,其中两个最近的碳原子之间的距离为 |
| D.CO2晶胞中,CO2分子的排列方式只有1种取向。 |
更新时间:2024-03-22 20:46:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】卤素可形成许多结构和性质特殊的化合物。如  在一定条件下可与
在一定条件下可与  、K反应生成KCl和化合物X。已知 X 晶胞结构如图所示(晶胞参数(
、K反应生成KCl和化合物X。已知 X 晶胞结构如图所示(晶胞参数( 
 其中Cu化合价为
其中Cu化合价为  。下列说法正确的是
。下列说法正确的是
 在一定条件下可与
在一定条件下可与  、K反应生成KCl和化合物X。已知 X 晶胞结构如图所示(晶胞参数(
、K反应生成KCl和化合物X。已知 X 晶胞结构如图所示(晶胞参数( 
 其中Cu化合价为
其中Cu化合价为  。下列说法正确的是
。下列说法正确的是
A.F⁻的最外层电子排布式是  |
| B.晶胞结构示意图中“白球”代表的是Cu |
C.上述反应化学方程式为  |
D.若阿伏加德罗常数的值为NA,则化合物X的密度  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为晶胞的俯视图。已知a点的坐标(0,0,0),b点的坐标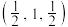 。下列说法正确的是
。下列说法正确的是
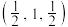 。下列说法正确的是
。下列说法正确的是
A. 的配位数为8 的配位数为8 | B.基态Se核外有34种不同空间运动状态的电子 |
C.晶胞中d点原子分数坐标为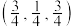 | D.若 换为 换为 ,则晶胞棱长保持不变 ,则晶胞棱长保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关晶体的叙述中,错误的是
| A.干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个 |
| B.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
| C.金属Cu晶体(面心立方晶胞)中,Cu的配位数为8 |
| D.氯化钠晶胞中,阴、阳离子的配位数均为6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关物质结构与性质的说法合理的是
A. 分子的极性强于 分子的极性强于 | B.干冰和冰都采取分子密堆积 |
C. 和 和 中键角都为 中键角都为 | D.邻羟基苯甲酸的沸点低于对羟基苯甲酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是( )
| A.熔融状态下能导电的化合物一定含离子键 |
| B.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| C.H2O2分子中所有的原子均为8电子稳定结构 |
| D.NaHSO4晶体中阴、阳离子的个数是1∶2且熔化时破坏的是离子键和共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】观察下列模型并结合有关信息,判断下列说法不正确的是
| 冰 | NaCl | S8 | HCN | |
| 结构模型示意图 |
|
|
|
|
| 备注 | — | 易溶于CS2 | — |
| A.36g冰中含共价键数目为4NA |
| B.NaCl晶体中每个Na+周围距离最近且相等的Cl-有4个 |
| C.S8分子中的共价键为非极性键 |
| D.HCN分子中含有2个σ键,2个π键 |
您最近一年使用:0次
【推荐1】物质的结构决定其性质。下列实例与解释不相符的是
| 选项 | 实例 | 解释 |
| A | 冠醚(18-冠-6)与K+可以形成超分子 | 冠醚(18-冠-6)的空穴与K+尺寸适配 |
| B | CF3COOH的酸性强于CH3COOH | F的电负性大,增加羧基中的羟基的极性 |
| C | 石墨与金刚石硬度差别大 | 石墨中碳碳键键能小于金刚石中碳碳键键能 |
| D | Fe3+比Fe2+更稳定 | Fe3+的价层电子的3d能级处于半充满稳定状态 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A. 过氧化氢所含的共价键数目为 过氧化氢所含的共价键数目为 |
B.12克石墨含 个 个 键,60克二氧化硅中含 键,60克二氧化硅中含 个 个 |
C.等物质的量的 和 和 中含有 中含有 键的数目均为 键的数目均为 |
D.金刚石晶体中 碳原子含有 碳原子含有 个 个 键 键 |
您最近一年使用:0次

 晶胞结构如图所示,该立方晶胞参数为
晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 或
或 之间的最短距离为
之间的最短距离为







 的P为顶点的晶胞中含两个N,剩余P占据晶胞部分面心,则面心占有率为
的P为顶点的晶胞中含两个N,剩余P占据晶胞部分面心,则面心占有率为